1 . 根据元素周期表中1~20号元素的性质和递变规律,填写下列空白。
(1)属于金属元素的有_____ 种,属于稀有气体元素的有_____ (填元素符号,下同)。
(2)第三周期中,原子半径最大的元素是(稀有气体元素除外)_____ 。
(3)推测 、N的非金属性强弱:
、N的非金属性强弱:_____ 大于_____ 。
(4)第三周期中金属性最强的元素与氧气反应,生成的化合物有_____ (写出两种化合物的化学式)。
(1)属于金属元素的有
(2)第三周期中,原子半径最大的元素是(稀有气体元素除外)
(3)推测
 、N的非金属性强弱:
、N的非金属性强弱:(4)第三周期中金属性最强的元素与氧气反应,生成的化合物有
您最近一年使用:0次
名校
2 . 我国科研团队成功研发“硅—石墨烯—锗晶体管”,代表着我国在这一尖端科技领域走在了世界的前列。
(1)碳元素在元素周期表中的位置是第___ 周期、第IVA族。
(2)硅元素最高价氧化物的化学式为___ 。
(3)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是___ (填字母)。
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
(1)碳元素在元素周期表中的位置是第
(2)硅元素最高价氧化物的化学式为
(3)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
您最近一年使用:0次
名校
解题方法
3 . 下表是元素周期表的一部分,①~⑦代表七种元素,它们在元素周期表中的位置如下。
请回答下列问题:
(1)元素⑥的原子结构示意图为___________ 。
(2)元素②~⑦最高价氧化物的水化物中,碱性最强的是___________ (填化学式)。
(3)②、③、④三种元素中,原子半径最小的是___________ (填元素符号)。
(4)元素①和⑦组成的化合物的水溶液与元素④的单质发生反应,其离子方程式为_______ 。
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ |
请回答下列问题:
(1)元素⑥的原子结构示意图为
(2)元素②~⑦最高价氧化物的水化物中,碱性最强的是
(3)②、③、④三种元素中,原子半径最小的是
(4)元素①和⑦组成的化合物的水溶液与元素④的单质发生反应,其离子方程式为
您最近一年使用:0次
名校
4 . 元素周期表在学习研究中有很重要的作用,如图是元素周期表的一部分。
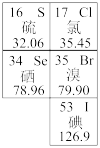
(1)市场上流行一种“富硒鸡蛋”,其中的硒是人体必需的微量元素,硒在元素周期表中的位置是:_______ 。
(2)写出硒元素中子数为46的核素的符号:_______ 。
(3)溴化硒(R)是一种重要的电子元件材料,其分子的球棍模型如图所示。
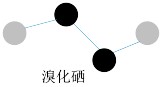
①写出该分子的电子式:_______ 。
②下列说法正确的是_______ (填标号)。
A.R属于离子化合物
B.离子半径:r(Se2-)>r(Cl-)
C.气态氢化物的还原性:H2Se<HCl
D.R分子中只有极性共价键
(4)下列事实不能说明溴元素的非金属性比硒元素强的是_______(填标号)。
(5) 和
和 均可作自来水消毒剂,且消毒时还原产物均为
均可作自来水消毒剂,且消毒时还原产物均为 ,则与8.7g
,则与8.7g 的氧化能力相当的
的氧化能力相当的 的质量为
的质量为_______ g。
(6)据报道, 还可通过
还可通过 与足量的潮湿
与足量的潮湿 固体反应制得,写出该反应的化学方程式
固体反应制得,写出该反应的化学方程式_______ 。
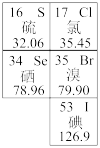
(1)市场上流行一种“富硒鸡蛋”,其中的硒是人体必需的微量元素,硒在元素周期表中的位置是:
(2)写出硒元素中子数为46的核素的符号:
(3)溴化硒(R)是一种重要的电子元件材料,其分子的球棍模型如图所示。

①写出该分子的电子式:
②下列说法正确的是
A.R属于离子化合物
B.离子半径:r(Se2-)>r(Cl-)
C.气态氢化物的还原性:H2Se<HCl
D.R分子中只有极性共价键
(4)下列事实不能说明溴元素的非金属性比硒元素强的是_______(填标号)。
| A.酸性:HBr>H2Se |
| B.化合物Se2Br2中硒显正价而溴显负价 |
| C.在溴水中通入H2Se,有沉淀生成 |
| D.稳定性:H2Se<HBr |
 和
和 均可作自来水消毒剂,且消毒时还原产物均为
均可作自来水消毒剂,且消毒时还原产物均为 ,则与8.7g
,则与8.7g 的氧化能力相当的
的氧化能力相当的 的质量为
的质量为(6)据报道,
 还可通过
还可通过 与足量的潮湿
与足量的潮湿 固体反应制得,写出该反应的化学方程式
固体反应制得,写出该反应的化学方程式
您最近一年使用:0次
名校
解题方法
5 . 表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,根据要求回答问题。
(1)④,⑥的元素符号分别是_______ ,_______ ;
(2)②的原子结构示意图是_______ ;
(3)由①和③两种元素组成的化合物的化学式是_______ ;
(4)④的最高价氧化物水化物的化学式为_______ ;
(5)④和⑤两种元素的金属性强弱顺序是④_______ ⑤(填“<”或“>”)。
族 周期 | IA | II A | IIIA | IV A | VA | VIA | VIIA | |
| 1 | ① | |||||||
| 2 | ② | ③ | Ne | |||||
| 3 | ④ | ⑤ | Al | S | ⑥ |
(1)④,⑥的元素符号分别是
(2)②的原子结构示意图是
(3)由①和③两种元素组成的化合物的化学式是
(4)④的最高价氧化物水化物的化学式为
(5)④和⑤两种元素的金属性强弱顺序是④
您最近一年使用:0次
2021-11-25更新
|
124次组卷
|
2卷引用:陕西省宝鸡市金台区2021-2022学年高二上学期期中考试化学(文)试题
6 . 卤族元素位于元素周期表___ 区。
您最近一年使用:0次
7 . 锰元素在周期表中的位置是___ 。
您最近一年使用:0次
8 . 钡元素在周期表中位于__ (填“s”“d”或“p”)区。
您最近一年使用:0次
9 . 汞的原子序数为80,位于元素周期表第___ 周期第ⅡB族。
您最近一年使用:0次
2021高三·全国·专题练习
10 . 如表所示为元素周期表的一部分,参照元素①~⑩在表中的位置,请回答下列问题:
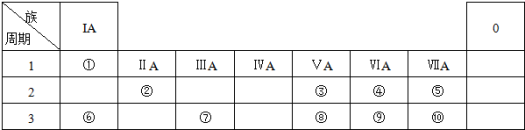
已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式___ 。

已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式
您最近一年使用:0次



