河北省石家庄市保定市2022届高三10月月考化学试题
河北
高三
阶段练习
2021-11-07
365次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、化学与STSE、常见无机物及其应用、化学实验基础、化学反应原理、有机化学基础
河北省石家庄市保定市2022届高三10月月考化学试题
河北
高三
阶段练习
2021-11-07
365次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、化学与STSE、常见无机物及其应用、化学实验基础、化学反应原理、有机化学基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
1. 化学和生活、社会发展息息相关,下列说法正确的是
| A.某团队研发的吸入式新冠疫苗性质稳定,常温下能长期保存 |
| B.CPU制造中的光刻技术是利用光敏树脂在曝光条件下成像,该过程是物理变化 |
| C.三星堆出土的青铜文物表面生成Cu2(OH)3Cl的过程是非氧化还原过程 |
D.聚合硫酸铁  (n<2)是新型絮凝剂,其中Fe显+3价 (n<2)是新型絮凝剂,其中Fe显+3价 |
【知识点】 胶体的性质和应用解读 氧化还原反应定义、本质及特征解读
您最近一年使用:0次
二、多选题 添加题型下试题
多选题
|
适中(0.65)
2. 2021年5月15日,中国“祝融号”火星车确认着陆在火星表面。火星大气层的主要成分是二氧化碳,其次是氮气、氯气,此外还有少量的氧气和水蒸气,下列说法正确的是
A.N2的电子式: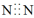 | B.中子数为7的碳原子: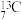 |
C.氧原子的核外电子排布: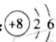 | D.氯气的分子式:Cl2 |
您最近一年使用:0次
三、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
3. 下列有关科技成果解读错误的是
| 选项 | 科技成果 | 相关解读 |
| A | 我国科学家首次利用CO2和H2人工合成淀粉 | 有助于实现碳达峰、碳中和 |
| B | 我国首套吨级氢液化系统研制成功 | 液氢汽化时因断裂化学键而吸热 |
| C | 我国科学家研制出了高强度、高耐蚀镁合金材料(AZ80) | AZ80材料属于金属材料 |
| D | 我国科学家发现磷酸锆可除去核废水中的 Sr Sr |  Sr的中子数与质子数之差为14 Sr的中子数与质子数之差为14 |
| A.A | B.B | C.C | D.D |
【知识点】 原子中相关数值及其之间的相互关系解读 常见合金的组成解读
您最近一年使用:0次
2021-11-01更新
|
430次组卷
|
3卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
单选题
|
较易(0.85)
解题方法
4. 下列有关物质的用途说法错误的是
| A.液氨用作制冷剂 |
| B.铁粉用作富脂食品真空包装中的除氧剂 |
| C.NaClO用作环境消毒剂 |
| D.植物油用作溴、碘的萃取剂 |
您最近一年使用:0次
2021-11-01更新
|
114次组卷
|
2卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
单选题
|
适中(0.65)
名校
5. 在实验室采用如图装置制备并收集气体,下列选项合理的是
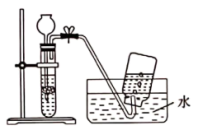

| 化学试剂 | 制备的气体 | |
| A | CaO浓氨水 | NH3 |
| B | Cu+HNO3(浓) | NO2 |
| C | Zn+稀硫酸 | H2 |
| D | MnO2+HCl(浓) | Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-01更新
|
347次组卷
|
4卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
单选题
|
适中(0.65)
6. 已知化学反应A2(g)+B2(g)=2AB(g)的能量变化曲线如图所示,下列叙述正确的是
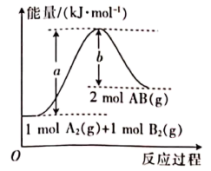

| A.该反应中反应物的总能量高于生成物的总能量 |
| B.该反应的反应热∆H=+(a-b)kJ/mol |
| C.升高温度,图中a、b的值减小,反应速率加快 |
| D.断裂1mol A-A键和1mol B-B键时,放出akJ能量 |
【知识点】 能量的相互转化 吸热反应和放热反应解读 影响化学反应速率的因素
您最近一年使用:0次
2021-11-01更新
|
241次组卷
|
5卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
7. 下列有关传统文化的解读正确的是
| 传统文化摘录 | 化学解读 | |
| A | 蜡烛有心还惜别,替人垂泪到天明 | 蜡烛和蛋白质的主要成分所含元素种类相同 |
| B | 以曾青涂铁,铁赤色如铜 | 氧化性:Cu2+>Fe2+ |
| C | 投泥拨水愈光明,烁玉流金见精悍 | 由煤转化的水煤气燃烧时放出的热量与直接燃煤放出的热量一样多 |
| D | 纷纷灿烂如星陨,赫赫喧豗似火攻 | 焰色反应为化学变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-01更新
|
201次组卷
|
4卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
安徽省部分学校2021-2022学年高三上学期10月联考化学试题河北省石家庄市保定市2022届高三10月月考化学试题福建省龙岩市六县一中2021-2022学年高三上学期期中联考考试化学试题(已下线)卷01 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)
单选题
|
适中(0.65)
名校
8. 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1g D2中含有的质子数为NA |
| B.粗铜电解精炼时,阳极每减少6.4g,阴极就析出铜原子0.1NA |
C.0.1mol/L的K2CO3溶液中CO 、HCO 、HCO 和H2CO3的粒子数之和为0.1NA 和H2CO3的粒子数之和为0.1NA |
| D.40mL 1mol/L硝酸与Fe完全反应(硝酸没有剩余,且气体产物只有NO),转移的电子数为0.03NA |
【知识点】 阿伏加德罗常数的求算解读 铜的电解精炼解读
您最近一年使用:0次
2021-11-01更新
|
353次组卷
|
4卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
单选题
|
适中(0.65)
9. 宏观辨识与微观探析是化学科核心素养之一,下列物质的性质实验对应的反应方程式书写正确的是
A.将铜丝插入FeCl3溶液中: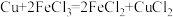 |
B.将Al片加入NaOH溶液中: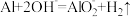 |
C.将SO2通入漂白粉溶液中: |
D.向AlCl3溶液中加入过量氨水: |
【知识点】 离子方程式的书写解读 二氧化硫与其他强氧化剂的反应解读
您最近一年使用:0次
四、多选题 添加题型下试题
多选题
|
适中(0.65)
名校
解题方法
10. 短周期主族元素W、X、Y、Z的原子序数依次增大,X、Z同主族,这四种元素与C、Li形成的某种离子液体的结构式为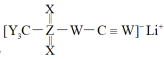 ,下列说法正确的是
,下列说法正确的是
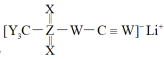 ,下列说法正确的是
,下列说法正确的是| A.最简单氢化物的热稳定性:W<Y |
| B.X分别与W、Y、Z形成化合物时,X的化合价相同 |
| C.将酚酞试液滴入0.1mol/L的Na2Z溶液中,溶液变红 |
| D.该离子液体中各原子最外层电子均满足8电子稳定结构(离子可以看成是带电的原子) |
您最近一年使用:0次
2021-11-02更新
|
1067次组卷
|
3卷引用:河北省石家庄市保定市2022届高三10月月考化学试题
五、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
11. 对下列粒子组在溶液中能否大量共存的判断和分析正确的是
| 选项 | 粒子组 | 判断和分析 |
| A | Na+、K+、ClO-、H2S | 能大量共存,粒子间不反应 |
| B | H+、 、 、 、C2H5OH 、C2H5OH | 能大量共存,粒子间不反应 |
| C | H+、K+、 、SO2 、SO2 | 不能大量共存,能发生反应: |
| D | Na+、 、 、 、 、 | 不能大量共存,能发生反应: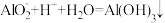 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-02更新
|
364次组卷
|
5卷引用:河北省石家庄市保定市2022届高三10月月考化学试题
单选题
|
适中(0.65)
12. 纳米材料Cu2O在光电领域有广泛应用,以硫酸厂的废渣(主要成分是CuO,含少量的Fe3O4、Fe2O3、SiO2、Al2O3等)为原料制备Cu2O的流程如图所示,已知:“还原”中氧化产物对环境友好。

下列判断正确的是

下列判断正确的是
| A.“酸浸”时未发生氧化还原反应 |
| B.“除杂”得到的滤渣的主要成分是Fe2O3和Al2O3 |
| C.试剂A可能是H2O2 |
| D.制备14.4gCu2O至少需要0.8gN2H4 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
13. 某硅燃料电池的结构如图所示,下列说法错误的是


| A.放电时,溶液的pH保持不变 |
| B.负极上发生的反应为Si-4e-+4OH-=Si(OH)4 |
| C.硅的最终氧化产物是SiO2或硅酸盐,与电解质溶液碱性的强弱有关 |
| D.正极的C在反应过程中也可能会被消耗,一段时间后需要更换 |
您最近一年使用:0次
2021-11-01更新
|
263次组卷
|
5卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
六、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
14. 我国的食品添加剂有多种,如富硒(Se)酵母、二氧化硅、硫黄等,新品种食品添加剂的安全性需通过审查和测试,食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂等,用于食品生产中能更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为___________ ;普通玻璃的主要成分为二氧化硅,用氢氟酸蚀刻普通玻璃时,发生反应的化学方程式为___________ 。
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。
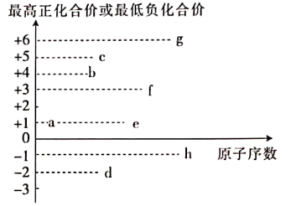
①由a、c、d三种元素形成的离子化合物的化学式为___________ 。
②图中所示元素中金属性最强的是___________ (填元素符号),工业上得到该元素的单质的原理为___________ (填化学方程式)。
③e、f、g元素的简单离子半径由大到小的顺序为___________ (用离子符号回答)。
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为___________ (填化学式)。
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为___________ 。
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。

①由a、c、d三种元素形成的离子化合物的化学式为
②图中所示元素中金属性最强的是
③e、f、g元素的简单离子半径由大到小的顺序为
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为
您最近一年使用:0次
2021-11-05更新
|
416次组卷
|
3卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
安徽省部分学校2021-2022学年高三上学期10月联考化学试题河北省石家庄市保定市2022届高三10月月考化学试题(已下线)解密05 物质结构 元素周期律(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
填空题
|
适中(0.65)
解题方法
15. 1909年,化学家哈伯用N2和H2在高温高压条件下首次合成了氨气,反应原理为 ,该反应的能量变化如图所示(a、b均大于零),回答下列问题:
,该反应的能量变化如图所示(a、b均大于零),回答下列问题:
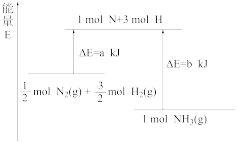
(1)根据图示可知,该反应为___________ (填“吸热”或“放热”)反应,写出生成2molNH3时的热化学方程式:___________ 。
(2)在500℃、30MPa下,断裂1molH-H键、1molN-H键、1molN≡N键需要吸收的能量分别为436kJ、391 kJ、946.5 kJ。
①每消耗0.6molN2时,该反应放出的热量为___________ 。
②向某一密闭容器中充入1.5molH2(g)和0.5molN2(g),在催化剂条件下进行上述反应,此时断裂的H-H吸收的热是___________ (填“>”、“<”或“=”)654kJ,原因是___________ 。
③加入催化剂,该反应的
___________ (填“变大”、“变小”或“不变”),原因是___________ 。
 ,该反应的能量变化如图所示(a、b均大于零),回答下列问题:
,该反应的能量变化如图所示(a、b均大于零),回答下列问题:
(1)根据图示可知,该反应为
(2)在500℃、30MPa下,断裂1molH-H键、1molN-H键、1molN≡N键需要吸收的能量分别为436kJ、391 kJ、946.5 kJ。
①每消耗0.6molN2时,该反应放出的热量为
②向某一密闭容器中充入1.5molH2(g)和0.5molN2(g),在催化剂条件下进行上述反应,此时断裂的H-H吸收的热是
③加入催化剂,该反应的

您最近一年使用:0次
2021-11-02更新
|
157次组卷
|
2卷引用:河北省石家庄市保定市2022届高三10月月考化学试题
七、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
16. 一氧化二氯(Cl2O)在1834年由Antoine Jerome Balard首次合成。实验室制备Cl2O并用水吸收制备次氯酸的实验装置如图所示。
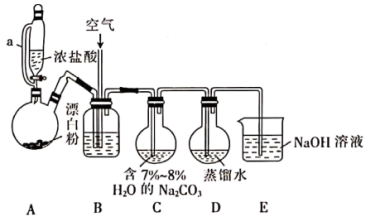
已知: 25℃时Cl2O为棕黄色气体,沸点为2.0℃,易溶于水同时生成次氯酸溶液,在3.8℃时即可逐步分解,与有机物接触时会爆炸,与氧气混合时的爆炸界限为25%。
回答下列问题:
(1)装置A中a管的作用是___________ ,双口烧瓶中发生反应的化学方程式为___________ 。
(2)装置B中盛放的适宜试剂是___________ ,为得到V(Cl2):V(空气)≈1:3的混合气体,可采用的方法是___________ ,实验过程中通空气的目的是___________ 。
(3)装置C、D不用橡皮塞及橡皮管的原因是___________ ,装置C需控温在1~10℃,合适的措施是___________ ,烧瓶中生成Cl2O的化学方程式为___________ 。
(4)装置D得到的是HClO或HClO与氯水的混合溶液,用滴定法测定其中有效氯的浓度。主要实验步骤如下:量取装置 中的溶液amL于碘量瓶中,用适量水稀释,然后加入足量NaI和稀硫酸,置于暗处静置一段时间后,用cmol/L Na2S2O3;标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液VmL。则制得的溶液有效氯的浓度为
中的溶液amL于碘量瓶中,用适量水稀释,然后加入足量NaI和稀硫酸,置于暗处静置一段时间后,用cmol/L Na2S2O3;标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液VmL。则制得的溶液有效氯的浓度为___________ g/L (列出计算式即可,有效氯浓度=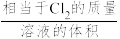 )。
)。

已知: 25℃时Cl2O为棕黄色气体,沸点为2.0℃,易溶于水同时生成次氯酸溶液,在3.8℃时即可逐步分解,与有机物接触时会爆炸,与氧气混合时的爆炸界限为25%。
回答下列问题:
(1)装置A中a管的作用是
(2)装置B中盛放的适宜试剂是
(3)装置C、D不用橡皮塞及橡皮管的原因是
(4)装置D得到的是HClO或HClO与氯水的混合溶液,用滴定法测定其中有效氯的浓度。主要实验步骤如下:量取装置
 中的溶液amL于碘量瓶中,用适量水稀释,然后加入足量NaI和稀硫酸,置于暗处静置一段时间后,用cmol/L Na2S2O3;标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液VmL。则制得的溶液有效氯的浓度为
中的溶液amL于碘量瓶中,用适量水稀释,然后加入足量NaI和稀硫酸,置于暗处静置一段时间后,用cmol/L Na2S2O3;标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液VmL。则制得的溶液有效氯的浓度为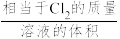 )。
)。
您最近一年使用:0次
2021-11-01更新
|
206次组卷
|
2卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
解答题-工业流程题
|
适中(0.65)
名校
17. 硼酸(H3BO3)广泛用于制玻璃等。以硼镁矿粉(主要成分是Mg2B2O5,含少量的FeO、Fe2O3、SiO2等)为原料制备硼酸的流程如图所示。

已知:H3BO3水溶液中存在 。
。
请回答下列问题:
(1)从绿色化学角度考虑,试剂A宜选择___________ (填标号)。
a.双氧水 b.硝酸 c.氯气
(2)氧化镁的作用是___________ (用离子方程式表示)。
(3)利用上述流程中的___________ (填标号)与碳酸氢铵反应制备MgCO3。
a.固体1 b.固体2 c.溶液1 d.溶液2
(4)在一定温度下,硼镁矿粉与硫酸、蒸馏水按照一定比例混合后搅拌反应。混合体系中液固比(mL/g)对硼浸出率的影响如图所示。最佳液固比为___________ mL/g。当液固比小于4 mL/g时,随着液固比的增大,硼浸出率增大的主要原因是___________ 。

(5)不同温度、pH下硼酸的萃取率如表所示。
表1 硼酸萃取率与温度的关系
表2 硼酸萃取率与pH的关系
萃取硼酸的过程是___________ (填“吸热”或“放热”)过程,pH增大,硼酸萃取率降低的主要原因是___________ 。
(6)硼酸纯度测定。准确称取a g硼酸样品于锥形瓶中,加入适量甘露醇和去氧蒸馏水,再滴滴酚酞溶液,用c mol/L NaOH溶液滴定至溶液呈粉红色,消耗NaOH溶液V1 mL。制备去氧蒸馏水的操作是___________ ;该硼酸样品的纯度为___________ 。

已知:H3BO3水溶液中存在
 。
。请回答下列问题:
(1)从绿色化学角度考虑,试剂A宜选择
a.双氧水 b.硝酸 c.氯气
(2)氧化镁的作用是
(3)利用上述流程中的
a.固体1 b.固体2 c.溶液1 d.溶液2
(4)在一定温度下,硼镁矿粉与硫酸、蒸馏水按照一定比例混合后搅拌反应。混合体系中液固比(mL/g)对硼浸出率的影响如图所示。最佳液固比为

(5)不同温度、pH下硼酸的萃取率如表所示。
表1 硼酸萃取率与温度的关系
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 萃取率/% | 98.9 | 98.7 | 98.5 | 98.3 | 98.1 |
表2 硼酸萃取率与pH的关系
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 萃取率/% | 99 | 99 | 99 | 97 | 95 | 92 | 89 |
萃取硼酸的过程是
(6)硼酸纯度测定。准确称取a g硼酸样品于锥形瓶中,加入适量甘露醇和去氧蒸馏水,再滴滴酚酞溶液,用c mol/L NaOH溶液滴定至溶液呈粉红色,消耗NaOH溶液V1 mL。制备去氧蒸馏水的操作是
【知识点】 物质分离、提纯综合应用解读 常见无机物的制备解读
您最近一年使用:0次
2021-11-02更新
|
272次组卷
|
2卷引用:河北省石家庄市保定市2022届高三10月月考化学试题
试卷分析
整体难度:适中
考查范围:认识化学科学、物质结构与性质、化学与STSE、常见无机物及其应用、化学实验基础、化学反应原理、有机化学基础
试卷题型(共 17题)
题型
数量
单选题
11
多选题
2
填空题
2
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 胶体的性质和应用 氧化还原反应定义、本质及特征 | |
| 3 | 0.85 | 原子中相关数值及其之间的相互关系 常见合金的组成 | |
| 4 | 0.85 | 漂白粉和漂粉精的用途 氨气 铁 萃取和分液 | |
| 5 | 0.65 | 氯气的实验室制法 氨气的实验室制法 二氧化氮 常见气体的制备与收集 | |
| 6 | 0.65 | 能量的相互转化 吸热反应和放热反应 影响化学反应速率的因素 | |
| 7 | 0.85 | 氧化性、还原性强弱的比较 焰色试验 蛋白质 化学科学对人类文明发展的意义 | |
| 8 | 0.65 | 阿伏加德罗常数的求算 铜的电解精炼 | |
| 9 | 0.65 | 离子方程式的书写 二氧化硫与其他强氧化剂的反应 | |
| 11 | 0.65 | 离子方程式的书写 离子共存 | |
| 12 | 0.65 | 氧化还原反应定义、本质及特征 含氧化铝的混合物的提纯 | |
| 13 | 0.65 | 原电池原理理解 新型电池 | |
| 二、多选题 | |||
| 2 | 0.65 | 化学用语综合判断 共价型分子结构式、电子式 元素、核素、同位素 | |
| 10 | 0.65 | 元素周期律、元素周期表的推断 元素周期律的应用 根据原子结构进行元素种类推断 | |
| 三、填空题 | |||
| 14 | 0.65 | 元素周期律、元素周期表的推断 元素周期表提供的元素信息 由元素性质的递变规律进行相关推断 “位构性”关系理解及应用 | |
| 15 | 0.65 | 化学反应热的计算 热化学方程式书写及正误判断 根据△H=反应物的键能之和-生成物的键能之和进行计算 | |
| 四、解答题 | |||
| 16 | 0.65 | 氯气的实验室制法 探究物质组成或测量物质的含量 物质制备的探究 | 实验探究题 |
| 17 | 0.65 | 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |



