名校
解题方法
1 . 下表是元素周期表的一部分,针对表中的①~⑨种元素,回答下列问题:
(1)元素⑥在周期表中的位置是_______ 。
(2)表中的①~⑨种元素,其最高价氧化物对应的水化物酸性最强的含氧酸是_______ (填化学式)。
(3)元素①与⑧形成的化合物属于_______ 化合物(填“共价”或“离子”)。
(4)元素⑤与⑧形成的化合物的电子式_______ ,该化合物是由_______ (填“离子”、“共价”)键形成的。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)元素⑥在周期表中的位置是
(2)表中的①~⑨种元素,其最高价氧化物对应的水化物酸性最强的含氧酸是
(3)元素①与⑧形成的化合物属于
(4)元素⑤与⑧形成的化合物的电子式
您最近一年使用:0次
2022-04-04更新
|
166次组卷
|
2卷引用:湖南省益阳市赫山区箴言中学2020-2021学年高一下学期期末考试化学试题
名校
2 . 1869年俄国科学家门捷列夫绘制出了第一张元素周期表,成为化学史上的里程碑之一,且大大地促进了化学学科的快速发展。下表是现代元素周期表的一部分,请据表回答下列问题:
(1)元素③的名称是___________ ,金属性最强的元素是___________ (填元素符号)。
(2)①②⑤三种元素原子半径由大到小的顺序为___________ (填序号)。
(3)元素⑦的单质的一种用途是___________ (填写“制造玻璃”或“制造计算机芯片”)。
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是___________ (填化学式)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
二 | ① | ② | ③ | ||||
三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)元素③的名称是
(2)①②⑤三种元素原子半径由大到小的顺序为
(3)元素⑦的单质的一种用途是
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是
您最近一年使用:0次
2022-03-16更新
|
640次组卷
|
3卷引用:湖南省长沙市长郡中学2020-2021学年高一下学期期中考试化学试题
名校
3 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:___________ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较Li+与H-的半径大小关系:r(Li+)___________ r(H-)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较Li+与H-的半径大小关系:r(Li+)
您最近一年使用:0次
2022-03-15更新
|
804次组卷
|
4卷引用:北京师范大学附属中学2021-2022学年高二上学期期末考试化学试题
4 . 联合国大会将2019年定为“国际化学元素周期表年” ,显示了元素周期律的重要性。下表列出了7种元素在周期表中的位置:
回答下列问题: 。
(1)⑦的元素符号是___________ ,③的原子结构示意图为___________ 。
(2)上述7种元素中,金属性最强的是___________ ( 填元素符号) ,最高价氧化物对应水化物具有两性的物质是___________ ( 填化学式)。
(3)用“>”、“<”、“=”填空。
(4)③的单质与②的简单氢化物反应的离子方程式为___________ ,
④的单质与③的最高价氧化物对应水化物反应的离子方程式___________ 。
(5)用电子式表示③和⑤形成化合物的过程___________ 。
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | |||||
| 4 | ⑥ | ⑦ | ||||||
(1)⑦的元素符号是
(2)上述7种元素中,金属性最强的是
(3)用“>”、“<”、“=”填空。
| 类别 | 比较 |
| 简单氢化物稳定性 | ① |
| 简单离子半径 | ③ |
| 元素的非金属性 | ⑤ |
④的单质与③的最高价氧化物对应水化物反应的离子方程式
(5)用电子式表示③和⑤形成化合物的过程
您最近一年使用:0次
名校
5 . 下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
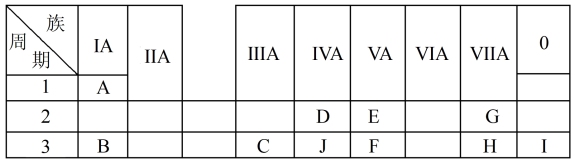
(1)表中元素,化学性质最不活泼的是_______ (填化学名称),只有负价而无正价的元素是_______ (填元素符号)。
(2)34号元素在元素周期表中的位置是_______ 。
(3)H最高价氧化物的化学式为_______ ,G和H氢化物中沸点更高的是_______ ,原因为:_______ 。
(4)A分别与E、G、H形成的化合物中,最稳定的是_______ 。
(5)在B、C、E、F中,原子半径最大的是_______ (填元素符号)。
(6)B、H两种元素所形成的化合物所含的化学键类型为_______ 。
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:_______ 。
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:_______ 。

(1)表中元素,化学性质最不活泼的是
(2)34号元素在元素周期表中的位置是
(3)H最高价氧化物的化学式为
(4)A分别与E、G、H形成的化合物中,最稳定的是
(5)在B、C、E、F中,原子半径最大的是
(6)B、H两种元素所形成的化合物所含的化学键类型为
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:
您最近一年使用:0次
名校
6 . 《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)Be在周期表中的位置:___________ , 10Be和9Be___________ (填序号)。
a. 是同一种原子 b. 具有相同的中子数 c. 具有几乎相同的化学性质 d. 互为同位素
(2)写出Al(OH)3与NaOH溶液反应的化学方程式:___________ 。
(3)研究表明28Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是___________(填序号)。
(1)Be在周期表中的位置:
a. 是同一种原子 b. 具有相同的中子数 c. 具有几乎相同的化学性质 d. 互为同位素
(2)写出Al(OH)3与NaOH溶液反应的化学方程式:
(3)研究表明28Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是___________(填序号)。
| A.比较Mg(OH)2与Al(OH)3的碱性强弱 |
| B.比较这两种元素的最高正化合价 |
| C.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液 |
| D.比较这两种金属的硬度和熔点 |
您最近一年使用:0次
名校
7 . 铁、铝和铜是人类使用最广泛的金属。回答下列问题:
(1)根据电子排布的特点,Al位于元素周期表的__ (填标号,下同),Fe位于元素周期表的__ 。
a.s区 b.p区 c.d区 d.ds区
(2)63Cu和65Cu互称为__ ,在元素周期表中位于第__ 周期,基态Cu+的电子排布式为__ 。
(3)经研究发现目前铁的最高价为+6价,其+6价化合物Na2FeO4在硫酸存在的条件下,可将Mn2+氧化为MnO ,而自身被还原为Fe3+,该反应的离子方程式为
,而自身被还原为Fe3+,该反应的离子方程式为__ 。
(1)根据电子排布的特点,Al位于元素周期表的
a.s区 b.p区 c.d区 d.ds区
(2)63Cu和65Cu互称为
(3)经研究发现目前铁的最高价为+6价,其+6价化合物Na2FeO4在硫酸存在的条件下,可将Mn2+氧化为MnO
 ,而自身被还原为Fe3+,该反应的离子方程式为
,而自身被还原为Fe3+,该反应的离子方程式为
您最近一年使用:0次
2022-01-09更新
|
228次组卷
|
2卷引用:辽宁省辽河油田第二高级中学2021-2022学年高二上学期期中考试化学试题
名校
8 . 下表是元素周期表的一部分,针对表中的①~⑦种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):

(1)在这些元素中,化学性质最不活泼的是___________ (填元素符号),原子结构示意图为___________ 。
(2)元素⑦在周期表中的位置是___________ 。
(3)在元素①③⑥中,与氧气加热条件下反应最不剧烈的单质是___________ (填元素符号),化学方程式为___________ 。
(4)碘位于元素周期表中元素⑦的正下方,其原子序数为___________ ,碘的一种核素含有78个中子,常用于甲状腺功能检查和甲状腺疾病治疗,该核素符号为___________ 。
(5)元素②形成的氧化物中,能造成温室效应的是___________ (填化学式);2mol该氧化物与3mol元素③的最高价氧化物对应的水化物充分反应,所得溶液常温下的pH___________ 7。(用“>”、“<”或“=”作答)

(1)在这些元素中,化学性质最不活泼的是
(2)元素⑦在周期表中的位置是
(3)在元素①③⑥中,与氧气加热条件下反应最不剧烈的单质是
(4)碘位于元素周期表中元素⑦的正下方,其原子序数为
(5)元素②形成的氧化物中,能造成温室效应的是
您最近一年使用:0次
9 . 下表是元素周期表的一部分,根据表中给出的10种元素,按要求作答。
(1)得电子能力最强的原子是___________ ;
(2)化学性质最不活泼的单质是___________ ﹔
(3)F与Cl相比,原子半径较大的是___________ ;
(4) 与
与 相比,热稳定性较强的是
相比,热稳定性较强的是___________ ﹔
(5)原子最外层电子数与最内层电子数相等的元素是___________ ﹔
(6)某阴离子的结构示意图为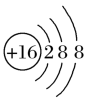 ,其离子符号是
,其离子符号是___________ ;
(7) 与
与 中,能与
中,能与 溶液反应的是
溶液反应的是___________ ﹔
(8)第三周期元素中能与冷水剧烈反应的金属单质是___________ ,写出该反应的化学方程式:___________ ;
(9)碳的一种氢化物结构式为 ,其分子式是
,其分子式是___________ ,其中碳元素与氢元素的质量比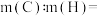
___________ ;(相对原子质量:C-12,H-1)
(10)下列各项性质的比较,符合相关性质递变规律的是___________(填标号 )。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Mg | Al | S | Cl |
(1)得电子能力最强的原子是
(2)化学性质最不活泼的单质是
(3)F与Cl相比,原子半径较大的是
(4)
 与
与 相比,热稳定性较强的是
相比,热稳定性较强的是(5)原子最外层电子数与最内层电子数相等的元素是
(6)某阴离子的结构示意图为
 ,其离子符号是
,其离子符号是(7)
 与
与 中,能与
中,能与 溶液反应的是
溶液反应的是(8)第三周期元素中能与冷水剧烈反应的金属单质是
(9)碳的一种氢化物结构式为
 ,其分子式是
,其分子式是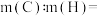
(10)下列各项性质的比较,符合相关性质递变规律的是___________(填
A.还原性: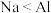 | B.非金属性: |
C.酸性: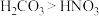 | D.碱性: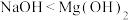 |
您最近一年使用:0次
名校
10 . 下图是元素周期表的一部分,请回答下列问题:
(1)Z元素在元素周期表中位于第_______ 族。
(2)Z的原子半径_______ (填“大于”“小于”或“等于”)Si的原子半径。
(3)Cl元素的非金属性比Z元素的_______ (填“强”或“弱”)。
(4)Z元素的气态氢化物的化学式为_______ 。
(5)P(红磷)与P4(白磷)是由同种元素组成的不同种物质,二者互为_______ (填“同素异形体”“同分异构体”或“同位素”)。
| 2 | ... | N | O | F | Ne |
| 3 | ... | P | Z | Cl | Ar |
(1)Z元素在元素周期表中位于第
(2)Z的原子半径
(3)Cl元素的非金属性比Z元素的
(4)Z元素的气态氢化物的化学式为
(5)P(红磷)与P4(白磷)是由同种元素组成的不同种物质,二者互为
您最近一年使用:0次



