解题方法
1 . a、b、c、d、e为前四周期元素(除稀有气体),原子序数依次增大。a的基态原子价电子层有3个未成对电子;b元素常见的盐可用于纺织、制皂、制玻璃和焙制糕点;c元素的氧化物为共价晶体,具有硬度高、熔点高、难溶于水、化学性质稳定等特点;d元素原子在同周期元素中原子半径最小;e元素在地壳中的含量排在第四位;回答下列问题:
(1)写出e元素在周期表中位置___________ 。a、c、d最高价氧化物水化物的酸性有弱到强的顺序为___________ (用化学式表示)
(2)将一定量 通入b的最高价氧化物对应水化物的溶液中,经一系列操作得到两种固态盐的混合物。现取mg固体混合物充分加热,质量减少ng。则mg固体混合物中热稳定性较低的物质的质量分数为
通入b的最高价氧化物对应水化物的溶液中,经一系列操作得到两种固态盐的混合物。现取mg固体混合物充分加热,质量减少ng。则mg固体混合物中热稳定性较低的物质的质量分数为___________ 。
(3)c元素与d形成化合物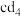 ,
,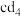 在潮湿空气中可产生白色烟雾,反应剧烈,且不可逆,反应的化学方程式为
在潮湿空气中可产生白色烟雾,反应剧烈,且不可逆,反应的化学方程式为___________ 。
(1)写出e元素在周期表中位置
(2)将一定量
 通入b的最高价氧化物对应水化物的溶液中,经一系列操作得到两种固态盐的混合物。现取mg固体混合物充分加热,质量减少ng。则mg固体混合物中热稳定性较低的物质的质量分数为
通入b的最高价氧化物对应水化物的溶液中,经一系列操作得到两种固态盐的混合物。现取mg固体混合物充分加热,质量减少ng。则mg固体混合物中热稳定性较低的物质的质量分数为(3)c元素与d形成化合物
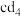 ,
,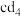 在潮湿空气中可产生白色烟雾,反应剧烈,且不可逆,反应的化学方程式为
在潮湿空气中可产生白色烟雾,反应剧烈,且不可逆,反应的化学方程式为
您最近一年使用:0次
2023-07-15更新
|
55次组卷
|
2卷引用:山东省泰安市宁阳县2022-2023学年高三上学期11月期中考试化学试题
解题方法
2 . 粉煤灰是燃煤电厂的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为38%,还有含量较多的SiO2。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4,有关化学反应方程式:Al6Si2O13+3Na2CO3=2NaAlSiO4+4NaAlO2+3CO2↑,结合上述反应完成填空:
(1)Na2CO3中所含化学键的类型是______ ,SiO2属于______ 晶体。
(2)在上述反应所涉及的元素中,原子核外电子数最多的元素在周期表中的位置是______ 。
(3)上述元素中有三种元素在元素周期表中处于相邻位置,其原子半径从大到小的顺序为______ 。(用元素符号表示)。
(4)二氧化碳分子的结构式为_______ 。
(5)上述元素中有两种元素位于同一主族,可以作为判断两者非金属性强弱的依据的是_____ (填编号)。
a.该两种原子形成的共价键中共用电子对的偏向 b.最高价氧化物熔沸点高低
c.最高价氧化物对应水化物的酸性强弱 d.单质与酸反应的难易程度
(1)Na2CO3中所含化学键的类型是
(2)在上述反应所涉及的元素中,原子核外电子数最多的元素在周期表中的位置是
(3)上述元素中有三种元素在元素周期表中处于相邻位置,其原子半径从大到小的顺序为
(4)二氧化碳分子的结构式为
(5)上述元素中有两种元素位于同一主族,可以作为判断两者非金属性强弱的依据的是
a.该两种原子形成的共价键中共用电子对的偏向 b.最高价氧化物熔沸点高低
c.最高价氧化物对应水化物的酸性强弱 d.单质与酸反应的难易程度
您最近一年使用:0次
3 . 合成氨工艺的一个重要工序是铜洗,其目的是用铜液 醋酸二氨合铜
醋酸二氨合铜 Ⅰ
Ⅰ ,氨水
,氨水 吸收在生产过程中产生的CO和
吸收在生产过程中产生的CO和 等气体,铜液吸收CO的反应是放热反应,其反应方程式为:
等气体,铜液吸收CO的反应是放热反应,其反应方程式为: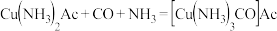 ; 完成下列填空:
; 完成下列填空:
 如果要提高上述反应的反应速率,可以采取的措施是
如果要提高上述反应的反应速率,可以采取的措施是 ______  选填编号
选填编号
 减压
减压  增加
增加 的浓度
的浓度  升温
升温 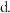 及时移走产物
及时移走产物
 铜液中的氨可吸收二氧化碳,写出该反应的化学方程式:
铜液中的氨可吸收二氧化碳,写出该反应的化学方程式: ______
 简述铜液吸收CO及铜液再生的操作步骤
简述铜液吸收CO及铜液再生的操作步骤 注明吸收和再生的条件
注明吸收和再生的条件 .
.______
 铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为
铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为 ______ 通过比较 ______ 可判断氮、磷两种元素的非金属性强弱.
 已知
已知 与
与 分子结构相似,
分子结构相似, 的电子式是
的电子式是 ______  熔点高于
熔点高于 ,其原因是
,其原因是 ______
 提取的
提取的 中含少量
中含少量 、SO
、SO 。将产品溶解,加入
。将产品溶解,加入 ,加热至沸,再加入
,加热至沸,再加入 溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是
溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是 ______ 。滤渣的主要成分是 ______ 、 ______ .
 称取
称取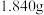 小苏打样品
小苏打样品 含少量
含少量 ,配置成250mL溶液,取
,配置成250mL溶液,取 用
用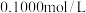 盐酸滴定,消耗盐酸
盐酸滴定,消耗盐酸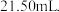 实验中所需的定量仪器出滴定管外,还有
实验中所需的定量仪器出滴定管外,还有 ______ 。选甲基橙而不选酚酞作为指示剂的原因是 ______  样品中
样品中 质量分数为
质量分数为 ______ 。( 保留3位小数)
 将一定量小苏打样品
将一定量小苏打样品 含少量
含少量 溶于足量盐酸,蒸干后称量固体质量,也可测量小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果
溶于足量盐酸,蒸干后称量固体质量,也可测量小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果 ______ 。(选填“偏高”、“偏低”或“不受影响”)
 醋酸二氨合铜
醋酸二氨合铜 Ⅰ
Ⅰ ,氨水
,氨水 吸收在生产过程中产生的CO和
吸收在生产过程中产生的CO和 等气体,铜液吸收CO的反应是放热反应,其反应方程式为:
等气体,铜液吸收CO的反应是放热反应,其反应方程式为: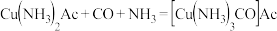 ; 完成下列填空:
; 完成下列填空:  如果要提高上述反应的反应速率,可以采取的措施是
如果要提高上述反应的反应速率,可以采取的措施是  选填编号
选填编号
 减压
减压  增加
增加 的浓度
的浓度  升温
升温  及时移走产物
及时移走产物  铜液中的氨可吸收二氧化碳,写出该反应的化学方程式:
铜液中的氨可吸收二氧化碳,写出该反应的化学方程式:  简述铜液吸收CO及铜液再生的操作步骤
简述铜液吸收CO及铜液再生的操作步骤 注明吸收和再生的条件
注明吸收和再生的条件 .
. 铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为
铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为  已知
已知 与
与 分子结构相似,
分子结构相似, 的电子式是
的电子式是  熔点高于
熔点高于 ,其原因是
,其原因是  提取的
提取的 中含少量
中含少量 、SO
、SO 。将产品溶解,加入
。将产品溶解,加入 ,加热至沸,再加入
,加热至沸,再加入 溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是
溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是  称取
称取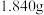 小苏打样品
小苏打样品 含少量
含少量 ,配置成250mL溶液,取
,配置成250mL溶液,取 用
用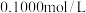 盐酸滴定,消耗盐酸
盐酸滴定,消耗盐酸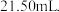 实验中所需的定量仪器出滴定管外,还有
实验中所需的定量仪器出滴定管外,还有  样品中
样品中 质量分数为
质量分数为  将一定量小苏打样品
将一定量小苏打样品 含少量
含少量 溶于足量盐酸,蒸干后称量固体质量,也可测量小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果
溶于足量盐酸,蒸干后称量固体质量,也可测量小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果
您最近一年使用:0次
2019-12-27更新
|
148次组卷
|
2卷引用:2019年秋高三化学复习强化练习—— 酸碱中和滴定
13-14高三上·上海·期末
解题方法
4 . 粉煤灰是燃煤电厂的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为38%,还有含量较多的SiO2。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4,有关化学反应方程式如下:Al6Si2O13+3Na2CO3→2NaAlSiO4+4NaAlO2+3CO2↑
结合上述反应完成下列填空:
(1)上述反应所涉及的元素中,原子核外电子运动状态最多的元素在周期表中的位置是___ ,其氧化物属于___ 晶体。
(2)上述元素中有三种元素在元素周期表中处于相邻位置,其原子半径从大到小的顺序为___ >___ >___ (用元素符号表示)。
(3)二氧化碳分子的空间构型为___ 型,碳酸钠溶液显碱性的原因是(用离子方程式表示)___ 。
(4)上述元素中有两种元素是同一主族,可以作为判断两者非金属性强弱的依据的是___ (填编号)。
a.该两种原子形成的共价键中共用电子对的偏向
b.最高价氧化物熔沸点高低
c.最高价氧化物对应水化物的酸性强弱
d.单质与酸反应的难易程度
结合上述反应完成下列填空:
(1)上述反应所涉及的元素中,原子核外电子运动状态最多的元素在周期表中的位置是
(2)上述元素中有三种元素在元素周期表中处于相邻位置,其原子半径从大到小的顺序为
(3)二氧化碳分子的空间构型为
(4)上述元素中有两种元素是同一主族,可以作为判断两者非金属性强弱的依据的是
a.该两种原子形成的共价键中共用电子对的偏向
b.最高价氧化物熔沸点高低
c.最高价氧化物对应水化物的酸性强弱
d.单质与酸反应的难易程度
您最近一年使用:0次
解题方法
5 . 短周期主族元素X、Y、Z、W原子序数依次增大,Ⅹ是空气中含量最多的元素,Y是海水中质量分数最大的元素,Z元素原子是短周期原子半径最大的,W与X属于同一主族。下列说法正确的是( )
| A.原子半径:W>Z>Y | B.由Y、Z组成的化合物中均不含共价键 |
| C.X的最高价氧化物对应水化物的酸性比W的强 | D.X的简单气态氢化物的热稳定性比Y的强 |
您最近一年使用:0次
6 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X是形成化合物种类最多的元素,Y原子最外层电子数是其内层电子数的2倍,W是地壳中含量最多的元素。下列叙述正确的是
| A.Y与W可以组成YW32-、Y2W42- |
| B.由X、Y、Z、W四种元素组成的既能与酸又能与碱反应的化合物,一定属于α-氨基酸 |
| C.若化合物Y2X4W2能发生银镜反应,则该化合物一定是甲酸甲酯 |
| D.混合物Y7X8、Y3 X8W3中X的质量分数约为8.7% |
您最近一年使用:0次
2010·上海浦东新·一模
解题方法
7 . 现有部分短周期元素的性质或结构如下表:
(1)X原子中电子运动状态共有____ 种。Z元素最简单的气态氢化物分子的空间构型是___ 。
(2)写出Y元素最高价氧化物对应水化物的电离方程式____________ 。
(3)下列说法能证明M、Z、X三种元素形成的化合物属于离子化合物的是______ 。
a.熔点比氯化钠高 b.水溶液能导电 c.液态时能导电 d.固体能导电
(4)与X同周期且非金属性强于X的元素是______ (填元素名称),写出能说明这一事实的化学方程式___________ 。
| 元素编号 | 元素性质或结构 |
| X | 海水中质量分数最大的元素,其氢化物是最常用的溶剂 |
| Y | 地壳中含量最多的金属元素 |
| Z | 形成化合物最多的元素 |
| M | 短周期主族元素中原子半径最大的元素 |
(2)写出Y元素最高价氧化物对应水化物的电离方程式
(3)下列说法能证明M、Z、X三种元素形成的化合物属于离子化合物的是
a.熔点比氯化钠高 b.水溶液能导电 c.液态时能导电 d.固体能导电
(4)与X同周期且非金属性强于X的元素是
您最近一年使用:0次
8 . X、Y、Z、W为短周期原子序数依次增大的四种主族元素,它们的原子半径与原子序数的关系如图所示(横坐标长度不代表具体数据),W单质遇冷水即可剧烈反应。下列说法不正确的是
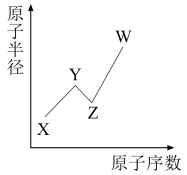

| A.若X、Y、Z均可形成简单阴离子,则离子半径:Y>Z>X |
| B.若Y与W可形成常见的供氧剂,则X与Z形成的化合物水溶液显酸性 |
| C.若Y是形成化合物种类最多的元素,则最简单氢化物的沸点:Y<Z |
| D.若Y和Z是空气中质量分数最大的两种元素,则X、Y、Z只能形成共价化合物 |
您最近一年使用:0次
9 . 短周期元素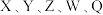 在元素周期表中的相对位置如图所示,其中W原子的质子数是其
在元素周期表中的相对位置如图所示,其中W原子的质子数是其 层电子数的三倍,下列说法不正确的是
层电子数的三倍,下列说法不正确的是
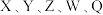 在元素周期表中的相对位置如图所示,其中W原子的质子数是其
在元素周期表中的相对位置如图所示,其中W原子的质子数是其 层电子数的三倍,下列说法不正确的是
层电子数的三倍,下列说法不正确的是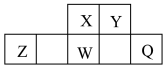
A.简单离子半径: |
B.最高价氧化物对应水化物的酸性: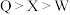 |
C.与 同主族的短周期元素,其最高价氧化物中氧元素的质量分数为 同主族的短周期元素,其最高价氧化物中氧元素的质量分数为 |
D.非金属性 |
您最近一年使用:0次
名校
解题方法
10 . 中药剂砒霜(主要成分为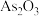 )可用于治疗急性白血病。工业上利用酸性高浓度含砷废水(主要成分是亚砷酸
)可用于治疗急性白血病。工业上利用酸性高浓度含砷废水(主要成分是亚砷酸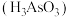 和砷酸
和砷酸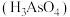 )提取粗
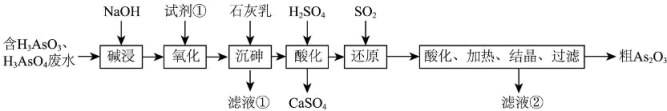
)提取粗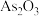 的工艺流程如图所示。回答下列问题:
的工艺流程如图所示。回答下列问题:
已知: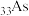 在元素周期表中位置与
在元素周期表中位置与 相邻:
相邻: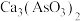 微溶于水,
微溶于水,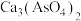 难溶于水。
难溶于水。
(1)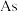 在元素周期表中的位置为
在元素周期表中的位置为______ ;比较酸性强弱:
______ 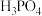 。(填
。(填 或
或 )。
)。
(2)若试剂①选择 ,则“氧化”过程反应中氧化剂与还原剂的物质的量之比是
,则“氧化”过程反应中氧化剂与还原剂的物质的量之比是______ 。
(3)写出“酸化”过程发生反应的化学方程式______ 。
(4)从综合利用的角度看,“滤液②”的主要成分可返回______ 步骤中循环再利用。
(5)还原步骤之后一系列操作,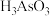 分解为
分解为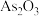 ,结晶得到粗
,结晶得到粗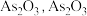 在不同温度和不同浓度硫酸中的溶解度
在不同温度和不同浓度硫酸中的溶解度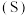 曲线如图所示。为了提高粗
曲线如图所示。为了提高粗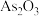 的沉淀率,结晶过程中应控制的条件为
的沉淀率,结晶过程中应控制的条件为______ 。

(6)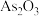 粗产品(含
粗产品(含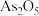 杂质)中
杂质)中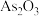 质量分数的测定:称取
质量分数的测定:称取 粗产品溶于适量
粗产品溶于适量 溶液,得到含
溶液,得到含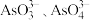 的混合溶液
的混合溶液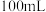 。取
。取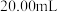 上述溶液与
上述溶液与 的
的 溶液进行反应(碱性环境中
溶液进行反应(碱性环境中 可将
可将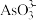 氧化为
氧化为 ),消耗
),消耗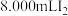 溶液。
溶液。
Ⅰ. 与
与 反应的离子方程式为
反应的离子方程式为______ 。
Ⅱ.粗产品中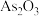 的质量分数为
的质量分数为______ (用含有 的代数式表示)。
的代数式表示)。
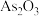 )可用于治疗急性白血病。工业上利用酸性高浓度含砷废水(主要成分是亚砷酸
)可用于治疗急性白血病。工业上利用酸性高浓度含砷废水(主要成分是亚砷酸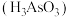 和砷酸
和砷酸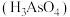 )提取粗
)提取粗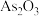 的工艺流程如图所示。回答下列问题:
的工艺流程如图所示。回答下列问题:
已知:
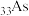 在元素周期表中位置与
在元素周期表中位置与 相邻:
相邻: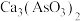 微溶于水,
微溶于水,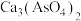 难溶于水。
难溶于水。(1)
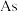 在元素周期表中的位置为
在元素周期表中的位置为
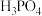 。(填
。(填 或
或 )。
)。(2)若试剂①选择
 ,则“氧化”过程反应中氧化剂与还原剂的物质的量之比是
,则“氧化”过程反应中氧化剂与还原剂的物质的量之比是(3)写出“酸化”过程发生反应的化学方程式
(4)从综合利用的角度看,“滤液②”的主要成分可返回
(5)还原步骤之后一系列操作,
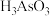 分解为
分解为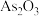 ,结晶得到粗
,结晶得到粗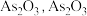 在不同温度和不同浓度硫酸中的溶解度
在不同温度和不同浓度硫酸中的溶解度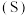 曲线如图所示。为了提高粗
曲线如图所示。为了提高粗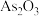 的沉淀率,结晶过程中应控制的条件为
的沉淀率,结晶过程中应控制的条件为
(6)
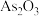 粗产品(含
粗产品(含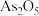 杂质)中
杂质)中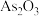 质量分数的测定:称取
质量分数的测定:称取 粗产品溶于适量
粗产品溶于适量 溶液,得到含
溶液,得到含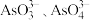 的混合溶液
的混合溶液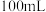 。取
。取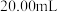 上述溶液与
上述溶液与 的
的 溶液进行反应(碱性环境中
溶液进行反应(碱性环境中 可将
可将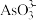 氧化为
氧化为 ),消耗
),消耗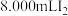 溶液。
溶液。Ⅰ.
 与
与 反应的离子方程式为
反应的离子方程式为Ⅱ.粗产品中
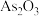 的质量分数为
的质量分数为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次



