名校
解题方法
1 . 短周期元素X、Y、Z、W的原子序数依次增大。X的原子核外有1个电子,Y是地壳中含量最多的元素,Z位于元素周期表第ⅢA族,W单质可广泛用于生产芯片。下列说法正确的是
| A.原子半径:Y<Z<W | B.元素的非金属性:X<Y<W |
| C.W的简单氢化物比Y的稳定 | D.Z单质制成的容器可盛放冷浓硫酸 |
您最近一年使用:0次
解题方法
2 . 下列装置或操作能达到实验目的的是
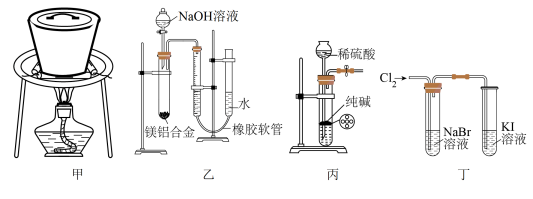
A.甲:用瓷坩埚加热熔化 固体 固体 | B.乙:测定一定质量镁铝合金中金属铝的含量 |
| C.丙:控制二氧化碳气体的生成与停止 | D.丁:验证 非金属性的强弱 非金属性的强弱 |
您最近一年使用:0次
解题方法
3 . X、Y、Z、W是原子序数依次增大的四种短周期元素,最外层电子数之和为17。Y是地壳中含量最多的元素,X、Y形成的某种化合物可表示为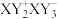 ,Z最外层电子数与K层电子数相等。下列说法错误的是
,Z最外层电子数与K层电子数相等。下列说法错误的是
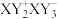 ,Z最外层电子数与K层电子数相等。下列说法错误的是
,Z最外层电子数与K层电子数相等。下列说法错误的是| A.简单离子半径:X>Y>Z | B.X、Y都能与Z形成离子键 |
| C.最简单氢化物的稳定性:W>X | D.Y的最简单氢化物的空间结构是直线形 |
您最近一年使用:0次
名校
4 . X、Y、Z、W为原子序数依次增大的前20号主族元素,且四种元素的原子序数之和为43.X元素被称为“元素之母”,Y的单质是空气中含量最多的成分,W焰色试验的颜色为砖红色。下列说法正确的是
| A.X和W均为元素周期表中的p区元素 |
| B.Y、Z的氧化物对应的水化物均为强酸 |
| C.X和Y形成的二元化合物常温常压下均为气态 |
| D.W所在周期基态原子最高能层电子数为1的元素有3种 |
您最近一年使用:0次
5 . 短周期主族元素X、Y、Z、W、M、T的原子序数依次增大,X的周期序数等于核外电子总数,Y与Z相邻且Z的最外层电子数是次外层的3倍,Z、W的最外层电子数之和与T的最外层电子数相等,M是地壳中含量最多的金属元素。回答下列问题:
(1)Y的元素符号是___________ ,W在元素周期表中的位置___________ 。
(2)Z、W、M、T的简单离子半径从大到小的顺序为___________ (用离子符号表示)。
(3)X、Z、W可形成多种二元化合物,下列说法不正确的是___________(填字母)。
(4)M的氧化物与W的最高价氧化物对应水化物的溶液反应的离子方程式是___________ 。
(5)由X和Y组成的18电子分子Y2X4,该分子的结构式为___________ 。
(6)不能证明T元素的非金属性比碘元素的非金属性强的事实是___________(填序号)。
(1)Y的元素符号是
(2)Z、W、M、T的简单离子半径从大到小的顺序为
(3)X、Z、W可形成多种二元化合物,下列说法不正确的是___________(填字母)。
| A.X2Z2和W2Z2中都含有非极性共价键 |
| B.X、W可形成离子化合物WX,其电子式为:Na+[:H]- |
| C.W2Z、W2Z2溶于X2Z中时,都发生化合反应 |
| D.W2Z2常用于呼吸面具中作为氧气的来源 |
(5)由X和Y组成的18电子分子Y2X4,该分子的结构式为
(6)不能证明T元素的非金属性比碘元素的非金属性强的事实是___________(填序号)。
| A.T的气态氢化物比碘的气态氢化物稳定 |
| B.T的氧化物对应水化物的酸性强于碘的氧化物对应水化物的酸性 |
| C.T的单质能将碘从其钠盐溶液中置换出来 |
| D.T的单质比碘单质更容易与H2反应 |
您最近一年使用:0次
6 . 家中的食品、调味品、洗涤剂和药品等都含有化学物质,以下是胃药和加碘食盐的标签,请回答下列问题。
(1)标签中涉及到的金属元素有___________  ,非金属元素有
,非金属元素有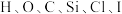 ;
; 在元素周期表中的位置是
在元素周期表中的位置是___________ , 的结构示意图为
的结构示意图为___________ 。
(2)写出由 两种元素组成的常见温室气体的电子式
两种元素组成的常见温室气体的电子式___________ 。
(3)比较下列性质,用“>”、“=”或“<”填空。
①酸性:
___________ 
②还原性:
___________ 
③离子半径: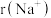
___________ 
(4)用以下对比实验探究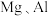 的金属性强弱以及
的金属性强弱以及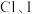 的非金属性强弱。
的非金属性强弱。
| 铝镁咀嚼片 【药品名】铝镁咀嚼片 【成分】氢氧化镁、氢氧化铝、二甲基硅油 【适应症】胃酸过多引起的胃痛、烧心等胃胀气的治疗 | 食用盐 【配料表】精制盐、碘酸钾 【碘含量(以I计)】21mg/kg~39mg/kg 【保质期】36个月 |
 ,非金属元素有
,非金属元素有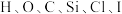 ;
; 在元素周期表中的位置是
在元素周期表中的位置是 的结构示意图为
的结构示意图为(2)写出由
 两种元素组成的常见温室气体的电子式
两种元素组成的常见温室气体的电子式(3)比较下列性质,用“>”、“=”或“<”填空。
①酸性:


②还原性:


③离子半径:
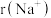

(4)用以下对比实验探究
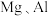 的金属性强弱以及
的金属性强弱以及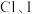 的非金属性强弱。
的非金属性强弱。| 比较Mg、Al金属性强弱 | 比较Cl、I非金属性强弱 |
选择的试剂: 溶液、 溶液、 溶液、氨水、 溶液、氨水、 溶液 溶液 | 选择的试剂:新制氯水、 溶液 溶液 |
操作:向两支试管中分别加入少许 溶液和 溶液和 溶液,然后滴加氨水,直到不再产生白色沉淀 溶液,然后滴加氨水,直到不再产生白色沉淀 和白色沉淀 和白色沉淀 为止,再向两支试管中分别加入 为止,再向两支试管中分别加入 溶液,边加边振荡,观察现象。 溶液,边加边振荡,观察现象。 | 操作:向盛有 溶液的试管中加入 溶液的试管中加入 新制氯水,振荡 新制氯水,振荡 |
| 现象: | 现象:溶液由无色变为棕黄色 化学方程式: |
结论:金属性 强于 强于 | 结论:非金属性Cl强于I |
您最近一年使用:0次
解题方法
7 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
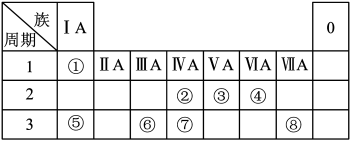
(1)地壳中含量居于第二位的元素在周期表中的位置是___________ 。
(2)②的最高价氧化物的分子式为___________ ;⑦的最高价氧化物对应水化物的分子式为___________ 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:___________ 、___________ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
(5)半径大小比较:③___________ ④;金属性强弱比较:⑤___________ ⑥(填“>”、“<”或“=”)。
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为___________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②的最高价氧化物的分子式为
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
| A.最高正化合价为+6 | B.气态氢化物比 稳定 稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
(5)半径大小比较:③
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
名校
解题方法
8 . X、Y、Z、M、W为原子序数依次增大的五种短周期元素,元素的性质或原子结构的相关叙述如表所示,回答下列问题。
(1)分别依次写出X、W的元素名称___________ 、___________ 。
(2)Y、Z、M的简单离子半径依次增大的顺序为___________ (填微粒符号)。
(3)X的简单气态氢化物与W的最高价氧化物对应的水化物反应的化学方程式为___________ 。
(4)X和Y简单气态氢化物的热稳定性较强的是___________ (填化学式)。
(5)Z的最高价氧化物对应的水化物的电子式为___________ ,该物质所含化学键类型为___________ ,该物质与M的单质反应的离子方程式为___________ 。
| 元素编号 | 元素性质或原子结构的相关叙述 |
| X | 元素原子L层是K层电子数的2.5倍 |
| Y | 元素原子最外层电子数比其次外层电子数多4 |
| Z | 元素原子最外层有1个电子,其阳离子与Y的阴离子核外电子总数相同 |
| M | 地壳中含量最多的金属元素 |
| W | 最高正化合价与最低负化合价代数和为6 |
(2)Y、Z、M的简单离子半径依次增大的顺序为
(3)X的简单气态氢化物与W的最高价氧化物对应的水化物反应的化学方程式为
(4)X和Y简单气态氢化物的热稳定性较强的是
(5)Z的最高价氧化物对应的水化物的电子式为
您最近一年使用:0次
9 . 使用含氟牙膏生成的难溶化合物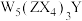 能有效预防龋齿。X、Y、Z、W为原子序数依次增大的前20号主族元素,X为地壳中含量最多的元素,Y与X同周期,Z的最外层电子数为内层电子总数的一半,W为金属元素。下列说法正确的是
能有效预防龋齿。X、Y、Z、W为原子序数依次增大的前20号主族元素,X为地壳中含量最多的元素,Y与X同周期,Z的最外层电子数为内层电子总数的一半,W为金属元素。下列说法正确的是
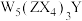 能有效预防龋齿。X、Y、Z、W为原子序数依次增大的前20号主族元素,X为地壳中含量最多的元素,Y与X同周期,Z的最外层电子数为内层电子总数的一半,W为金属元素。下列说法正确的是
能有效预防龋齿。X、Y、Z、W为原子序数依次增大的前20号主族元素,X为地壳中含量最多的元素,Y与X同周期,Z的最外层电子数为内层电子总数的一半,W为金属元素。下列说法正确的是| A.原子半径:X<Y<Z<W |
| B.简单氢化物的稳定性:Y<X |
C. 中含有离子键和非极性共价键 中含有离子键和非极性共价键 |
| D.Z的最高价氧化物对应的水化物为强酸 |
您最近一年使用:0次
10 . 某长石矿物的化学式为 ,
,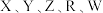 是原子序数依次增大的前20号主族元素。元素Z、W是常见的金属元素,元素R在地壳中的含量仅次于元素Y。下列说法错误的是
是原子序数依次增大的前20号主族元素。元素Z、W是常见的金属元素,元素R在地壳中的含量仅次于元素Y。下列说法错误的是
 ,
,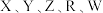 是原子序数依次增大的前20号主族元素。元素Z、W是常见的金属元素,元素R在地壳中的含量仅次于元素Y。下列说法错误的是
是原子序数依次增大的前20号主族元素。元素Z、W是常见的金属元素,元素R在地壳中的含量仅次于元素Y。下列说法错误的是| A.X、Y形成的二元化合物常温常压下呈液态 |
B.Z、W最高价氧化物对应水化物的碱性; |
| C.X、Y、Z、R四种元素形成的单质中,R熔点最高 |
| D.Z、R、W最高价氧化物对应的水化物之间均可发生反应 |
您最近一年使用:0次



