解题方法
1 . 下表是元素周期表的一部分,针对编号①~⑫元素,回答下列有关问题:
(1)在这些元素中,非金属性最强的元素是_______ (填元素符号,下同),最不活泼的元素是_______ 。
(2)写出元素①对应气态氢化物的化学式和电子式:_______ 、_______ 。
(3)在元素③和④中,单质与水反应较剧烈的是_______ (填元素符号),它与水反应的化学方程式是_______ 。
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是_______ (填化学式)。
(5)能证明⑧和⑫单质氧化性强弱的实验事实 用离子方程式表示)是
用离子方程式表示)是_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |  |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)写出元素①对应气态氢化物的化学式和电子式:
(3)在元素③和④中,单质与水反应较剧烈的是
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是
(5)能证明⑧和⑫单质氧化性强弱的实验事实
 用离子方程式表示)是
用离子方程式表示)是
您最近一年使用:0次
2 . 下表是元素周期表中主族的一部分,其中c是地壳中含量最多的元素,回答下列问题:__________ , 的结构式为
的结构式为___________ 。
(2)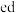 为
为__________ (填“离子”或“共价”)化合物,能证明该结论的实验依据为___________ .
(3)用电子式表示物质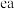 的形成过程
的形成过程__________________ ,该物质能与 反应生成
反应生成 ,反应中
,反应中 作
作________ 剂。
(4) 最高价氧化物水化物的碱性由强到弱的顺序为
最高价氧化物水化物的碱性由强到弱的顺序为_________ (用化学式表示)。
(5)若 均为上述元素形成的10电子微粒,相互之间能发生离子反应:
均为上述元素形成的10电子微粒,相互之间能发生离子反应: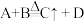 ,写出该反应的离子方程式
,写出该反应的离子方程式____________________ 。
(6)下列有关说法正确的是__________ 。
A.a和e最外层电子数相同,均为碱金属元素 B.考古时利用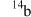 测定一些文物的年代
测定一些文物的年代
C.科学家常在 等元素区域寻找新型农药
等元素区域寻找新型农药
D.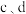 形成阴离子时,c原子得到的电子更多,所以非金属性
形成阴离子时,c原子得到的电子更多,所以非金属性
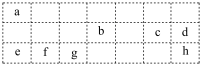
 的结构式为
的结构式为(2)
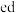 为
为(3)用电子式表示物质
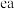 的形成过程
的形成过程 反应生成
反应生成 ,反应中
,反应中 作
作(4)
 最高价氧化物水化物的碱性由强到弱的顺序为
最高价氧化物水化物的碱性由强到弱的顺序为(5)若
 均为上述元素形成的10电子微粒,相互之间能发生离子反应:
均为上述元素形成的10电子微粒,相互之间能发生离子反应: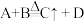 ,写出该反应的离子方程式
,写出该反应的离子方程式(6)下列有关说法正确的是
A.a和e最外层电子数相同,均为碱金属元素 B.考古时利用
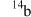 测定一些文物的年代
测定一些文物的年代C.科学家常在
 等元素区域寻找新型农药
等元素区域寻找新型农药D.
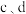 形成阴离子时,c原子得到的电子更多,所以非金属性
形成阴离子时,c原子得到的电子更多,所以非金属性
您最近一年使用:0次
解题方法
3 . 下表为元素周期表中的一部分.
用化学式或元素符号回答下列问题:
(1)①③⑤中,最高价氧化物对应水化物中碱性最强的是____________ .
(2)②③④中形成的简单离子半径由大到小的顺序是____________ .
(3)⑨的最高价氧化物对应水化物的化学式为____________ .①和⑨两元素形成化合物的化学式为____________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为____________ .
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是____________ ,三者非金属性的强弱顺序为____________ .
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(1)①③⑤中,最高价氧化物对应水化物中碱性最强的是
(2)②③④中形成的简单离子半径由大到小的顺序是
(3)⑨的最高价氧化物对应水化物的化学式为
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
名校
解题方法
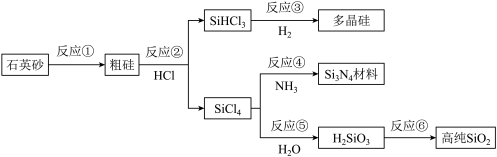
4 . 如图,通过工业联产可有效解决多晶硅(Si)生产中副产物SiCl4._______ 。
(2)反应①工业生产采用焦炭高温还原法制备,其化学方程式为_______ 。
(3)流程中涉及的化学反应属于氧化还原反应的有_______ (填反应序号)。
(4)高温下,反应④的化学方程式为_______ 。
(5)在多晶硅、Si3N4材料和高纯SiO2中,可用于制造光导纤维的是_______ 。
(6)实验室不能使用玻璃塞的细口瓶装氢氧化钠,原因是_______ (用化学方程式表示)。
(7)Si和Ge属于同主族元素,下列预测合理的是_______ (填选项序号)。
a.Ge与H2化合难于Si
b.GeO2既有氧化性又有还原性
c.酸性H2GeO3>H2SiO3
d.Si和Ge都可做半导体材料
(2)反应①工业生产采用焦炭高温还原法制备,其化学方程式为
(3)流程中涉及的化学反应属于氧化还原反应的有
(4)高温下,反应④的化学方程式为
(5)在多晶硅、Si3N4材料和高纯SiO2中,可用于制造光导纤维的是
(6)实验室不能使用玻璃塞的细口瓶装氢氧化钠,原因是
(7)Si和Ge属于同主族元素,下列预测合理的是
a.Ge与H2化合难于Si
b.GeO2既有氧化性又有还原性
c.酸性H2GeO3>H2SiO3
d.Si和Ge都可做半导体材料
您最近一年使用:0次
名校
解题方法
5 . W、X、Y、Z、M、G、H七种短周期元素,原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y、G同主族,可形成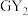 、
、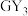 两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
(1)Y在元素周期表中的位置为_______ 。
(2)X的气态氢化物的电子式为_____ ,工业合成X的气态氢化物的化学方程式为______ 。
(3)Y、Z、G三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(4)Z、M最高价氧化物对应的水化物相互反应的离子方程式为_______ ,G的最高价氧化物对应的水化物的浓溶液与金属铜反应的化学方程式为_______ 。
(5)G的非金属性_______ (填“>”或“<”)H的非金属性,下列表述可以作为验证的证据的是_______ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、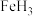
D.比较这两种元素单质与酸或碱反应的难易程度
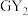 、
、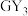 两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:(1)Y在元素周期表中的位置为
(2)X的气态氢化物的电子式为
(3)Y、Z、G三种元素原子半径由大到小的顺序是
(4)Z、M最高价氧化物对应的水化物相互反应的离子方程式为
(5)G的非金属性
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、
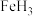
D.比较这两种元素单质与酸或碱反应的难易程度
您最近一年使用:0次
名校
解题方法
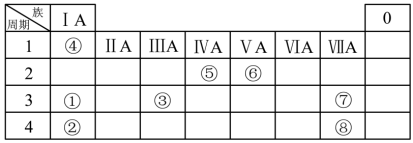
6 . 几种主族元素在周期表中的位置如下
(1)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素在周期表中的位置是_______ 。
(2)①②③三种元素最高价氧化物对应水化物碱性最强的是_______ (填化学式)。
(3)①③⑦三种元素所形成的简单离子的半径由大到小的顺序是_______ (用元素的离子符号表示)。
(4)⑥元素最高价氧化物的水化物的浓溶液不稳定,受热或见光易分解,写出该反应的化学方程式_______ 。⑥的气态氢化物与⑦的气态氢化物水溶液反应生成X,写出X的电子式_______ ,X中含有的化学键类型有_______ 。
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是_______ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦的氧化物对应的水化物的酸性强于⑧的氧化物对应的水化物的酸性
c.⑦的单质能将⑧的单质从其钠盐溶液中置换出来
(1)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素在周期表中的位置是
(2)①②③三种元素最高价氧化物对应水化物碱性最强的是
(3)①③⑦三种元素所形成的简单离子的半径由大到小的顺序是
(4)⑥元素最高价氧化物的水化物的浓溶液不稳定,受热或见光易分解,写出该反应的化学方程式
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是
a.⑦的氢化物比⑧的氢化物稳定
b.⑦的氧化物对应的水化物的酸性强于⑧的氧化物对应的水化物的酸性
c.⑦的单质能将⑧的单质从其钠盐溶液中置换出来
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题:
(1)②元素原子的电子式是:_______ 。
(2)硅元素在周期表中的位置是:第_______ 周期_______ 族。
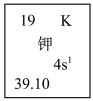
(3)如图所示钾元素的部分信息,“30.97”数值表示_______ 。______ (填元素符号)。③和⑧两种元素形成的气态氢化物稳定性强的是_______ (填化学式)。写出④的最高价氧化物对应水合物和⑧的最高价氧化物对应水合物相互反应的化学方程式_______ 。
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因_______ 。能证明这一事实的化学反应为_______ (写一个化学方程式)。
(6)能证明O元素的非金属性强于S元素的依据是_______ 。
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是_______ 。
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是_______ 。
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是_______ 。
族 周期 | ⅠA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)②元素原子的电子式是:
(2)硅元素在周期表中的位置是:第
(3)如图所示钾元素的部分信息,“30.97”数值表示
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因
(6)能证明O元素的非金属性强于S元素的依据是
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是
| A.质子数相同 | B.质量相同 |
| C.化学性质相同 | D.位置相同(周期表中) |
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是
| A.在周期表中金属与非金属的分界处可以找到催化剂材料 |
| B.对氟、氯、硫、磷、砷等元素的研究,有助于制造出新品种的农药 |
| C.在过渡元素中可寻找制造半导体的元素 |
| D.可在第IA、IIA族元素中寻找制造耐高温、耐腐蚀合金的元素 |
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是
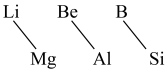
| A.Li在空气中燃烧生成Li2O、Li3N | B.硼酸是弱酸 |
| C.Be不与水反应 | D.Be(OH)2是两性氢氧化物 |
您最近一年使用:0次
8 . X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,X最外层电子数是内层电子数的2倍,Y的单质与氢气在暗处能剧烈化合并发生爆炸,Z短周期元素中原子半径最大,W其氧化物是两性氧化物,Q同周期元素中,最高价氧化物对应水化物的酸性最强。
(1)元素Y在元素周期表中的位置是___________ 。
(2)Z在氧气中完全燃烧的产物的化学式为___________ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。___________ 、___________ ;M为___________ (填化学式),其作用是___________ 。
②能说明X元素的非金属性比硅元素强的实验现象是___________ 。
(5)元素Z与W相比,金属性较弱的是___________ (填元素名称),请写出能证明这一结论的实验事实___________ 。(列举一条)
(1)元素Y在元素周期表中的位置是
(2)Z在氧气中完全燃烧的产物的化学式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。

②能说明X元素的非金属性比硅元素强的实验现象是
(5)元素Z与W相比,金属性较弱的是
您最近一年使用:0次
名校
9 . 如图为元素周期表的一部分,参照元素①~⑩在表中的位置,回答下列问题:
(1)写出元素锗(Ge,原子序数32)在元素周期表中的位置______ 。
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为______ 。
(3)③⑦⑧最高价氧化物对应水化物酸性由强到弱的顺序为(填化学式)______ 。
(4)写出②的单质在足量④的单质中燃烧产物的电子式______ 。用电子式表示⑤和⑩组成简单化合物的形成过程______ 。
(5)④和⑨的单质均能与 反应生成
反应生成 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性
型化合物的热稳定性______ (填化学式)。
(6)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:

i.M中所含的化学键种类为______ (填字母)。
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.生成Z和M的离子方程式______ 。
ⅲ.Z→N的化学方程式______ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(1)写出元素锗(Ge,原子序数32)在元素周期表中的位置
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为
(3)③⑦⑧最高价氧化物对应水化物酸性由强到弱的顺序为(填化学式)
(4)写出②的单质在足量④的单质中燃烧产物的电子式
(5)④和⑨的单质均能与
 反应生成
反应生成 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性
型化合物的热稳定性(6)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:

i.M中所含的化学键种类为
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.生成Z和M的离子方程式
ⅲ.Z→N的化学方程式
您最近一年使用:0次
解题方法
10 . 下表是元素周期表的部分,根据表中的 种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:_____________ (填元素符号)。
(2)在这些元素中,最高价氧化物对应的水化物酸性最强的物质是_____________ (填化学式,下同),碱性最强的物质是_____________ 。
(3)比较①与⑥的最高价氧化物对应的水化物,_____________ 的酸性强(填化学式)。
(4)在①~ ⑨元素中,最高价氧化物的水化物呈两性的物质是_________________ (写化学式),写出它与⑨的最高价氧化物对应的水化物反应的离子方程式_________________________ 。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:
(2)在这些元素中,最高价氧化物对应的水化物酸性最强的物质是
(3)比较①与⑥的最高价氧化物对应的水化物,
(4)在①~ ⑨元素中,最高价氧化物的水化物呈两性的物质是
您最近一年使用:0次



