名校
解题方法
1 . 元素 R、X、T、Z、Q 在元素周期表中的相对位置如图所示,其中 R 的氢化物的水溶液可以用来刻蚀玻璃,则下列判断正确的是
| R | ||
| X | T | Z |
| Q |
| A.气态氢化物的酸性:R>T>Q |
| B.气态氢化物的还原性:X>T |
| C.R 与 Q 的电子数相差 16 |
| D.R 的单质通入 T 的钠盐溶液中能置换出T 的单质 |
您最近一年使用:0次
2020-05-08更新
|
153次组卷
|
3卷引用:江西省南昌市第二中学2019-2020学年高一下学期第一次月考化学试题
名校
2 . 短周期主族元素W、X、Y、Z的原子序数依次增大,它们的原子最外层电子数总和等于Z原子序数,由这四种元素组成一种化合物M具有如下性质下列推断正确的是( )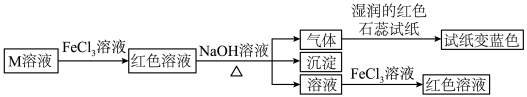

| A.原子半径Z>Y>X>W |
| B.最高价氧化物对应的水化物酸性:Y>X |
| C.简单阴离子的还原性:W<Z |
| D.W、Y、Z组成的化合物只含有共价键 |
您最近一年使用:0次
2020-04-16更新
|
207次组卷
|
9卷引用:【南昌新东方】2019 南昌外国语 高一下 第一次月考
(已下线)【南昌新东方】2019 南昌外国语 高一下 第一次月考 【全国百强校】山东省淄博实验中学2019届高三下学期寒假学习效果检测(开学考试)理科综合化学试题【全国百强校】湖北省沙市中学2019届高三理科能力测试(十三)化学试题四川省阆中中学2020届高三上学期期中考试理综化学试题吉林省梅河口市第五中学2021届高三上学期第二次月考化学试题(已下线)第五章 物质结构与性质元素周期律 第28练 元素推断与无机物的性质河南省南阳市第一中学校2023-2024学年高三上学期第三次月考化学试题新疆石河子第一中学2023-2024学年高三上学期第二次月考化学试题河南省南阳市第一中学校2023-2024学年高三上学期第三次月考化学试题
名校
3 . 元素周期表中的四种元素的有关信息如下,请用合理的化学用语 填写空白。
(1)X元素周期表中的位置为_____ ,X、Y、W三种元素的简单离子半径从大到小的顺序为_______ 。
(2)足量W的最高价氧化物的水化物的稀溶液与1mol甲完全反应,放出热量QkJ,请写出表示该过程中和热的热化学方程式_____ 。
(3)下列有关W的气态氢化物丁的说法正确的有_______ (选填字母)
a、丁比氯化氢沸点高 b、丁比氯化氢稳定性好
c、丁比氟化氢还原性弱 d、丁比氟化氢酸性弱
(4)请写出丙溶于丁的水溶液的离子方程式____________ 。
| 在周期表中的区域 | 元素代号 | 有关信息 |
| 短周期元素 | X | X的最高价氧化物的水化物甲是一种胃酸中和剂,且能溶于强碱溶液 |
| Y | Y的一种氢化物可用于制造纯碱和做制冷剂 | |
| 长周期元素 | Z | Z的一种盐乙可以做净水剂, 的某种氧化物丙可以做红色涂料 的某种氧化物丙可以做红色涂料 |
| W | W元素大量存在于海藻中,它的银盐可用于人工降雨 |
(1)X元素周期表中的位置为
(2)足量W的最高价氧化物的水化物的稀溶液与1mol甲完全反应,放出热量QkJ,请写出表示该过程中和热的热化学方程式
(3)下列有关W的气态氢化物丁的说法正确的有
a、丁比氯化氢沸点高 b、丁比氯化氢稳定性好
c、丁比氟化氢还原性弱 d、丁比氟化氢酸性弱
(4)请写出丙溶于丁的水溶液的离子方程式
您最近一年使用:0次
19-20高三·江西南昌·期中
4 . 由位于元素周期表前三周期的W、X、Y、Z四种元素“组合”成的一种超分子结构如图。Z、X、Y的族序数依次增大,X、Y位于同一周期,Z与W同主族。下列说法正确的是( )


| A.Y的单质的氧化性在同主族中最弱 |
| B.简单离子半径:Y>Z |
| C.W与Y可组成多种离子化合物 |
| D.氢化物的热稳定性:X>Y |
您最近一年使用:0次
解题方法
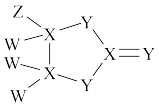
5 . 有一种化合物结构如图所示,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,X、Y是同周期元素,Z的含氧酸均具有氧化性,该化合物相对分子质量小于125。下列有关说法正确的是

| A.WZ沸点高于W2Y的沸点 |
| B.X的含氧酸一定为二元弱酸 |
| C.原子半径大小:Z>Y>X>W |
| D.X与Z组成的化合物中可能含有非极性键 |
您最近一年使用:0次
16-17高三上·江西南昌·期末
解题方法
6 . W,X,Y,Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻,Y与Z相邻。已知W元素的氢化物与Z元素的氢化物反应只生成一种盐a;X,Y位于同一族,它们能组成YX2,YX3两种常见化合物。请回答下列问题:
(1)X元素位于周期表的位置为_______________ 。
(2)X,Y,Z三种元素形成的单质中,氧化性最弱的是________ (填化学式)。
(3)a溶液的pH____ 7(填“>”、“<”或“=”),用离子方程式解释为:___________ 。
(4)Y与Z可形成共价化合物Y2Z2,分子中Y与Z均满足8电子稳定结构,则Y2Z2的电子式为______ 。Y2Z2遇水很易反应,产生的气体能使品红溶液褪色,则其与水反应的化学方程式为_________ 。
(5)工业上用氧化WH3法制取WO,该反应的热化学方程式为:4WH3(g)+5O2(g)=4WO(g)+6H2O(g)∆H=-905.8kJ/mol;已知W2(g)+O2(g)=2WO(g)∆H=+180kJ/mol,则WH3与氧气反应产生两种无污染物质的热化学方程式为__________________ 。
(1)X元素位于周期表的位置为
(2)X,Y,Z三种元素形成的单质中,氧化性最弱的是
(3)a溶液的pH
(4)Y与Z可形成共价化合物Y2Z2,分子中Y与Z均满足8电子稳定结构,则Y2Z2的电子式为
(5)工业上用氧化WH3法制取WO,该反应的热化学方程式为:4WH3(g)+5O2(g)=4WO(g)+6H2O(g)∆H=-905.8kJ/mol;已知W2(g)+O2(g)=2WO(g)∆H=+180kJ/mol,则WH3与氧气反应产生两种无污染物质的热化学方程式为
您最近一年使用:0次
名校
解题方法
7 . 短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数,且X、Y、W原子最外层电子数之和恰好等于Z元素的核电荷数,X与W的最高化合价之和为8。常见元素Z的单质是目前使用量最大的主族金属元素单质,下列说法中不正确的是
| A.因为Z的氧化物熔点很高,不适宜于电解,故工业上常用电解Z与W的化合物的方法制取单质Z |
| B.沸点:YX3>XW |
| C.化合物YW3遇水能强烈水解,产物之一具有强氧化性 |
| D.离子化合物YX5假如存在。该物质与水反应必然生成气体X2,同时得到一种弱碱溶液 |
您最近一年使用:0次
2020-02-24更新
|
102次组卷
|
2卷引用:江西临川二中2019届高三第二次模拟考试化学试卷
名校
解题方法
8 . 有A、B、C、D、E、F、G7种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是____ ,B位于周期表中第____ 周期____ 族,C的原子结构示意图是________________ 。
(2)E的单质颜色是_______ 。
(3)A元素与D元素形成的化合物的电子式是_________ 。
(4)G的单质与水反应的化学方程式是________ 。
(5)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是_____ (填化学式,下同),酸性最强的是_______ ,气态氢化物最稳定的是__________ 。
(6)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是_______________ 。
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是
(2)E的单质颜色是
(3)A元素与D元素形成的化合物的电子式是
(4)G的单质与水反应的化学方程式是
(5)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是
(6)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
您最近一年使用:0次
名校
9 . X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价。回答下列问题:
(1)元素X原子结构示意图为________ 。
(2)元素Y的最高价氧化物的分子式为__________ ,其中一种同位素可测定文物年代,这种同位素的符号是________ 。
(3)元素Z能与氢元素形成18电子分子,分子式为_________ 。
(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为___________ 。
(5)ZW3常温下呈液态,可与水反应生成一种具有漂白性的酸和一种碱性气体,反应的化学方程式为_______ 。
(6)探寻物质的性质差异性是学习的重要方法之一。X、Y、Z、W四种元素的最高价氧化物的水化物中酸性明显不同于其他三种酸的是_______ (用酸的分子式表示)。
(1)元素X原子结构示意图为
(2)元素Y的最高价氧化物的分子式为
(3)元素Z能与氢元素形成18电子分子,分子式为
(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为
(5)ZW3常温下呈液态,可与水反应生成一种具有漂白性的酸和一种碱性气体,反应的化学方程式为
(6)探寻物质的性质差异性是学习的重要方法之一。X、Y、Z、W四种元素的最高价氧化物的水化物中酸性明显不同于其他三种酸的是
您最近一年使用:0次
名校
解题方法
10 . A、B、C、D、E、F是短周期主族元素,且原子序数依次增大。在短周期中A元素原子半径最小,D元素原子半径最大,B的简单氢化物的水溶液呈碱性,C、E同主族,形成的化合物为EC2、EC3。回答下列问题:
(1)E在元素周期表中的位置为_____________________________ 。
(2)比较B与C简单氢化物的热稳定性:_____ > 。(填化学式)
(3)D,C两元素组成的化合物D2C2的电子式为_____________________ ,D2C2与水反应的化学方程式为 ______________________________________________ 。
(4)下列事实能说明元素F的非金属性比元素E的非金属性强的是______ 。
A.元素F形成的单质比元素E形成的单质的熔点低
B.F和E两元素的简单氢化物受热分解,前者的分解温度高
C.F2通入到D2E的溶液中出现浑浊
D.F氢化物的酸性比E氢化物的酸性强
(1)E在元素周期表中的位置为
(2)比较B与C简单氢化物的热稳定性:
(3)D,C两元素组成的化合物D2C2的电子式为
(4)下列事实能说明元素F的非金属性比元素E的非金属性强的是
A.元素F形成的单质比元素E形成的单质的熔点低
B.F和E两元素的简单氢化物受热分解,前者的分解温度高
C.F2通入到D2E的溶液中出现浑浊
D.F氢化物的酸性比E氢化物的酸性强
您最近一年使用:0次
2018-10-29更新
|
367次组卷
|
3卷引用:江西省南昌市八一中学2019-2020学年高一下学期期末考试化学试题



