解题方法
1 . 元素周期表与元素周期律在学习、研究中有很重要的作用。下表所示为某5种元素的相关信息,已知W、X都位于第三周期。
请回答:
(1)W在元素周期表中的位置为_______ ,Q、W、X形成的简单离子半径的由大到小顺序是_______ (用离子符号表示)。
(2)用电子式表示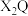 的形成过程:
的形成过程:_______ 。
(3)写出Y的单质与Q最简单氢化物反应的化学方程式_______ 。根据元素周期律可知金属性:Y>X,用原子结构解释原因:_______ 。
(4)下列对于Z及其化合物的推断中正确的是_______(填字母)。
(5)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入硫酸亚铁溶液中,主要的反应现象是_______ 。
(6)原子序数为Q的2倍的元素,与Q组成的气体化合物具有漂白性,请设计简单实验方案验证其漂白性_______ 。
| 元素 | 相关信息 |
| Q | 最外层电子数是次外层电子数的3倍 |
| W | 最高化合价为 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)的火焰呈紫色 |
| Z | 与W同主族且其单质在 溶液中呈橙色 溶液中呈橙色 |
(1)W在元素周期表中的位置为
(2)用电子式表示
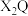 的形成过程:
的形成过程:(3)写出Y的单质与Q最简单氢化物反应的化学方程式
(4)下列对于Z及其化合物的推断中正确的是_______(填字母)。
A.Z的化合价中有 和 和 |
| B.Z的最高价氧化物对应水化物的酸性强于W的最高价氧化物对应水化物的酸性 |
| C.Z简单气态氢化物的稳定性弱于W简单气态氢化物的稳定性 |
| D.Z单质可以从含有W的盐溶液中置换出W |
(6)原子序数为Q的2倍的元素,与Q组成的气体化合物具有漂白性,请设计简单实验方案验证其漂白性
您最近一年使用:0次
名校
2 . 原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成 、
、 和HW三种共价化合物:Y与氧元素可组成
和HW三种共价化合物:Y与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。
(1)写出 的电子式:
的电子式:_______ ,其中含有的化学键是_______ 。
(2)用电子式表示 的形成过程
的形成过程_______ 。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是_______ (填化学式)。
(4) 、
、 和HW三种化合物,其中一种与另外两种都能反应的是
和HW三种化合物,其中一种与另外两种都能反应的是_______ (填化学式)
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式_______ 。
 、
、 和HW三种共价化合物:Y与氧元素可组成
和HW三种共价化合物:Y与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。(1)写出
 的电子式:
的电子式:(2)用电子式表示
 的形成过程
的形成过程(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
(4)
 、
、 和HW三种化合物,其中一种与另外两种都能反应的是
和HW三种化合物,其中一种与另外两种都能反应的是(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
您最近一年使用:0次
名校
解题方法
3 . 短周期元素W、X、Y、Z的原子序数依次增加,由这些元素组成的常见物质的转化关系如下图,其中a、b、d、g为化合物,a为淡黄色固体,c是Z的单质,在铝热反应中常做引发剂;f可作电极材料下列有关说法正确的是
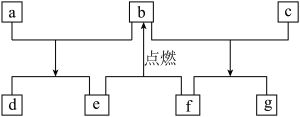

| A.简单氢化物的沸点:Y>X |
| B.简单离子的半径:Y>Z>X |
| C.阳离子的氧化性:Y>Z |
| D.b和g所含的化学键类型相同 |
您最近一年使用:0次
名校
4 . 下表为对部分短周期元素的性质或原子结构的描述。
下列有关说法中正确的是
| 元素编号 | 元素性质或原子结构 |
| T | M层上的电子数是原子核外电子层数的2倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| A.元素的非金属性:Z>T |
| B.最高价氧化物对应水化物的酸性:X>T |
| C.气态氢化物的热稳定性:X>Y |
| D.Z、T两种元素的原子半径:Z>T |
您最近一年使用:0次
2021-06-21更新
|
776次组卷
|
8卷引用:陕西省安康市白河高中2021-2022学年高二上学期期末考试化学试题
解题方法
5 . 下列是元素周期表的一部分:
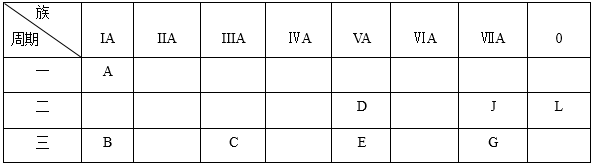
根据以上元素在周期表中的位置,用化学式 填写空白。
(1)非金属性最强的元素是_________ ;化学性质最不活泼的是_________ ;除L外,原子半径最大的是_________ ;A与D形成的10电子离子是_________ 。
(2)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、D、E四种元素的最高价氧化物对应水化物的化学式 排列成序是__________________ ;
(3)B元素可以形成两种氧化物,分别写出两种氧化物的电子式_________ ,_________ 。
(4)B、C、G、J四种元素的简单离子的半径由大到小的顺序为_________ 。

根据以上元素在周期表中的位置,用
(1)非金属性最强的元素是
(2)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、D、E四种元素的最高价氧化物对应水化物的
(3)B元素可以形成两种氧化物,分别写出两种氧化物的电子式
(4)B、C、G、J四种元素的简单离子的半径由大到小的顺序为
您最近一年使用:0次
6 . A、B、X、D、E、Y为短周期元素,原子序数依次增大,有关信息如表中所示:
(1)六种元素中原子半径最大的是_______ ( 填元素符号)。
(2)A在周期表中的位置是_______ 。
(3)A和B的最简单氢化物中较稳定的是_______ (填化学式)。
(4)B、X以原子个数比为1:1组成的化合物W,常用于呼吸面具中做供氧剂。写出W的电子式_______ ,其所含化学键的类型为_______ 。
(5)D的氧化物与X的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(6)Y的最高价氧化物对应的水化物的化学式为_______ 。
(7)下列说法中能证明Y的非金属性强于E的是_______( 填字母)。
| A | 一种同位素常用于文物年代的测定 |
| B | 最外层电子数是电子层数的3倍 |
| X | M层有1个电子,单质需保存在煤油中 |
| D | 地壳中含量最多的金属元素 |
| E | 与B可形成EB2和EB3两种物质,EB2是形成酸雨的主要物质 |
| Y | 单质可用于生产漂白液、漂白粉 |
(2)A在周期表中的位置是
(3)A和B的最简单氢化物中较稳定的是
(4)B、X以原子个数比为1:1组成的化合物W,常用于呼吸面具中做供氧剂。写出W的电子式
(5)D的氧化物与X的最高价氧化物对应的水化物反应的离子方程式是
(6)Y的最高价氧化物对应的水化物的化学式为
(7)下列说法中能证明Y的非金属性强于E的是_______( 填字母)。
| A.E的单质在常温下为固体而Y的单质为气体 |
| B.与Fe反应时,Y的单质能生成高价铁化合物,E的单质只能生成低价铁化合物 |
| C.简单气态氢化物的稳定性:Y>E |
| D.H2EO3的酸性弱于HYO3 |
您最近一年使用:0次



