名校
解题方法
1 . X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)元素X的元素符号为____ ;元素Y的元素名称为____ 。
(2)元素Q的基态原子的核外电子排布式为____ 。
(3)分子XZ2的空间结构是____ ;分子YZ2中Y原子的杂化方式是____ 。
(4)相同条件下分子XZ2与分子YZ2在水中的溶解度较大的是____ (填分子式),理由是____ 。
(5)用氢键表示式写出E的氢化物溶液中存在的氢键:____ (任写两种)。
(1)元素X的元素符号为
(2)元素Q的基态原子的核外电子排布式为
(3)分子XZ2的空间结构是
(4)相同条件下分子XZ2与分子YZ2在水中的溶解度较大的是
(5)用氢键表示式写出E的氢化物溶液中存在的氢键:
您最近一年使用:0次
解题方法
2 . A、B、D、E、F为短周期元素,非金属元素A的最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物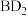 。
。 与
与 具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是_______ ;常温下F的单质和NaOH溶液反应的产物中氧化产物与还原产物的物质的量之比为_______ 。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为_______ ,其与等物质的量的F单质在水中反应的离子方程式为_______
(3)元素A、B、D组成的2种化合物都是厨房中的常见物质,写出这2种化合物反应的化学方程式_______ 。
(4)由这些元素组成的物质;其组成和结构信息如下表:
a的电子式为_______ ;b与水反应的化学方程式为_______ 。
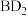 。
。 与
与 具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:(1)A在周期表中的位置是
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为
(3)元素A、B、D组成的2种化合物都是厨房中的常见物质,写出这2种化合物反应的化学方程式
(4)由这些元素组成的物质;其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 由A和E形成的二元离子化合物 |
| b | 化学式为 |
您最近一年使用:0次
3 . X、Y、Z、W、R五种元素的性质或结构信息如表,根据表中的信息回答下列问题:
(1)写出元素R在元素周期表中的位置:_______ 。
(2)由X、Z、R三种元素形成的化合物XRZ的结构式为_______ ;化合物WR的电子式为_______ 。
(3)Y、Z的最简单氢化物中较稳定的是_______ (填化学式),判断依据是_______ 。由Y和Z组成且Y和Z的质量之比为7:4的化合物的分子式是_______ 。
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:_______ ,燃烧片刻后取出燃烧管,迅速将集气瓶倒扣在过量的烧碱溶液中,可能产生的现象是_______ ,所得溶液中存在的溶质除了过量的NaOH外,还含有的是_______ (填化学式)。
| 元素 | X | Y | Z | W | R |
| 性质或结构信息 | 是原子半径最小的元素 | 常见单质为空气中的主要成分之一 | 是海水中质量分数最大的元素 | 原子核内有11个质子 | 原子核外有3个电子层,常见单质为气体 |
(2)由X、Z、R三种元素形成的化合物XRZ的结构式为
(3)Y、Z的最简单氢化物中较稳定的是
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:
您最近一年使用:0次
2022-01-19更新
|
259次组卷
|
7卷引用:湖南省衡阳市祁东县2021-2022学年高一上学期期末考试化学试题
名校
4 . W、X、Y、Z是原子序数依次增大的短周期主族元素,且原子序数总和为25,Y是地壳中含量最多的元素,由这四种元素形成的某化合物结构如图所示。下列叙述不正确的是
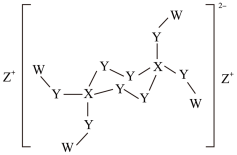

| A.简单离子半径:Y>Z |
| B.该化合物具有强氧化性,可杀菌消毒 |
C.X的最高价氧化物的水化物分子式为 |
| D.该化合物中既含有离子键,又含有极性共价键和非极性共价键 |
您最近一年使用:0次
名校
解题方法
5 . 短周期主族元素A、B、C、D、E、F和G原子序数依次递增,其中A是原子半径最小的元素, 的空间结构呈正四面体形,D是地壳中含量最多的元素,E、F和G同周期,E是该周期中原子半径最大的元素,F的单质是黄色晶体。下列说法错误的是
的空间结构呈正四面体形,D是地壳中含量最多的元素,E、F和G同周期,E是该周期中原子半径最大的元素,F的单质是黄色晶体。下列说法错误的是
 的空间结构呈正四面体形,D是地壳中含量最多的元素,E、F和G同周期,E是该周期中原子半径最大的元素,F的单质是黄色晶体。下列说法错误的是
的空间结构呈正四面体形,D是地壳中含量最多的元素,E、F和G同周期,E是该周期中原子半径最大的元素,F的单质是黄色晶体。下列说法错误的是A.原子半径: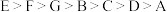 |
B.氧化物对应的水化物酸性: |
| C.D与E、E与G均可形成离子化合物 |
| D.C的气态氢化物和最高价含氧酸可以反应生成盐 |
您最近一年使用:0次
2023-03-11更新
|
334次组卷
|
3卷引用:湖南省长沙市名校联考联合体2022-2023学年高一下学期第一次月考化学试题
名校
解题方法
6 . A、B、C、D、E、F为原子序数依次增大的六种短周期主族元素。已知:A是宇宙中含量最高的元素;B、C形成的化合物是形成酸雨的主要物质;D、E、F为同周期元素,它们的最高价氧化物的水化物均可两两反应。用元素符号回答下列问题:
(1)元素C原子核内质子数比中子数少2个,满足该条件的原子符号为_______ ;元素E在周期中的位置:_______ 。
(2)若元素F的单质是一种黄绿色气体,常温时由F形成的最高价氧化物甲是一种液态物质,将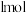 甲完全溶于水形成溶液时放出
甲完全溶于水形成溶液时放出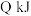 的热量,写出该过程的热化学反应方程式
的热量,写出该过程的热化学反应方程式_______ ;若元素F的单质是一种黄色固体,下列表述中能证明元素C的非金属性强于F的是_______ (填写序号)。
①元素C和F形成的化合物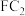 中,F化合价为
中,F化合价为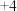 ,C化合价为
,C化合价为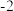
②元素C、F各自形成的最简单氢化物的沸点:前者>后者
③常温时,元素C的单质为气态,F的单质为固态
④元素C的单质可将F从其氢化物溶液中置换出来
(3)元素A、B可形成一种离子化合物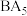 ,该化合物的电子式为
,该化合物的电子式为_______ 。
(4)用高能射线照射A、C形成的10电子分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的化学式_______ ,该阳离子存在的化学键类型有_______ 。
(5)写出元素D、E的最高价氧化物的水化物相互反应的离子方程式_______ 。
(1)元素C原子核内质子数比中子数少2个,满足该条件的原子符号为
(2)若元素F的单质是一种黄绿色气体,常温时由F形成的最高价氧化物甲是一种液态物质,将
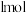 甲完全溶于水形成溶液时放出
甲完全溶于水形成溶液时放出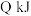 的热量,写出该过程的热化学反应方程式
的热量,写出该过程的热化学反应方程式①元素C和F形成的化合物
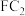 中,F化合价为
中,F化合价为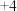 ,C化合价为
,C化合价为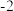
②元素C、F各自形成的最简单氢化物的沸点:前者>后者
③常温时,元素C的单质为气态,F的单质为固态
④元素C的单质可将F从其氢化物溶液中置换出来
(3)元素A、B可形成一种离子化合物
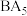 ,该化合物的电子式为
,该化合物的电子式为(4)用高能射线照射A、C形成的10电子分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的化学式
(5)写出元素D、E的最高价氧化物的水化物相互反应的离子方程式
您最近一年使用:0次
2023-05-11更新
|
581次组卷
|
2卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高一下学期4月期中考试化学试题
解题方法
7 . 短周期主族元素 、
、 、
、 、
、 、
、 的原子序数依次增大,且位于三个周期,
的原子序数依次增大,且位于三个周期, 是地壳中含量最多的元素,Z、
是地壳中含量最多的元素,Z、 是金属元素且形成的最高价氧化物对应的水化物可以发生反应,
是金属元素且形成的最高价氧化物对应的水化物可以发生反应, 是同周期中原子半径最小的元素。
是同周期中原子半径最小的元素。
回答下列问题:
(1) 在周期表中的位置是
在周期表中的位置是_________ , 的最简单氢化物的结构式为
的最简单氢化物的结构式为_________ 。
(2) 的最高价氧化物对应水化物的电子式为
的最高价氧化物对应水化物的电子式为_________ ; 、
、 、
、 的简单离子半径由大到小的顺序为
的简单离子半径由大到小的顺序为
___________________________ (用相应离子符号表示)。
(3)举例说明金属性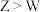 :
:____________________________________ ,写出 的最高价氧化物对应水化物与强碱反应的离子方程式:
的最高价氧化物对应水化物与强碱反应的离子方程式:____________________________________ 。
 、
、 、
、 、
、 、
、 的原子序数依次增大,且位于三个周期,
的原子序数依次增大,且位于三个周期, 是地壳中含量最多的元素,Z、
是地壳中含量最多的元素,Z、 是金属元素且形成的最高价氧化物对应的水化物可以发生反应,
是金属元素且形成的最高价氧化物对应的水化物可以发生反应, 是同周期中原子半径最小的元素。
是同周期中原子半径最小的元素。回答下列问题:
(1)
 在周期表中的位置是
在周期表中的位置是 的最简单氢化物的结构式为
的最简单氢化物的结构式为(2)
 的最高价氧化物对应水化物的电子式为
的最高价氧化物对应水化物的电子式为 、
、 、
、 的简单离子半径由大到小的顺序为
的简单离子半径由大到小的顺序为(3)举例说明金属性
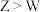 :
: 的最高价氧化物对应水化物与强碱反应的离子方程式:
的最高价氧化物对应水化物与强碱反应的离子方程式:
您最近一年使用:0次
2023-02-18更新
|
151次组卷
|
2卷引用:湖南省衡阳县第四中学2022-2023学年高一下学期第一次(3月)月考化学试题
名校
8 . 中学化学常见部分元素原子结构及性质如下表所示:
(1)A元素在周期表中的位置是_______ 。
(2)F与E可以形成原子个数比分别为2:1、1:1的两种化合物X和Y,其中一种化合物能与A元素的低价阳离子在酸性溶液中发生氧化还原反应,请书写该反应的离子方程式_______ 。
(3)请写出G的单质与氢氧化钠溶液反应的化学方程式_______ 。
(4)下列有关DE2的描述正确的是_______ (填标号)。
①为酸性氧化物 ②可与水反应生成酸
③可用来制作光导纤维 ④60gDE2含有分子的个数为NA
| 元素 | 结构及性质 |
| A | 工业上用量最大的金属,它有两种氯化物,相对分子质量之差为35.5 |
| D | 单质被誉为“信息革命的催化剂”,其元素在地壳中的含量位居第二 |
| E | 通常情况下,E不显正价,A、C、F都能与E形成两种或两种以上化合物 |
| F | F在周期表中可以排在IA族,也有人提出排在ⅦA族 |
| G | 在第三周期中简单离子半径最小 |
(2)F与E可以形成原子个数比分别为2:1、1:1的两种化合物X和Y,其中一种化合物能与A元素的低价阳离子在酸性溶液中发生氧化还原反应,请书写该反应的离子方程式
(3)请写出G的单质与氢氧化钠溶液反应的化学方程式
(4)下列有关DE2的描述正确的是
①为酸性氧化物 ②可与水反应生成酸
③可用来制作光导纤维 ④60gDE2含有分子的个数为NA
您最近一年使用:0次
9 . 已知A、B、C、D、E是原子序数依次增大的短周期主族元素,F是第四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号 完成下列空白:
①元素:A___________ 、D___________ 、F___________
②B、C两种元素第一电离能的大小关系为:___________
(2)元素F的基态价层电子排布式是:___________
(3)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是___________
(4)F元素位于周期表的___________ 区。
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。(1)请用
①元素:A
②B、C两种元素第一电离能的大小关系为:
(2)元素F的基态价层电子排布式是:
(3)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是
电离能( ) ) | I1 | I2 | I3 | I4 | I5 |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近一年使用:0次
解题方法
10 . 短周期主族元素X、Y、Z、W的原子序数依次增大,其中X是地壳中含量最多的元素,X原子的电子数与Y、Z、W原子的最外层电子数之和相等。Y、Z原子的最外层电子数之和与W的最外层电子数相等,且X、Y可形成两种常见的离子化合物,且晶体中的阴阳离子个数比均为1∶2,下列说法不正确的是
| A.工业上通常采用电解法制备Y和Z的单质 |
B.W和X形成的物质 是酸性氧化物,能与水反应生成W的最高价含氧酸 是酸性氧化物,能与水反应生成W的最高价含氧酸 |
| C.与水反应的剧烈程度:Y>Z |
| D.简单离子半径大小:X>Y>Z |
您最近一年使用:0次



