1 . W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外层电子数之和,也是Y的最外层电子数的2倍。W、X的单质常温下均为气体,下列说法正确的是
| A.最简单氢化物的沸点:X>Z |
| B.仅由W和X两种元素不可能形成离子化合物 |
| C.工业上常采用电解熔融的Y的氯化物来获得Y的单质, |
| D.Y元素的单质与X(或Z)元素的最高价氧化物对应水化物的浓溶液不会发生反应 |
您最近一年使用:0次
解题方法
2 . 已知X、Y、Z、W、R、P、Q是短周期主族元素,部分信息如表所示:
请完成下列问题:
(1)Y在周期表中的位置是_______ ,Z与P形成的化合物Z3P中的化学键类型为_______ 。
(2)W的氢化物在同主族元素的氢化物中沸点最高,其原因是_______ 。
(3)Y与R相比,非金属性较强的是_______ (用元素符号表示),下列方法能证明这一结论的是_______ (填字母序号)。
A.常温下Y的单质呈固态,R的单质呈气态
B.R、Y的氢化物稳定性不同
C.Y与R形成的化合物中的化合价
D.R、Y的氧化物的水化物的酸性强弱
(4)工业上制备Y的单质粗品的化学反应方程式为_______ ,锗Ge与Y是同一主族元素,锗Ge不与NaOH溶液反应,但在有H2O2存在时可与NaOH溶液反应生成锗酸盐,其化学方程式为_______ 。
| X | Y | Z | W | R | P | Q | |
| 原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
| 主要化合价 | -4、+4 | -2 | -1、+7 | -3、+5 | +3 | ||
| 其他 | 阳离子 核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(1)Y在周期表中的位置是
(2)W的氢化物在同主族元素的氢化物中沸点最高,其原因是
(3)Y与R相比,非金属性较强的是
A.常温下Y的单质呈固态,R的单质呈气态
B.R、Y的氢化物稳定性不同
C.Y与R形成的化合物中的化合价
D.R、Y的氧化物的水化物的酸性强弱
(4)工业上制备Y的单质粗品的化学反应方程式为
您最近一年使用:0次
2021-04-11更新
|
109次组卷
|
2卷引用:广西贵港市覃塘区覃塘高级中学2020-2021学年高一3月月考化学试题
3 . 如表为元素周期表中的一部分,列出10种元素在周期表中的位置.用化学符号回答下列各题
(1)10种元素中,化学性质最不活泼的是_______ .(符号)
(2)②③④三种元素形成的离子中,离子半径由大到小的顺序是_______ .(离子符号)
(3)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是_______ 。
(4)元素⑦的氢化物的化学式为_______ ;该氢化物常温下和②单质反应的化学方程式是_______ ;若该氢化物和元素⑧的单质反应,则化学方程式为_______ 。
(5)⑨的最高价氧化物对应水化物的化学式为_______ ;①和⑨两元素形成化合物为_______ ;该化合物灼烧时火焰颜色为_______ 。
(6)①和⑤元素最高价氧化物对应水化物相互反应的离子方程式为_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)②③④三种元素形成的离子中,离子半径由大到小的顺序是
(3)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是
(4)元素⑦的氢化物的化学式为
(5)⑨的最高价氧化物对应水化物的化学式为
(6)①和⑤元素最高价氧化物对应水化物相互反应的离子方程式为
您最近一年使用:0次
解题方法
4 . A+、B2-、C-、D、E、F3+分别表示含10个电子的六种粒子(离子或分子)。其中:
a.A+、B2-、F3+核外电子层结构相同
b.C-是由两种元素组成二核粒子
c.D是两种元素组成的四原子分子
d.E在常温下是无色液体
e.往含F3+的溶液中滴加含C-的溶液至过量,先有白色沉淀生成,后白色沉淀消失
(1)C-的电子式:_______ 。
(2)电子式表示D的形成过程_______ 。
(3)含F3+的溶液中通入过量D,反应的离子方程式是_______ 。
(4)A单质与E反应的生成的化合物中化学键的类型是_______ 。
a.A+、B2-、F3+核外电子层结构相同
b.C-是由两种元素组成二核粒子
c.D是两种元素组成的四原子分子
d.E在常温下是无色液体
e.往含F3+的溶液中滴加含C-的溶液至过量,先有白色沉淀生成,后白色沉淀消失
(1)C-的电子式:
(2)电子式表示D的形成过程
(3)含F3+的溶液中通入过量D,反应的离子方程式是
(4)A单质与E反应的生成的化合物中化学键的类型是
您最近一年使用:0次
名校
5 . W、X、Y、Z是汽车尾气中含有的4种主要元素。W元素原子核外只有1个电子;X是金刚石的组成元素;X、Y、Z是原子序数依次递增的同一短周期元素,这三种元素原子最外层电子数之和为15。
(1)W在元素周期表中的位置为____ 。
(2)X的最高价氧化物对应的水化物的化学式为____ 。
(3)Y与Z的原子半径大小关系为:Y____ Z(填“>”或“<”)。
(4)Y的气态氢化物稳定性比Z的气态氢化物稳定性____ (填“强”或“弱”)。
(1)W在元素周期表中的位置为
(2)X的最高价氧化物对应的水化物的化学式为
(3)Y与Z的原子半径大小关系为:Y
(4)Y的气态氢化物稳定性比Z的气态氢化物稳定性
您最近一年使用:0次
2020-12-17更新
|
180次组卷
|
2卷引用:广西壮族自治区2018年12月普通高中学业水平考试化学试题
解题方法
6 . 几种短周期元素的原子半径及主要化合价如下表∶
分析判断下列说法不正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 186 | 160 | 75 | 74 |
| 主要化合价 | +1 | +2 | +5、+3、-3 | -2 |
| A.Y可在Z单质气体中燃烧生成一种化合物 |
| B.X、Y、W的离子半径由小到大的顺序是X<Y<W |
| C.X、Y的最高价氧化物对应水化物的碱性∶X>Y |
| D.X与W形成的两种常见化合物均为离子化合物 |
您最近一年使用:0次
7 . 短周期元素X、Y、Z、Q、W、R的原子序数与其常见化合价关系如下图所示。下列说法正确的是
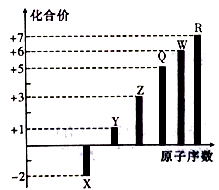

| A.X、Y、R形成的某种化合物可以用于漂白、消毒 |
| B.Q元素形成的可溶性盐的溶液不可能显酸性 |
| C.X、Y、Z、W、R的简单离子半径大小顺序为R>W>Z>Y>X |
| D.Y、Z和W三者最高价氧化物对应的水化物间不能两两相互反应 |
您最近一年使用:0次
8 . A、B、C、D四种元素都是短周期元素。A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100mL2mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍。根据上述条件,回答:
(1)元素C位于第_____ 周期______ 族,它的最高价氧化物的化学式为_______ 。
(2)A是________ 元素,B是___________ 元素,D是___________ 元素。(填元素符号)
(3)A与D形成稳定化合物的化学式为________ ,该化合物是由____________ 键形成的。写出该化合物与CO2反应的化学方程式_______________________________________ 。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为_______________________________________________________________ 。
(1)元素C位于第
(2)A是
(3)A与D形成稳定化合物的化学式为
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
您最近一年使用:0次



