名校
1 . 已知A、B、C、D、E、F、G、H是原子序数依次增大的短周期主族元素,已知A的某种原子核内没有中子,A和D,C和G分别为同一主族元素,B原子的最外层电子数比次外层多3,F的最高价氧化物的水化物既可以和强酸反应也可以和强碱溶液反应,G的单质常出现在火山口。
(1)C在元素周期表中的位置是_______ 。
(2)C、D分别形成的简单离子中,半径较大的是______ (填离子符号)。
(3)G和H的最高价氧化物的水化物酸性较强的是______ (填化学式)。
(4)由A、C、D形成的化合物中化学键的类型为_______ ,C、D形成摩尔质量为 的化合物的电子式为
的化合物的电子式为______ ,由A、B形成 化合物的结构式为
化合物的结构式为______ 。
(5)甲烷可与 组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式
组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式_______ 。
(6)D、F的最高价氧化物的水化物相互反应的离子方程式为_______ 。
(7)可用湿润的______ 试纸检验H对应单质,涉及反应的离子方程式为_______ 。
(8)由B、H形成的化合物分子中,B和H原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:________ 。
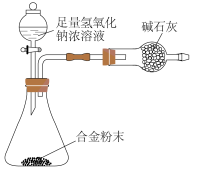
(9)E与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中E元素的含量。(装置中因空气质量引起的误差忽略不计)实验需要测定三个物理量:合金的质量m,反应前装置和药品的总质量a以及反应后装置和药品的总质量b,合金中E元素的质量分数是______ (用含m、a、b的式子表示)。
(1)C在元素周期表中的位置是
(2)C、D分别形成的简单离子中,半径较大的是
(3)G和H的最高价氧化物的水化物酸性较强的是
(4)由A、C、D形成的化合物中化学键的类型为
 的化合物的电子式为
的化合物的电子式为 化合物的结构式为
化合物的结构式为(5)甲烷可与
 组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式
组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式(6)D、F的最高价氧化物的水化物相互反应的离子方程式为
(7)可用湿润的
(8)由B、H形成的化合物分子中,B和H原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:
(9)E与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中E元素的含量。(装置中因空气质量引起的误差忽略不计)实验需要测定三个物理量:合金的质量m,反应前装置和药品的总质量a以及反应后装置和药品的总质量b,合金中E元素的质量分数是
您最近半年使用:0次
7日内更新
|
96次组卷
|
2卷引用:福建省厦门双十中学2023-2024学年高一下学期4月月考化学试题
2 . 短周期主族元素W、X、Y、Z原子序数依次增大,且最外层电子数满足W+Z=X+Y,X的简单氢化物的水溶液可刻蚀玻璃,Z的基态原子s轨道电子数比p轨道电子数少1。下列说法正确的是
| A.简单离子半径:Z>X>W |
| B.Y的单质可与水反应生成气体 |
| C.电负性:W>Y>Z |
| D.工业中可通过电解Z的氯化物得到Z的单质 |
您最近半年使用:0次
名校
解题方法
3 . 某种离子液体的阴离子结构如图,Q、W、X、Y、Z五种短周期元素的原子半径依次增大,基态Q原子的电子填充3个能级,有4对成对电子,Z与其他元素不在同一周期,下列说法正确的是
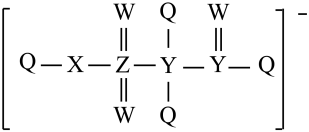
| A.最高价氧化物对应水化物的酸性:Q>X |
| B.Q、W、X的第一电离能依次减小 |
| C.氢化物的沸点:W>Y |
| D.X、Y、Z均至少有两种氧化物 |
您最近半年使用:0次
名校
解题方法
4 . 现有部分短周期元素的信息如表所示:
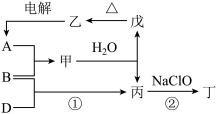
A、B、D三种单质(分别对应X、Y、Z元素组成的单质)和甲、乙、丙、丁、戊五种化合物之间的转化关系如图所示(某些条件已略去)。其中丁是一种高能燃料,分子中含有18个电子,其组成元素与丙相同。________ ,元素X的最高价氧化物的水化物和NaOH溶液反应的离子方程式为________ 。
(2)丙的结构式为________ ,丙的水溶液中浓度最高的阳离子的电子式为________ 。
(3)乙中所含的化学键类型有________ (填序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)丁的结构式为________ 。
(5)反应②中,74.5gNaClO参加反应时转移2mol电子,该反应的化学方程式为________ 。
(6)A与 、C(石墨)在高温下反应只生成乙和碳化钛(TiC),该反应的化学方程式为
、C(石墨)在高温下反应只生成乙和碳化钛(TiC),该反应的化学方程式为________ 。
元素编号 | 元素性质或原子结构信息 |
X | 第三周期元素中简单离子半径最小的元素 |
Y | 其最简单氢化物的水溶液呈碱性 |
Z | 原子核外电子数和所在周期数相等 |
(2)丙的结构式为
(3)乙中所含的化学键类型有
a.离子键 b.极性共价键 c.非极性共价键
(4)丁的结构式为
(5)反应②中,74.5gNaClO参加反应时转移2mol电子,该反应的化学方程式为
(6)A与
 、C(石墨)在高温下反应只生成乙和碳化钛(TiC),该反应的化学方程式为
、C(石墨)在高温下反应只生成乙和碳化钛(TiC),该反应的化学方程式为
您最近半年使用:0次
名校
5 . 根据表中八种短周期元素的有关信息判断,下列说法错误的是
元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A.元素②⑥形成的化合物具有两性 |
| B.元素②气态氢化物的沸点小于元素⑤气态氢化物的沸点 |
| C.⑧最高价氧化物对应的水化物的碱性为同周期中最强 |
| D.元素④位于周期表中的P区 |
您最近半年使用:0次
名校
解题方法
6 . 短周期主族元素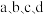 的原子序数依次增大。四种元素形成的单质依次为
的原子序数依次增大。四种元素形成的单质依次为 。而
。而 是这些元素组成的二元化合物,其中
是这些元素组成的二元化合物,其中 为形成酸雨的主要物质之一,
为形成酸雨的主要物质之一,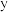 为淡黄色固体,
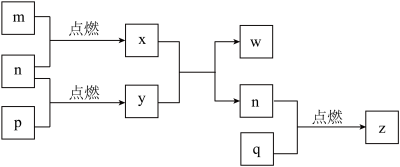
为淡黄色固体,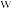 水溶液可使酚酞溶液变红。上述物质转化关系如图所示。下列说法正确的是
水溶液可使酚酞溶液变红。上述物质转化关系如图所示。下列说法正确的是
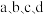 的原子序数依次增大。四种元素形成的单质依次为
的原子序数依次增大。四种元素形成的单质依次为 。而
。而 是这些元素组成的二元化合物,其中
是这些元素组成的二元化合物,其中 为形成酸雨的主要物质之一,
为形成酸雨的主要物质之一,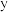 为淡黄色固体,
为淡黄色固体,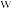 水溶液可使酚酞溶液变红。上述物质转化关系如图所示。下列说法正确的是
水溶液可使酚酞溶液变红。上述物质转化关系如图所示。下列说法正确的是
A.原子半径的大小: |
B. 的电子式一定是: 的电子式一定是: 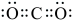 |
C.简单氢化物的沸点: |
D.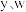 溶于水,破坏的化学键类型完全相同 溶于水,破坏的化学键类型完全相同 |
您最近半年使用:0次
名校
解题方法
7 . 五种短周期元素 的原子序数依次增大,A和C同族,
的原子序数依次增大,A和C同族, 和D同族,C离子和B离子有相同的电子层结构。
和D同族,C离子和B离子有相同的电子层结构。 和
和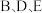 分别形成共价型化合物
分别形成共价型化合物 。
。 和
和 形成的气态化合物
形成的气态化合物 在水中呈碱性,
在水中呈碱性, 和
和 形成化合物
形成化合物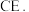 下列说法正确的是
下列说法正确的是
 的原子序数依次增大,A和C同族,
的原子序数依次增大,A和C同族, 和D同族,C离子和B离子有相同的电子层结构。
和D同族,C离子和B离子有相同的电子层结构。 和
和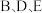 分别形成共价型化合物
分别形成共价型化合物 。
。 和
和 形成的气态化合物
形成的气态化合物 在水中呈碱性,
在水中呈碱性, 和
和 形成化合物
形成化合物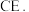 下列说法正确的是
下列说法正确的是A.气态氢化物 中热稳定性最弱的是 中热稳定性最弱的是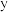 |
B.五种元素中原子半径最大的是 |
C. 最高价氧化物对应水化物的化学式为 最高价氧化物对应水化物的化学式为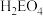 |
D.C的单质在空气中燃烧产物的化学式为 |
您最近半年使用:0次
名校
解题方法
8 . X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,则下列说法中不正确的是
| X | Y | |
| Z | W |
| A.原子半径:Z>W>Y |
| B.最高价氧化物对应水化物的酸性:Z>W>X |
| C.四种元素的单质中,Z单质的熔点最高 |
| D.W单质能与水反应,生成一种具有漂白性的物质 |
您最近半年使用:0次
名校
解题方法
9 . 2021年6月11日国家航天局公布了“祝融号”火星车拍摄的首批科学影像图。已知:火星气体及岩石中富含X、Y、Z、W四种元素,X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,其单质与冷水反应后溶液能使酚酞试液变为红色,X、W为同一主族元素,Y地壳中含量最高的元素,火星岩石含有W的最高价化合物Z2WY3。下列判断正确的是
| A.原子半径:Z>W>Y>X |
| B.W位于元素周期表第三周期VIIA族 |
| C.最高价氧化物对应水化物的酸性:X>W |
| D.X、Y、Z三种元素组成的化合物中没有离子 |
您最近半年使用:0次
名校
10 . 已知 、
、 、
、 、
、 是元素周期表的前18号元素,甲、乙、丙、丁均是由
是元素周期表的前18号元素,甲、乙、丙、丁均是由 、
、 、
、 、
、 组成的单质或化合物。
组成的单质或化合物。 的一种同位素可用于考古断代,
的一种同位素可用于考古断代, 是海洋中含量最多的元素;甲在常温下为气态,乙是一种淡黄色固体,且乙可与甲反应生成
是海洋中含量最多的元素;甲在常温下为气态,乙是一种淡黄色固体,且乙可与甲反应生成 元素的单质和丙,丁是
元素的单质和丙,丁是 元素的单质,其原子
元素的单质,其原子 层电子数等于
层电子数等于 层电子数。下列说法中错误的是
层电子数。下列说法中错误的是
 、
、 、
、 、
、 是元素周期表的前18号元素,甲、乙、丙、丁均是由
是元素周期表的前18号元素,甲、乙、丙、丁均是由 、
、 、
、 、
、 组成的单质或化合物。
组成的单质或化合物。 的一种同位素可用于考古断代,
的一种同位素可用于考古断代, 是海洋中含量最多的元素;甲在常温下为气态,乙是一种淡黄色固体,且乙可与甲反应生成
是海洋中含量最多的元素;甲在常温下为气态,乙是一种淡黄色固体,且乙可与甲反应生成 元素的单质和丙,丁是
元素的单质和丙,丁是 元素的单质,其原子
元素的单质,其原子 层电子数等于
层电子数等于 层电子数。下列说法中错误的是
层电子数。下列说法中错误的是| A.甲在工业上可作为生产丙的原料 |
| B.乙在工业领域中被广泛用于漂白剂、杀菌剂、消毒剂 |
| C.丙的水溶液呈碱性,只能与酸反应,不能与碱反应 |
D.丁在一定条件下可与甲反应生成 元素的单质 元素的单质 |
您最近半年使用:0次



