名校
1 . A、B、C、D、E、 F、G、H是周期表中前四周期的七种元素,有关性质或结构信息如下表:
(1) B元素符号为________ ,A与C以原子个数比为1:1形成的化合物的电子式为_______ ,用电子式表示C与E形成化合物的过程________ 。
(2) A、C、E所形成简单离子半径由大到小的顺序是____________ ,H的最高价氧化物对应水化物的化学式为_________ ,A、D、H的氢化物的沸点由高到低的顺序为____________________ 。
(3) 非金属性D_________ E(填“大于”或“小于”)。下列事实能证明这一结论的是________ (选填字母序号)。
a.E的熔点低于D
b.氢化物的还原性:D > E
c.最高价氧化物对应的水化物酸性:E > D
d.氢化物的酸性:E >D
| 元素 | 有关性质或结构信息 |
| A | 地壳中含量最多的元素 |
| B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
| C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
| D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
| E | E与D同周期,且在该周期中原子半径最小 |
| F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
| G | G是形成化合物种类最多的元素 |
| H | H是与D相邻的同主族元素,且原子半径:H>D |
(1) B元素符号为
(2) A、C、E所形成简单离子半径由大到小的顺序是
(3) 非金属性D
a.E的熔点低于D
b.氢化物的还原性:D > E
c.最高价氧化物对应的水化物酸性:E > D
d.氢化物的酸性:E >D
您最近一年使用:0次
名校
解题方法
2 . 元素 R、X、T、Z、Q 在元素周期表中的相对位置如图所示,其中 R 的氢化物的水溶液可以用来刻蚀玻璃,则下列判断正确的是
| R | ||
| X | T | Z |
| Q |
| A.气态氢化物的酸性:R>T>Q |
| B.气态氢化物的还原性:X>T |
| C.R 与 Q 的电子数相差 16 |
| D.R 的单质通入 T 的钠盐溶液中能置换出T 的单质 |
您最近一年使用:0次
2020-05-08更新
|
153次组卷
|
3卷引用:四川省内江市第六中学2019-2020学年高一下学期入学考试化学A试题
名校
3 . 短周期主族元素W、X、Y、Z的原子序数依次增大,它们的原子最外层电子数总和等于Z原子序数,由这四种元素组成一种化合物M具有如下性质下列推断正确的是( )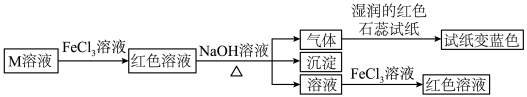

| A.原子半径Z>Y>X>W |
| B.最高价氧化物对应的水化物酸性:Y>X |
| C.简单阴离子的还原性:W<Z |
| D.W、Y、Z组成的化合物只含有共价键 |
您最近一年使用:0次
2020-04-16更新
|
207次组卷
|
9卷引用:四川省阆中中学2020届高三上学期期中考试理综化学试题
四川省阆中中学2020届高三上学期期中考试理综化学试题【全国百强校】山东省淄博实验中学2019届高三下学期寒假学习效果检测(开学考试)理科综合化学试题【全国百强校】湖北省沙市中学2019届高三理科能力测试(十三)化学试题(已下线)【南昌新东方】2019 南昌外国语 高一下 第一次月考 吉林省梅河口市第五中学2021届高三上学期第二次月考化学试题(已下线)第五章 物质结构与性质元素周期律 第28练 元素推断与无机物的性质河南省南阳市第一中学校2023-2024学年高三上学期第三次月考化学试题新疆石河子第一中学2023-2024学年高三上学期第二次月考化学试题河南省南阳市第一中学校2023-2024学年高三上学期第三次月考化学试题
名校
解题方法
4 . 前四周期主族元素V、W、X和Y,原子序数依次增大且最外层电子数之和为11,元素V的一种核素可用于文物断代,W的气态氢化物和其最高价氧化物的水化物能形成离子化合物,X是短周期原子半径最大的原子。下列说法正确的是:
| A.简单离子半径大小:r(W) < r(X ) < r(Y) |
| B.X与氧能形成两种只含离子键的化合物 |
| C.最高价氧化物对应水化物碱性:X > Y |
| D.简单氢化物的稳定性:W > V |
您最近一年使用:0次
名校
5 . 已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是
| A.X、Y、Z、W的离子半径依次减小 |
| B.W与X形成的化合物中可能含共价键 |
| C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
您最近一年使用:0次
名校
6 . 短周期主族元素R、X、Y、Z的原子序数依次增大,R元素最高正价和最低负价的代数和为2,在短周期主族元素中X原子半径最大,四种元素的原子最外层电子总数为16,Z元素形成的单质可使湿润的有色布条褪色。下列说法错误的是
| A.最高价氧化物对应水化物的碱性:X>Y |
| B.R元素的氢化物可用作制冷剂 |
| C.Y在地壳中的含量居第三 |
| D.Z形成的含氧酸酸性最强 |
您最近一年使用:0次
7 . A、B、C、D、E是四种短周期元素,A是原子半径最小的元素;B原子M层上的电子数是原子核外电子层数的2倍;C原子最外层电子数是次外层电子数的2倍;D的氢化物水溶液呈碱性;E元素的最高价氧化物的水化物是酸性最强的含氧酸。用元素符号或化学式回答下列问题:
(1)元素B的离子结构示意图为___________ 。
(2)B的最高价氧化物的水化物与D的气态氢化物形成的盐中含有的化学键:___________ 。
(3)用电子式表示A2B的形成过程___________ 。A2B与H2O沸点更高的是___________ 。
(4)DE3常温下呈液态,可与水反应生成一种酸和一种碱,写出对应的化学方程式为___________ 。
(5)CB2的结构式___________ 。
(6)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:___________
(7)工业上用H2和Cl2反应制HCl,各共价键键能数据为H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式为___________
(1)元素B的离子结构示意图为
(2)B的最高价氧化物的水化物与D的气态氢化物形成的盐中含有的化学键:
(3)用电子式表示A2B的形成过程
(4)DE3常温下呈液态,可与水反应生成一种酸和一种碱,写出对应的化学方程式为
(5)CB2的结构式
(6)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:
(7)工业上用H2和Cl2反应制HCl,各共价键键能数据为H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式为
您最近一年使用:0次
名校
8 . 短周期主族元素W、X、Y、Z,它们在周期表中位置如图所示,X的一种氢化物与其最高价氧化物对应水化物反应生成盐。下列说法正确的是
| X | Y | ||
| W | Z | ||
| T |
A.T元素单质具有半导体的特性,T与Y元素可形成两种化合物TY和 |
| B.由Y、Z和氢三种元素形成的化合物中,Z的化合价越高氧化性越强 |
| C.W的氧化物是酸性氧化物,能与碱、水反应,不能与酸反应 |
| D.X的氢化物分子中所有原子均满足8电子结构 |
您最近一年使用:0次
2020-06-09更新
|
99次组卷
|
2卷引用:四川省攀枝花市第十五中学2019-2020学年高一下学期期中考试化学试题
名校
解题方法
9 . 短周期主族元素W、X、Y 和 Z 的原子序数依次增大,W 的气态氢化物的水溶液使酚酞变红 并且可与X 的氢化物形成一种共价化合物。Y 是地壳中含量最多的金属元素,Z原子最外层电子数是其内层电子总数的 3/5。下列说法中一定正确的是
| A.它们的简单离子半径大小顺序: W<X<Y<Z |
| B.X的简单气态氢化物稳定性比Z 的强 |
| C.W的氧化物对应水化物为强酸,具有强氧化性 |
| D.工业上一般采取电解Y 的熔融氯化物来生产Y的单质 |
您最近一年使用:0次
名校
解题方法
10 . 现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于D的下一个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1。试回答:
(1)A元素在周期表中的位置为________ 、E是________ (填元素名称)。
(2)D的单质分子的结构式_______ ,C元素最高价氧化物的水化物的电子式____ 。
(3)写出工业上冶炼B单质的化学方程式_______________ 。
(4)写出CD的溶液中通入氯气的离子方程式________________ 。
(5)比较B、C、E三种元素形成的简单离子氧化性的强弱:(B、C、E离子用实际离子符号表示)氧化性_________ 。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于D的下一个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1。试回答:
(1)A元素在周期表中的位置为
(2)D的单质分子的结构式
(3)写出工业上冶炼B单质的化学方程式
(4)写出CD的溶液中通入氯气的离子方程式
(5)比较B、C、E三种元素形成的简单离子氧化性的强弱:(B、C、E离子用实际离子符号表示)氧化性
您最近一年使用:0次
2020-05-19更新
|
129次组卷
|
3卷引用:四川省仁寿第一中学校南校区2020-2021学年高一下学期开学考试化学试题



