9-10高三下·西藏拉萨·阶段练习
解题方法
1 . U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
⑴.V的单质分子的结构式为_______________ ;XW的电子式为____________ ;U元素在周期表中的位置是_____________ 。
⑵.U元素形成的同素异形体的晶体类型可能是(填序号)__________ 。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
⑶.U、V、W形成的10电子氢化物中,U、V、W的氢化物沸点最高的是(写化学式)____________ ;V、W的氢化物分子结合H+能力较强的是(写化学式)______________ ,用一个离子方程式加以证明___________________________________________ 。
请回答下列问题:
⑴.V的单质分子的结构式为
⑵.U元素形成的同素异形体的晶体类型可能是(填序号)
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
⑶.U、V、W形成的10电子氢化物中,U、V、W的氢化物沸点最高的是(写化学式)
您最近一年使用:0次
23-24高三下·陕西西安·阶段练习
2 . X、Y、Z、W为原子序数依次增大的短周期主族元素,原子序数之和为37。四种元素所形成的常见单质有三种在常温下为气体,在一定条件下,Z与X、Y、W均能形成原子个数比为1∶1的离子化合物。下列说法错误的是
| A.Y的简单氢化物在同主族元素中稳定性最强 |
| B.Y、Z所形成的物质中可能含不同种化学键 |
| C.简单离子半径:W>Z>Y>X |
| D.由X、Y两种元素组成的含18电子的分子能使酸性KMnO4溶液褪色 |
您最近一年使用:0次
3 . 有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中正确的是
| A.简单氢化物的稳定性Y>W |
| B.X、W、M三种元素形成的一种常见消毒剂,其结构中只有离子键 |
| C.元素Y与W可以形成离子化合物 |
| D.元素W和M的某些单质可作为水处理中的消毒剂 |
您最近一年使用:0次
名校
解题方法
4 . W、X、Y、Z、Q为原子序数依次增大的5种短周期元素,W的阴离子与锂离子具有相同电子层结构,X的气态氢化物可与其最高价含氧酸反应生成离子化合物,X、Y、Z的最高价氧化物对应水化物之间两两反应均可生成盐和水,Q的最高价氧化物对应的的水化物为最强含氧酸。下列说法错误的是
| A.W、Y均可以与氧原子形成1:1、1:2型化合物 |
| B.Y、Z、Q的简单离子半径大小关系:Q> Y >Z |
| C.Q元素单质具有强氧化性、漂白性 |
| D.X的氢化物稳定性比它同周期右边主族元素的氢化物稳定性差 |
您最近一年使用:0次
5 . 如图是五种短周期元素的原子序数与其在氢化物中化合价的关系图,则下列说法不正确的是
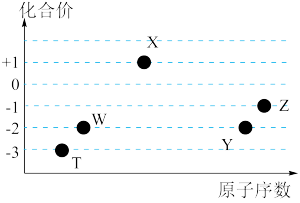

| A.X的氢化物具有很强的还原性 |
| B.YW2、ZW2、X2W2都能使品红溶液褪色,且褪色原理相同 |
| C.Y、Z元素的最高价氧化物对应的水化物都呈酸性,而且酸性:HZO4 > H2YO4 |
| D.元素W、T的氢化物的沸点比同主族中相邻的氢化物高,是因为这两种氢化物分子间存在氢键 |
您最近一年使用:0次
2020-02-06更新
|
176次组卷
|
2卷引用:西藏自治区昌都市第一高级中学2020届高三下学期第二次模拟考试理综化学试题
解题方法
6 . 短周期元素W、X、Y和Z的原子序数依次增大,元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是
| A.元素X与氢形成原子个数比为1:1的化合物有多种 |
| B.Z的原子半径比Y的原子半径大 |
| C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 |
| D.元素Z可与元素X形成共价化合物XZ2,且各微粒均满足8电子的稳定结构 |
您最近一年使用:0次
7 . 有五种短周期主族元素 X、 Y、 Z、 R、 Q, 它们的原子序数逐渐增大; 在周期表中的相对位置如图所示,Z是组成叶绿素的金属元素。下列说法错误的是
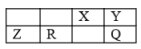

| A.工业上都用电解法制Z、R单质 |
| B.X和Y 的单质熔点: X<Y |
| C.Z、R、Y 的简单离子半径: Y>Z>R |
| D.Y和Q的最高价氧化物对应水化物酸性:Y>Q |
您最近一年使用:0次
8 . 短周期元素W、X、Y、Z的原子序数依次增加,W-与Ne具有相同的电子层结构,X的族序数等于周期数,Y与Z最外层电子数之和为10。下列说法不正确的是
| A.原子半径:X>Y>Z>W | B.单质沸点:W>Y>Z |
| C.气态氢化物的稳定性:W>Z>Y | D.简单离子半径大小:Z>W>X |
您最近一年使用:0次
名校
9 . X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增。Z的+2价阳离子电子层结构与氖相同,X、M同主族,Y在同周期主族元素中原子半径最大。Y和M可以形成Y2M型化合物。下列有关说法错误的是( )
| A.X与Y能形成两种化合物 |
| B.简单氢化物的稳定性:N>M |
| C.原子半径:r(Y)>r(M)>r(X) |
| D.Y、Z、N的最高价的氧化物的水化物两两之间能发生反应 |
您最近一年使用:0次
2019-03-09更新
|
319次组卷
|
5卷引用:西藏日喀则市南木林高级中学2021-2022学年高三上学期第三次月考理综化学试题
名校
10 . 已知V、W、X、Y、Z五种短周期元素在周期表中的位置如图所示,W的气态氢化物与Z的气态氢化物反应只能生成一种盐。则下列说法不正确的是( )。


| A.X在元素周期表中的位置为第二周期ⅥA族 |
| B.Y、Z两种元素的简单离子的半径大小关系是Y>Z |
| C.V、W的最高价氧化物对应水化物的酸性强弱为V>W |
| D.Y与Z所形成Y2Z2分子中,Y与Z均满足最外层8e-稳定结构且含有极性键和非极性键 |
您最近一年使用:0次



