解题方法
1 . 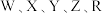 为短周期主族元素,原子序数依次增大。
为短周期主族元素,原子序数依次增大。 元素最外层电子数是次外层电子数的2倍;
元素最外层电子数是次外层电子数的2倍; 的阴离子和
的阴离子和 的阳离子与氖原子的电子层结构相同;常温下,
的阳离子与氖原子的电子层结构相同;常温下, 的单质是气体,
的单质是气体,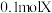 的气体与足量的氢气完全反应共有
的气体与足量的氢气完全反应共有 电子转移;
电子转移; 的单质在点燃时与
的单质在点燃时与 的单质充分反应,生成淡黄色固体,此淡黄色固体能与化合物
的单质充分反应,生成淡黄色固体,此淡黄色固体能与化合物 反应生成
反应生成 的单质;
的单质; 与
与 同族,
同族, 的气态氢化物能与其最高价含氧酸的浓溶液发生氧化还原反应。回答下列问题:
的气态氢化物能与其最高价含氧酸的浓溶液发生氧化还原反应。回答下列问题:
(1)在元素周期表中,W位于___________ 族,属于___________ 区。X、Y、R三种元素的简单离子的离子半径由小到大顺序为___________ (用离子符号表示)。
(2)X和Z的简单氢化物中,沸点更高的是___________ (填化学式),这是因为___________ 。
(3)Z元素在周期表的位置为___________ ,其非金属性比R弱,下列表述能证明这一事实的有___________ (填标号)。
A.常温下Z的单质和R的单质状态不同
B.R的简单氢化物比Z的简单氢化物稳定
C.一定条件下Z和R的单质都能与钠反应
D.Z的最高价含氧酸的酸性弱于R的最高价含氧酸
E.R的单质能与Z的简单氢化物反应生成Z的单质
(4)Z元素的低价氧化物与R单质的水溶液反应的离子方程式为___________ 。经测定 形成的氢化物
形成的氢化物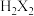 为二元弱酸,其酸性比碳酸弱,实验室常用稀硫酸处理
为二元弱酸,其酸性比碳酸弱,实验室常用稀硫酸处理 来制备
来制备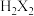 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
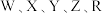 为短周期主族元素,原子序数依次增大。
为短周期主族元素,原子序数依次增大。 元素最外层电子数是次外层电子数的2倍;
元素最外层电子数是次外层电子数的2倍; 的阴离子和
的阴离子和 的阳离子与氖原子的电子层结构相同;常温下,
的阳离子与氖原子的电子层结构相同;常温下, 的单质是气体,
的单质是气体,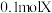 的气体与足量的氢气完全反应共有
的气体与足量的氢气完全反应共有 电子转移;
电子转移; 的单质在点燃时与
的单质在点燃时与 的单质充分反应,生成淡黄色固体,此淡黄色固体能与化合物
的单质充分反应,生成淡黄色固体,此淡黄色固体能与化合物 反应生成
反应生成 的单质;
的单质; 与
与 同族,
同族, 的气态氢化物能与其最高价含氧酸的浓溶液发生氧化还原反应。回答下列问题:
的气态氢化物能与其最高价含氧酸的浓溶液发生氧化还原反应。回答下列问题:(1)在元素周期表中,W位于
(2)X和Z的简单氢化物中,沸点更高的是
(3)Z元素在周期表的位置为
A.常温下Z的单质和R的单质状态不同
B.R的简单氢化物比Z的简单氢化物稳定
C.一定条件下Z和R的单质都能与钠反应
D.Z的最高价含氧酸的酸性弱于R的最高价含氧酸
E.R的单质能与Z的简单氢化物反应生成Z的单质
(4)Z元素的低价氧化物与R单质的水溶液反应的离子方程式为
 形成的氢化物
形成的氢化物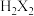 为二元弱酸,其酸性比碳酸弱,实验室常用稀硫酸处理
为二元弱酸,其酸性比碳酸弱,实验室常用稀硫酸处理 来制备
来制备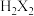 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . W、X、Y、Z 是原子序数依次增大的四种短周期元素。W 的气态氢化物能使紫色石蕊溶液变蓝,W、X和Y三种元素的最高价氧化物的水化物两两之间可以发生反应,W、X、Y、Z 的最外层电子数之和为 16。回答下列问题:
(1)Z 单质的电子式是__ 。W的气态氢化物能使紫色石蕊溶液变蓝的原因__ (用化学方程式表示)。
(2)X、Y、Z 三种元素的简单离子的离子半径由大到小的顺序是____ (用离子符号表示)。
(3)不能能证明Z的非金属性比W强的实验事实是____ (填字母)。
A.HZ的稳定性比WH3的稳定性性强
B.Z2与H2化合比W2与H2化合容易
C.HZ的水溶液酸性比WH3的水溶液酸性强
D.Z的最高价氧化物对应水化物的酸性比W强
(4)Z和氧元素、硫元素组成的SOZ2是一种液态化合物,沸点为77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色。请写出SOZ2和水反应的化学方程式_ 。
(5) Y和Z两元素形成化合物中化学键的类型为____ 。
(6)用电子式表示X2O的形成过程____ 。
(7)砷(As)与W位于同一主族,下列推断正确的是_____ (填序号)。
①砷元素的最低负化合价为−3价
②砷的最高价氧化物对应的水化物属于酸
③热稳定性:AsH3>NH3
(1)Z 单质的电子式是
(2)X、Y、Z 三种元素的简单离子的离子半径由大到小的顺序是
(3)不能能证明Z的非金属性比W强的实验事实是
A.HZ的稳定性比WH3的稳定性性强
B.Z2与H2化合比W2与H2化合容易
C.HZ的水溶液酸性比WH3的水溶液酸性强
D.Z的最高价氧化物对应水化物的酸性比W强
(4)Z和氧元素、硫元素组成的SOZ2是一种液态化合物,沸点为77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色。请写出SOZ2和水反应的化学方程式
(5) Y和Z两元素形成化合物中化学键的类型为
(6)用电子式表示X2O的形成过程
(7)砷(As)与W位于同一主族,下列推断正确的是
①砷元素的最低负化合价为−3价
②砷的最高价氧化物对应的水化物属于酸
③热稳定性:AsH3>NH3
您最近一年使用:0次
名校
3 . 已知A、B、C、D、E五种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,C与A同主族;A与B、D、E所形成的常见化合物在常温下均呈气态,在周期表中D与E左右相邻,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数与E的最外层电子数相同。
请回答下列问题:
(1)B在元素周期表的位置为________________________ 。
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序为_________ (用离子符号表示)。
(3)A、B、E可组成一种化合物,其原子个数之比为4:1:1,该化合物的水溶液与C的最高价氧化物的水化物反应的离子方程式为__________________________________________________ 。
(4)B的一种氢化物分子中含有18个电子,其化学式为_________________ 。
(5)BE3在常温下是一种淡黄色的液体,遇水即发生水解可生成一种具有漂白性的物质和一种核外电子总数为10的气体,写出该反应的化学方程式_________________________________ 。
(6)下列事实能证明D与E非金属性强弱的是__________ (选填字母序号)。
A.比较这两种元素的气态氢化物的沸点 B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性 D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(7)已知D、E两种元素形成的化合物H,H结构与过氧化氢相似。5.4g的H中含有的电子数目为_______________ 。
请回答下列问题:
(1)B在元素周期表的位置为
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序为
(3)A、B、E可组成一种化合物,其原子个数之比为4:1:1,该化合物的水溶液与C的最高价氧化物的水化物反应的离子方程式为
(4)B的一种氢化物分子中含有18个电子,其化学式为
(5)BE3在常温下是一种淡黄色的液体,遇水即发生水解可生成一种具有漂白性的物质和一种核外电子总数为10的气体,写出该反应的化学方程式
(6)下列事实能证明D与E非金属性强弱的是
A.比较这两种元素的气态氢化物的沸点 B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性 D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(7)已知D、E两种元素形成的化合物H,H结构与过氧化氢相似。5.4g的H中含有的电子数目为
您最近一年使用:0次
解题方法
4 . 现有部分短周期元素的性质或原子结构如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是___ 。
(2)元素Y与氢元素形成一种离子YH ,写出该微粒的化学式:
,写出该微粒的化学式:___ (用元素符号表示).
(3)元素Z与元素T相比,非金属性较强的是___ (用元素符号表示),下列表述中能证明这一事实的是___ 。
①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是___ (填化学式),理由是_____ ;Z的最高价氧化物对应的水化物与W的最高价氧化物对应的水化物反应的离子方程式为___ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| W | 其单质既能跟酸反应,又能跟碱反应,都产生H2 |
(2)元素Y与氢元素形成一种离子YH
 ,写出该微粒的化学式:
,写出该微粒的化学式:(3)元素Z与元素T相比,非金属性较强的是
①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是
您最近一年使用:0次
2020-07-02更新
|
43次组卷
|
2卷引用:甘肃省陇南市徽县二中2020-2021学年高一下学期第一次月考化学试题
2007·天津·高考真题
真题
解题方法
5 . U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为_______ ;XW的电子式为_______ ;Z元素在周期表中的位置是_______ 。
(2)U元素形成的同素异形体的晶体类型可能是(填序号)_______ 。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)_______ ;V、W的氢化物分子结合H+能力较强的是(写化学式)_______ ,用一个离子方程式加以证明_______ 。
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为_______ ,由此可知VW和YW2还原性较强的是(写化学式)_______ 。
请回答下列问题:
(1)V的单质分子的结构式为
(2)U元素形成的同素异形体的晶体类型可能是(填序号)
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为
您最近一年使用:0次
2010·甘肃·二模
解题方法
6 . A、B、C、D、E、F是元素周期表中六种短周期元素,请根据表中信息回答下列问题
(1)元素B 的离子结构示意图__________ 元素F的最高价氧化物的化学式__________ 。
(2)元素A、D分别与元素C 形成原子个数比为1:2的化合物甲和1:1 的化合物乙,则甲属于_________ 分子(填“极性”或“非极性”),化合物乙的电子式________ ,甲与乙反应的化学方程式为______________________________________ 。
(3)元素B、D组成化合物丙,其晶体类型为_______ ,化合物丙的溶液呈_____ (填“酸性”“碱性”或“中性”)。
(4)元素A与氢元素组成的最简单的化合物丁是一种优质燃料,燃烧热值高。
①实验测得,在常温常压下,1g化合物丁完全燃烧生成液态水,放出55.65 kJ 热量。则表示化合物丁的燃烧热的热化学方程式为_________________________________________________ 。
②某实验小组依据丁燃烧的反应原理,设计如下图所示的电池装置。

a.该电池正极的电极反应为______________________________ 。
b.工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为_______________________________________ 。
(5)G也是短周期元素,其核外电子层数与最外层电子数相等,且与E处于元素周期表中对角线位置,它们的单质及其化合物的性质相似,写出G的氧化物与NaOH溶液反应的离子方程式:________ 。若E的氯化物熔沸点较低、易升华,则E的氯化物是_______ 化合物(填“离子”或“共价”),试设计一个简单实验证明你的选择________________ 。
| 元素 | A | B | C | D | E | F |
性质或结构信息 | 形成化合物种类最多的元素 | 最高正价是最低负价绝对值的3倍 | 族序数等于周期数的3倍 | 周期数是族序数的3倍 | 地壳中含量最高的金属元素 | 最高价氧化物对应水化物是最强的含氧酸 |
(2)元素A、D分别与元素C 形成原子个数比为1:2的化合物甲和1:1 的化合物乙,则甲属于
(3)元素B、D组成化合物丙,其晶体类型为
(4)元素A与氢元素组成的最简单的化合物丁是一种优质燃料,燃烧热值高。
①实验测得,在常温常压下,1g化合物丁完全燃烧生成液态水,放出55.65 kJ 热量。则表示化合物丁的燃烧热的热化学方程式为
②某实验小组依据丁燃烧的反应原理,设计如下图所示的电池装置。

a.该电池正极的电极反应为
b.工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为
(5)G也是短周期元素,其核外电子层数与最外层电子数相等,且与E处于元素周期表中对角线位置,它们的单质及其化合物的性质相似,写出G的氧化物与NaOH溶液反应的离子方程式:
您最近一年使用:0次
23-24高三上·安徽·阶段练习
名校
解题方法
7 . X、Y、Z、W是原子序数依次增大的前20号元素,常温下只有一种元素的单质为气态。基态X原子s轨道上的电子数是p轨道上的2倍,Y的简单氢化物与其最高价含氧酸反应会产生白烟,Z与X形成的某种化合物常温下为液体,基态W原子有1个未成对电子。下列说法错误的是
| A.氢化物的沸点:Y>Z>X |
| B.电负性:Y>Z>X>W |
| C.原子半径:W>Z>X>Y |
| D.上述元素形成的某种化合物的溶液可用于检测Fe3+ |
您最近一年使用:0次
8 . 短周期主族元素X、Y、Z、U、V、W在元素周期表中的相对位置如图所示。已知:常温常压下,W的单质为黄绿色气体。下列说法错误的是
| Y | Z | U | ||
| X | V | W |
A.简单离子半径: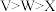 |
B.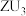 分子中所有原子均达到了8电子稳定结构 分子中所有原子均达到了8电子稳定结构 |
C.最高价氧化物对应水化物的酸性: |
| D.Z的最简单氢化物的水溶液呈酸性 |
您最近一年使用:0次
2023-07-14更新
|
50次组卷
|
2卷引用:甘肃省部分学校2022-2023学年高一下学期期末考试化学试题
解题方法
9 . 离子液体是在室温或接近室温时呈液态的盐类物质。某离子液体结构中,Q、R、T、X、Y和Z是原子序数依次增大的短周期主族元素,基态T原子和Y原子最外层均有两个单电子,Q、R、X和Z质子数均为奇数且和为22。下列说法错误的是
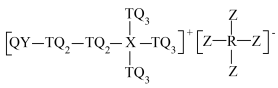
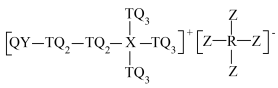
A.电负性: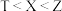 |
B.化合物中 和 和 均为 均为 杂化 杂化 |
| C.该离子液体难挥发,可用作溶剂 |
| D.该离子液体中含非极性键,不含配位键 |
您最近一年使用:0次
名校
10 . 某陶瓷颗粒增强材料(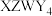 )由X、Y、Z、W四种短周期主族元素组成,其中X与Y、Z与W分别同周期,四种元素的原子半径与最外层电子数的关系如图所示。下列说法错误的是
)由X、Y、Z、W四种短周期主族元素组成,其中X与Y、Z与W分别同周期,四种元素的原子半径与最外层电子数的关系如图所示。下列说法错误的是
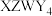 )由X、Y、Z、W四种短周期主族元素组成,其中X与Y、Z与W分别同周期,四种元素的原子半径与最外层电子数的关系如图所示。下列说法错误的是
)由X、Y、Z、W四种短周期主族元素组成,其中X与Y、Z与W分别同周期,四种元素的原子半径与最外层电子数的关系如图所示。下列说法错误的是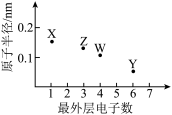
| A.简单离子半径:Y>Z |
| B.最简单氢化物的热稳定性:Y>W |
C.该物质中各元素的最外层均满足 结构 结构 |
| D.工业上通过电解Z、Y的化合物(熔融)冶炼Z单质 |
您最近一年使用:0次
2023-04-21更新
|
526次组卷
|
5卷引用:甘肃省武威第一中学2023-2024学年高三上学期第三次月考化学试题
甘肃省武威第一中学2023-2024学年高三上学期第三次月考化学试题(已下线)2023年普通高中学业水平选择性考试化学押题卷(六)(已下线)化学-2023年高考押题预测卷02(天津卷)(含考试版、全解全析、参考答案、答题卡)湖南省长沙市雅礼中学2023-2024学年高三上学期一模化学试题(已下线)通关练06 元素位-构-性推断-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)



