解题方法
1 . 在短周期元素中有部分元素的原子具有核外电子排布有2个未成对电子的特点。具有这样特点的元素中:
(1)A元素原子的半径最大,写出A在元素周期表中的位置___________ ,其原子核外电子排布式为___________ ,A与上述元素中原子半径最小的元素B形成的化合物晶体类型为___________ 。
(2)C元素的单质能溶解于C与D形成的化合物中,写出该化合物的分子式___________ ,推断该化合物___________ (难、微、易)溶于水。
(3)C、D元素均可与B元素形成化合物,此2种化合物都可与水反应形成对应的酸,2种酸的分子式相似,写出2种酸的分子式___________ ,简述证明2种酸酸性相对强弱的方法___________ 。
Cu2S和CuS均可被KMnO4酸性溶液氧化,在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① + Cu2S +
+ Cu2S + →
→ + SO2↑ +
+ SO2↑ + + H2O(未配平)
+ H2O(未配平)
② + CuS +
+ CuS + →
→ + SO2↑ +
+ SO2↑ + + H2O(未配平)
+ H2O(未配平)
(4)下列关于反应①的说法中错误的是___________ (选填编号)。
a.还原性的强弱关系是: > Cu2S
> Cu2S
b.氧化剂与还原剂的物质的量之比为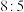
c.生成2.24L(标况下)SO2,转移电子的物质的量是0.8mol
d.被氧化的元素是正一价的Cu和负二价的S
(4)写出反应②中反应物配平后的系数并标出电子转移方向和数目:___________
___________ +___________CuS +___________
+___________CuS +___________
已知:KMnO4在稀硫酸存在下能将H2O2氧化为O2,KMnO4被还原为 ;H2O2在前面反应生成
;H2O2在前面反应生成 的催化下能发生分解反应生成H2O和O2。
的催化下能发生分解反应生成H2O和O2。
(5)稀硫酸中,某KMnO4和H2O2发生氧化还原反应方程式如下:
2KMnO4 + 7H2O2 + 3H2SO4 → K2SO4 + 2MnSO4 + 6O2↑ + 10H2O,反应中1mol KMnO4氧化H2O2的物质的量是___________ mol, 反应中的氧化剂是___________ ,氧化剂与还原剂的物质的量比为___________ 。
(1)A元素原子的半径最大,写出A在元素周期表中的位置
(2)C元素的单质能溶解于C与D形成的化合物中,写出该化合物的分子式
(3)C、D元素均可与B元素形成化合物,此2种化合物都可与水反应形成对应的酸,2种酸的分子式相似,写出2种酸的分子式
Cu2S和CuS均可被KMnO4酸性溶液氧化,在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①
 + Cu2S +
+ Cu2S + →
→ + SO2↑ +
+ SO2↑ + + H2O(未配平)
+ H2O(未配平)②
 + CuS +
+ CuS + →
→ + SO2↑ +
+ SO2↑ + + H2O(未配平)
+ H2O(未配平)(4)下列关于反应①的说法中错误的是
a.还原性的强弱关系是:
 > Cu2S
> Cu2Sb.氧化剂与还原剂的物质的量之比为
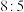
c.生成2.24L(标况下)SO2,转移电子的物质的量是0.8mol
d.被氧化的元素是正一价的Cu和负二价的S
(4)写出反应②中反应物配平后的系数并标出电子转移方向和数目:
___________
 +___________CuS +___________
+___________CuS +___________
已知:KMnO4在稀硫酸存在下能将H2O2氧化为O2,KMnO4被还原为
 ;H2O2在前面反应生成
;H2O2在前面反应生成 的催化下能发生分解反应生成H2O和O2。
的催化下能发生分解反应生成H2O和O2。(5)稀硫酸中,某KMnO4和H2O2发生氧化还原反应方程式如下:
2KMnO4 + 7H2O2 + 3H2SO4 → K2SO4 + 2MnSO4 + 6O2↑ + 10H2O,反应中1mol KMnO4氧化H2O2的物质的量是
您最近一年使用:0次
2010·上海浦东新·一模
解题方法
2 . 现有部分短周期元素的性质或结构如下表:
(1)X原子中电子运动状态共有____ 种。Z元素最简单的气态氢化物分子的空间构型是___ 。
(2)写出Y元素最高价氧化物对应水化物的电离方程式____________ 。
(3)下列说法能证明M、Z、X三种元素形成的化合物属于离子化合物的是______ 。
a.熔点比氯化钠高 b.水溶液能导电 c.液态时能导电 d.固体能导电
(4)与X同周期且非金属性强于X的元素是______ (填元素名称),写出能说明这一事实的化学方程式___________ 。
| 元素编号 | 元素性质或结构 |
| X | 海水中质量分数最大的元素,其氢化物是最常用的溶剂 |
| Y | 地壳中含量最多的金属元素 |
| Z | 形成化合物最多的元素 |
| M | 短周期主族元素中原子半径最大的元素 |
(2)写出Y元素最高价氧化物对应水化物的电离方程式
(3)下列说法能证明M、Z、X三种元素形成的化合物属于离子化合物的是
a.熔点比氯化钠高 b.水溶液能导电 c.液态时能导电 d.固体能导电
(4)与X同周期且非金属性强于X的元素是
您最近一年使用:0次
3 . 化合物X(只含有一种阳离子)由三种短周期元素组成,按照如下流程进行实验。已知固体A为一种单质和一种化合物的混合物,溶液C的焰色反应星黄色。
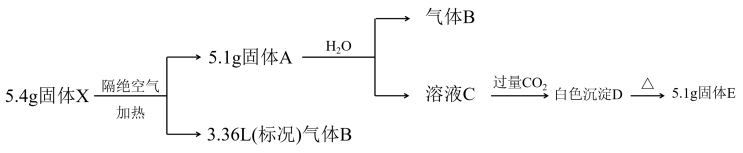
(1)E的化学式为_______ ,化合物X中阴离子的电子式为_______ 。
(2)写出确定气体B的依据:_______ 。
(3)上述流程中溶液C生成白色沉淀D的离子方程式为_______ 。
(4)化合物X在加热条件下可将CuO还原成Cu,反应化学方程式为_______ 。A中的化合物在加热条件下也可以将CuO还原成Cu,取足量A中的化台物与W g CuO(设CuO完全反应)共热,请设计实验证明还原产物的组成_______ 。(提示:CuO的还原产物可能为 ,
, 在酸性条件下不稳定,发生反应为
在酸性条件下不稳定,发生反应为
 )
)

(1)E的化学式为
(2)写出确定气体B的依据:
(3)上述流程中溶液C生成白色沉淀D的离子方程式为
(4)化合物X在加热条件下可将CuO还原成Cu,反应化学方程式为
 ,
, 在酸性条件下不稳定,发生反应为
在酸性条件下不稳定,发生反应为
 )
)
您最近一年使用:0次
2021·山东·模拟预测
名校
4 . X、Y、Z、W为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W形成的最高价氧化物分别为甲、乙、丙。x、y2、z、w分别为X、Y、Z、W的单质,丁是化合物。其转化关系如图所示,下列判断正确的是
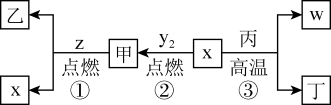

| A.反应①、②属于氧化还原反应,③属于非氧化还原反应 |
| B.Y的离子半径比Z的离子半径大 |
| C.反应③可以证明X的非金属性强于W |
| D.一定条件下,x与甲反应生成丁 |
您最近一年使用:0次
解题方法
5 . 短周期主族元素W、X、Y、Z的原子序数依次增加,m、n、p是由这些元素组成的二元化合物,r是一种气态单质,n为淡黄色粉末,相关物质转化关系如图所示。室温下,0. 0lmol/L的s溶液pH为12,X的质子数是W与Z的质子数之和的一半。下列说法正确的是
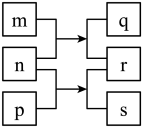

| A.原子半径:W<X<Y |
| B.简单氢化物沸点:Z<X<Y |
| C.n、s中均含有离子键和共价键 |
| D.q溶于水时温度升高,证明其水解过程放热 |
您最近一年使用:0次
解题方法
6 . 短周期主族元素R、X、Y、Z的原子序数依次增大,R、Y位于同主族,X2 YR3水溶液在空气中久置,其溶液由碱性变为中性。下列说法正确的是( )
| A.简单离子半径:X>Y>Z>R |
| B.X2Y与Z2反应可证明Z的非金属性比Y强 |
| C.Y的氧化物对应的水化物一定是强酸 |
| D.X和R组成的化合物只含一种化学键 |
您最近一年使用:0次
11-12高三上·上海·期末
解题方法
7 . U、V、W、X、Y是原子序数依次增大的五种短周期常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体
请回答下列问题:
(1)V元素原子的L层电子排布式为__________________ ;XW的电子式为____________ 。
(2)U元素形成的同素异形体的晶体类型可能是(填序号)__________ 。
①原子晶体②离子晶体③分子晶体④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)________________ ;V、W的氢化物分子结合H+能力较强的是(写化学式)____________ ,用一个离子方程式加以证明________________________ 。
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为_____________________________ ,由此可知VW和YW2还原性较强的是(写化学式)__________________________________ 。
请回答下列问题:
(1)V元素原子的L层电子排布式为
(2)U元素形成的同素异形体的晶体类型可能是(填序号)
①原子晶体②离子晶体③分子晶体④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为
您最近一年使用:0次
名校
解题方法
8 . W、X、Y、Z为原子序数依次递增的前20号主族元素。W、Y均为非金属元素,而W、Z的最外层电子数之比为2:1,X是地壳中含量最高的金属元素,X、Y形成的二元化合物溶水后同时生成沉淀和臭鸡蛋气味的气体,下列说法正确的是( )
| A.Z对应的金属氢化物只存在离子键 |
| B.X、Z分别对应的金属氯化物的水溶液均呈酸性 |
| C.H2YO3的酸性比H2WO3强,则证明非金属性:Y>W |
| D.Y的两种气态氧化物分别通入BaCl2溶液中均产生白色沉淀 |
您最近一年使用:0次
2019-03-27更新
|
1178次组卷
|
2卷引用:广东省珠海市2019届高三第一学期学业质量监测理科综合化学试题
2007·天津·高考真题
真题
解题方法
9 . U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为_______ ;XW的电子式为_______ ;Z元素在周期表中的位置是_______ 。
(2)U元素形成的同素异形体的晶体类型可能是(填序号)_______ 。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)_______ ;V、W的氢化物分子结合H+能力较强的是(写化学式)_______ ,用一个离子方程式加以证明_______ 。
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为_______ ,由此可知VW和YW2还原性较强的是(写化学式)_______ 。
请回答下列问题:
(1)V的单质分子的结构式为
(2)U元素形成的同素异形体的晶体类型可能是(填序号)
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为
您最近一年使用:0次
名校
解题方法
10 . 如图是元素周期表的一部分:
(1)元素⑩原子结构示意图为__________ 。
(2)元素③④的第一电离能大小关系为_______ (填化学用语,下同),原因是__________________ ,④-⑧中最高价氧化物对应水化物酸性最强的是_______ 。
(3)写出元素⑦的最高价氧化物与NaOH溶液反应的离子方程式_________ 。
(4)元素⑤ 与⑧ 元素相比,非金属性较强的是__________ (用元素符号表示),下列表述中能证明这一事实的是__________ 。
A.气态氢化物的挥发性和稳定性 B.两元素的电负性
C.单质分子中的键能 D.含氧酸的酸性
E.氢化物中X—H键的键长 F.两单质在自然界中的存在形式
(5)根据下列五种元素的第一至第四电离能数据(单位:KJ·mol﹣1),回答下面各题:
①T元素最可能是________ (填“s”、“p”、“d”、“ds”等)区元素;在周期表中,最可能处于同一主族的是_________ 。(填元素代号 );
②下列离子的氧化性最弱的是______________ 。
A.S2+ B.R2+ C.U+ D.T3+

(1)元素⑩原子结构示意图为
(2)元素③④的第一电离能大小关系为
(3)写出元素⑦的最高价氧化物与NaOH溶液反应的离子方程式
(4)元素⑤ 与⑧ 元素相比,非金属性较强的是
A.气态氢化物的挥发性和稳定性 B.两元素的电负性
C.单质分子中的键能 D.含氧酸的酸性
E.氢化物中X—H键的键长 F.两单质在自然界中的存在形式
(5)根据下列五种元素的第一至第四电离能数据(单位:KJ·mol﹣1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
②下列离子的氧化性最弱的是
A.S2+ B.R2+ C.U+ D.T3+
您最近一年使用:0次
2018-04-19更新
|
197次组卷
|
2卷引用:福建省华安一中、长泰一中等四校2017-2018学年高二下学期第一次(4月)联考化学试题



