解题方法
1 . N、P、 是重要的氮族元素,氮族元素的单质及其化合物的应用较为广泛。回答下列问题:
是重要的氮族元素,氮族元素的单质及其化合物的应用较为广泛。回答下列问题:
(1)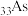 与P位于同一主族,磷原子的结构示意图为
与P位于同一主族,磷原子的结构示意图为___________ ,砷在周期表中的位置是___________ 。
(2)下列能说明N和P非金属性相对强弱的是___________(填标号)。
(3)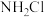 比
比 稳定性高,易水解,因水解后能产生可杀菌消毒的物质而成为饮用水的缓释消毒剂,
稳定性高,易水解,因水解后能产生可杀菌消毒的物质而成为饮用水的缓释消毒剂,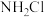 发生水解的化学方程式为
发生水解的化学方程式为___________ 。
(4)白磷有剧毒,白磷中毒可用硫酸铜溶液解毒,白磷与硫酸铜反应如下: ,反应中
,反应中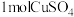 可氧化
可氧化___________ 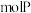 。
。
 是重要的氮族元素,氮族元素的单质及其化合物的应用较为广泛。回答下列问题:
是重要的氮族元素,氮族元素的单质及其化合物的应用较为广泛。回答下列问题:(1)
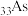 与P位于同一主族,磷原子的结构示意图为
与P位于同一主族,磷原子的结构示意图为(2)下列能说明N和P非金属性相对强弱的是___________(填标号)。
A. 比 比 稳定性强 稳定性强 |
B. 溶液与 溶液与 反应生成 反应生成 |
| C.硝酸显强氧化性,磷酸不显强氧化性 |
| D.常温下,氮气是气体,磷单质是固体 |
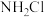 比
比 稳定性高,易水解,因水解后能产生可杀菌消毒的物质而成为饮用水的缓释消毒剂,
稳定性高,易水解,因水解后能产生可杀菌消毒的物质而成为饮用水的缓释消毒剂,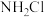 发生水解的化学方程式为
发生水解的化学方程式为(4)白磷有剧毒,白磷中毒可用硫酸铜溶液解毒,白磷与硫酸铜反应如下:
 ,反应中
,反应中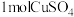 可氧化
可氧化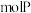 。
。
您最近一年使用:0次
20-21高二下·福建泉州·期中
解题方法
2 . 原子序数依次增加的前四周期的主族元素A~I,有关性质如下:
已知E的单质是一种常见的半导体材料,分析表中数据,回答有关问题:
(1)元素G在周期表中的位置是___________ ,元素B的气态氢化物的电子式为___________ 。
(2)元素A、B、G可形成化合物BA4G属于___________ 晶体(填“离子”、“分子”或“原子”)。
(3)元素D、G、I的非金属性由强到弱的顺序是___________ (用元素符号表示),元素C、D的气态氢化物的稳定性顺序为___________ (用化学式表示)
| 元素代号 | A | B | C | D | E | F | G | H | I |
| 原子半径/nm | 0.037 | 0.074 | 0.073 | 0.071 | 0.143 | 0.102 | 0.099 | 0.197 | 0.114 |
| 主要化合价 | +1 | +5、-3 | -2 | -1 | +4、-4 | +6、-2 | +7、-1 | +2 | +7、-1 |
已知E的单质是一种常见的半导体材料,分析表中数据,回答有关问题:
(1)元素G在周期表中的位置是
(2)元素A、B、G可形成化合物BA4G属于
(3)元素D、G、I的非金属性由强到弱的顺序是
您最近一年使用:0次
名校
解题方法
3 . 下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,用相应的化学用语 回答下列问题;
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号_______ 。
(2)④、⑦、⑩的离子半径由大到小的顺序为_______ (用元素符号作答)。
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式____ ,该物质含有的化学键类型有_____ 。
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为____ ,元素⑤和⑩的氢化物中,酸性更强的是_____ 。
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程____ 。
| ① | |||||||
| ② | ③ | ④ | ⑤ | ||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号
(2)④、⑦、⑩的离子半径由大到小的顺序为
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程
您最近一年使用:0次
2021-05-24更新
|
190次组卷
|
4卷引用:四川省遂宁市第二中学2020-2021学年高一下学期半期考试化学试题
四川省遂宁市第二中学2020-2021学年高一下学期半期考试化学试题(已下线)专题03 化学键【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版必修2)江西省南昌市进贤县第一中学2020-2021学年高一下学期期末考试化学试题河南省部分名校2020-2021学年高一下学期期末联考化学试题
20-21高二·全国·课时练习
4 . A、B、C都是短周期元素。B、C的离子核外电子排布相同,组成B2C型离子化合物。A、B元素的化合价相同,A、C元素组成的化合物中,A占11.1%,在标准状况下,0.04 mol B元素的单质与水完全反应放出448 mL H2。
(1)写出各元素的符号:A是______ ,B是______ ,C是______ 。
(2)写出A元素组成的单质的电子式:______ ,分子中的化学键有______ 。
(3)写出A和C组成的化合物的电子式:______ 。
(4)A、C还可以形成另一种化合物,该化合物是一种氧化剂,其溶液有弱酸性,试写出其电子式:______ 。分子中的化学键有______ 共价键和______ 共价键。
(1)写出各元素的符号:A是
(2)写出A元素组成的单质的电子式:
(3)写出A和C组成的化合物的电子式:
(4)A、C还可以形成另一种化合物,该化合物是一种氧化剂,其溶液有弱酸性,试写出其电子式:
您最近一年使用:0次
20-21高二·全国·课时练习
5 . 元素X和Y属于同一主族。负二价的元素X和氢的化合物在通常状况下是一种液体,其中X的质量分数为88.9%;元素X和元素Y可以形成两种化合物,在这两种化合物中,X的质量分数分别为50%和60%。
(1)确定X、Y两种元素在周期表中的位置分别为________________ 、________________ 。
(2)在元素X和元素Y两种元素形成的化合物中,写出X质量分数为50%的化合物的化学式_______ ;该分子的中心原子以_______ 杂化,分子构型为_______ 。
(3)写出X的质量分数为60%的化合物的化学式________________ ;该分子的中心原子以________ 杂化,分子构型为________ 。
(4)由氢元素与X元素形成的化合物中,含有非极性键的是________ (写分子式),分子构型为V形的是________ (写分子式)。
(1)确定X、Y两种元素在周期表中的位置分别为
(2)在元素X和元素Y两种元素形成的化合物中,写出X质量分数为50%的化合物的化学式
(3)写出X的质量分数为60%的化合物的化学式
(4)由氢元素与X元素形成的化合物中,含有非极性键的是
您最近一年使用:0次
解题方法
6 . 8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价(或最低负化合价)的变化如图所示。

已知:X为元素周期表中相对原子质量最小的元素,B为氮元素。请回答下列问题:
(1)A在元素周期表中的位置是_______________ ;G的原子结构示意图为__________________ 。
(2)X2D电子式为___________________ 。
(3)写出单质E与H2O反应的化学方程式__________________ 。
(4)下列有关物质性质的推断,正确的是_________________ (填“序号”)。
a.金属性:E>G b.氢化物的稳定性:D<L c.最高价氧化物的水化物酸性:L<Q
(5)Q的单质通入淀粉-KI溶液,溶液变蓝,写出该反应的离子方程式___________________ ,该实验说明Q的非金属性强于碘,请从原子结构的角度解释其原因______________________ 。

已知:X为元素周期表中相对原子质量最小的元素,B为氮元素。请回答下列问题:
(1)A在元素周期表中的位置是
(2)X2D电子式为
(3)写出单质E与H2O反应的化学方程式
(4)下列有关物质性质的推断,正确的是
a.金属性:E>G b.氢化物的稳定性:D<L c.最高价氧化物的水化物酸性:L<Q
(5)Q的单质通入淀粉-KI溶液,溶液变蓝,写出该反应的离子方程式
您最近一年使用:0次
19-20高一·全国·假期作业
解题方法
7 . X、Y、Z、M、R、Q是短周期主族元素,部分信息如表所示:
①表中与X位于同族的元素是_______ (填元素符号),该元素对应离子的结构示意图为_______ 。
②Y与R相比,非金属性较强的是___ (用元素符号表示),下列事实能证明这一结论的是____ (填母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性: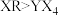
c.最高价氧化物对应水化物的酸性: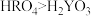
③根据表中数据推测,Y的原子半径的范围是_______ 。
④Z、Q的最高价氧化物对应的水化物在水中反应生成盐的化学式是_______ 。
| X | Y | Z | M | R | Q | |
原子半径/nm | 0. 186 | 0.074 | 0.099 | 0. 143 | ||
主要化合价 | -4, +4 | -2 | -1,+ 7 | +3 | ||
其他 | 简单阳离子核外无电子 | 无机非金属材料的“主角” | 焰色反应呈黄色 |
①表中与X位于同族的元素是
②Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:
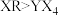
c.最高价氧化物对应水化物的酸性:
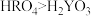
③根据表中数据推测,Y的原子半径的范围是
④Z、Q的最高价氧化物对应的水化物在水中反应生成盐的化学式是
您最近一年使用:0次
解题方法
8 . 已知A、B、C、D、E都是短周期的主族元素,原子序数依次增大,其中A是空气中含量最多的元素,C是短周期中原子半径最大的元素,C与B可形成C2B和C2B2两种物质,E是地壳中含量最多的金属元素。请回答下列问题:
(1)①A在元素周期表中的位置_______ 。
②上述元素的最高价氧化物对应的水化物中碱性最强的是_______ (填化学式)。
③写出C2B2的电子式_______ 。
(2)C、D、E三种元素对应的简单离子的半径由大到小的顺序是_______ (填离子符号)。
(3)写出单质E与 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(1)①A在元素周期表中的位置
②上述元素的最高价氧化物对应的水化物中碱性最强的是
③写出C2B2的电子式
(2)C、D、E三种元素对应的简单离子的半径由大到小的顺序是
(3)写出单质E与
 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
解题方法
9 . 随着原子序数的递增,八种短周期元素(用字母x~h表示)的原子半径相对大小、最高正价或最低负价的变化如图所示。

请回答下列问题:
(1)x形成的阴离子的结构示意图为___________ 。
(2)如果1个z原子中含8个中子,则其原子符号为___________ 。
(3)f的单质和e的最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(4)比较d、e常见离子的半径大小:___________ (填离子符号,用“>”连接)。
(5)g、h两元素最高价氧化物对应水化物的酸性更强的是___________ (填化学式)。

请回答下列问题:
(1)x形成的阴离子的结构示意图为
(2)如果1个z原子中含8个中子,则其原子符号为
(3)f的单质和e的最高价氧化物对应的水化物相互反应的化学方程式为
(4)比较d、e常见离子的半径大小:
(5)g、h两元素最高价氧化物对应水化物的酸性更强的是
您最近一年使用:0次
解题方法
10 . A、B、C、D(气体)均为常见的10电子微粒其中A(4核微粒)能使紫色石蕊溶液变红,B(2核微粒)能使酚酞溶液变红,D能使湿润的红色石蕊试纸变蓝。A与B反应可生成C。
写出各微粒的化学或离子符号。A:_____ 、B:_____ 、C:_____ 、D:_____ 。
写出各微粒的化学或离子符号。A:
您最近一年使用:0次



