名校
解题方法
1 . A、B、D、E、X是原子序数依次增大的五种短周期元素。A是形成化合物种类最多的元素;B与A同周期,B、D能形成两种化合物D2B和D2B2;D是短周期中原子半径最大的主族元素;E的周期序数和族序数相等;D、X的原子最外层电子数之和为8。
(1)A在周期表中的位置是____ ;D2B2的电子式为____ 。
(2)A的单质与浓硫酸共热,反应的化学方程式为____ 。
(3)将X单质通入如图试管中,观察到的实验现象为____ 。

说明X的非金属性强于碘,从原子结构的角度解释其原因是____ 。
(4)镓(31Ga)与E为同主族元素,氮化镓(GaN)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,GaN商用进入快车道。下列说法正确的是____ (填字母序号)。
a.Ga位于元素周期表的第四周期
b.GaN中Ga的化合价为+3
c.Ga3+的离子半径小于E3+的离子半径
(5)XB2是一种高效消毒剂,工业上用其处理中性废水中的锰,使Mn2+转化为MnO2沉淀除去,X被还原至最低价,该反应的离子方程式为____ 。
(1)A在周期表中的位置是
(2)A的单质与浓硫酸共热,反应的化学方程式为
(3)将X单质通入如图试管中,观察到的实验现象为

说明X的非金属性强于碘,从原子结构的角度解释其原因是
(4)镓(31Ga)与E为同主族元素,氮化镓(GaN)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,GaN商用进入快车道。下列说法正确的是
a.Ga位于元素周期表的第四周期
b.GaN中Ga的化合价为+3
c.Ga3+的离子半径小于E3+的离子半径
(5)XB2是一种高效消毒剂,工业上用其处理中性废水中的锰,使Mn2+转化为MnO2沉淀除去,X被还原至最低价,该反应的离子方程式为
您最近一年使用:0次
名校
2 . 下表是元素周期表的一部分,请参照元素①~⑥的位置回答下列问题:
(1)元素①的一种核素中,含有1个质子和1个中子,该核素组成的符号是_______ 。
(2)⑤的原子结构示意图是_______ 。
(3)上述元素中,原子半径最大的是_______ (写元素符号)。
(4)用电子式表示①、⑥组成的化合物的形成过程_______ 。
(5)金属性:③_______ ④(填“>”或“<”),列举一条能证明该结论的事实:_______ 。
(6)下列说法正确的是_______ (填序号)。
a.②、③组成的化合物只有一种
b.氢化物的稳定性②小于⑤
c.⑥在化合物中呈现的最高化合价为 价
价
(7)34号元素硒(Se)和⑤位于同一主族,是生命必需元素,硒酸 的酸性比
的酸性比
_______ (填“强”或“弱”),请从位 - 构 - 性角度 分析原因_______ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
(2)⑤的原子结构示意图是
(3)上述元素中,原子半径最大的是
(4)用电子式表示①、⑥组成的化合物的形成过程
(5)金属性:③
(6)下列说法正确的是
a.②、③组成的化合物只有一种
b.氢化物的稳定性②小于⑤
c.⑥在化合物中呈现的最高化合价为
 价
价(7)34号元素硒(Se)和⑤位于同一主族,是生命必需元素,硒酸
 的酸性比
的酸性比
您最近一年使用:0次
2023-01-07更新
|
374次组卷
|
2卷引用:北京市第八中学2022-2023学年高一上学期期末考试化学试题
名校
3 . A、B、D、X、Y是原子序数依次增大的五种短周期主族元素。A是地壳中含量最多的元素,A、X是同主族元素;B是短周期中原子半径最大的元素;D的周期序数和族序数相等。用化学用语回答下列问题:
(1)写出X元素的简单离子的结构示意图_______ 。
(2)A、B、D三种元素的简单离子半径从大到小的顺序是_______ (填离子符号)。
(3)B、Y两元素形成的化合物有重要用途,用电子式表示它的形成过程_______ 。
(4)写出B、D两元素的最高价氧化物对应水化物发生反应的离子方程式_______ 。
(5) 与A、X是同一主族的元素,且在元素周期表中与X相邻。
与A、X是同一主族的元素,且在元素周期表中与X相邻。
①根据元素周期律,下列推断正确的是_______ (填字母序号)。
a. 的最高正化合价为
的最高正化合价为 价 b.
价 b. 的还原性比
的还原性比 强
强
c. 的酸性比
的酸性比 强 d.
强 d. 在一定条件下可与
在一定条件下可与 溶液反应
溶液反应
②室温下向 固体表面吹入
固体表面吹入 ,可得到两种单质和
,可得到两种单质和 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(6)将Y的单质通入石蕊溶液中发生的颜色变化如下图,请在方框内填写出导致该阶段颜色变化的主要粒子符号_______ 。

(1)写出X元素的简单离子的结构示意图
(2)A、B、D三种元素的简单离子半径从大到小的顺序是
(3)B、Y两元素形成的化合物有重要用途,用电子式表示它的形成过程
(4)写出B、D两元素的最高价氧化物对应水化物发生反应的离子方程式
(5)
 与A、X是同一主族的元素,且在元素周期表中与X相邻。
与A、X是同一主族的元素,且在元素周期表中与X相邻。①根据元素周期律,下列推断正确的是
a.
 的最高正化合价为
的最高正化合价为 价 b.
价 b. 的还原性比
的还原性比 强
强c.
 的酸性比
的酸性比 强 d.
强 d. 在一定条件下可与
在一定条件下可与 溶液反应
溶液反应②室温下向
 固体表面吹入
固体表面吹入 ,可得到两种单质和
,可得到两种单质和 ,该反应的化学方程式为
,该反应的化学方程式为(6)将Y的单质通入石蕊溶液中发生的颜色变化如下图,请在方框内填写出导致该阶段颜色变化的主要粒子符号

您最近一年使用:0次
名校
4 . 原子序数由小到大排列的四种短周期元素 、
、 、
、 、
、 ,其中
,其中 、
、 、
、 与氢元素可组成
与氢元素可组成 、
、 和
和 三种共价化合物;
三种共价化合物; 与氧元素可组成
与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。
(1)写出 的电子式:
的电子式:___________ 。其中含有的化学键是___________ 。
(2)用电子式表示 的形成过程
的形成过程___________ 。
(3) 、
、 、
、 三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是___________ (填化学式)。
(4) 、
、 和
和 三种化合物,其中一种与另外两种都能反应的是
三种化合物,其中一种与另外两种都能反应的是___________ (填化学式)。
(5)由 、
、 组成的化合物分子中,
组成的化合物分子中, 、
、 原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式___________ 。
 、
、 、
、 、
、 ,其中
,其中 、
、 、
、 与氢元素可组成
与氢元素可组成 、
、 和
和 三种共价化合物;
三种共价化合物; 与氧元素可组成
与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。(1)写出
 的电子式:
的电子式:(2)用电子式表示
 的形成过程
的形成过程(3)
 、
、 、
、 三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是(4)
 、
、 和
和 三种化合物,其中一种与另外两种都能反应的是
三种化合物,其中一种与另外两种都能反应的是(5)由
 、
、 组成的化合物分子中,
组成的化合物分子中, 、
、 原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
您最近一年使用:0次
2022-04-01更新
|
204次组卷
|
13卷引用:北京四中2017-2018学年高一下学期第二次月考化学试题
北京四中2017-2018学年高一下学期第二次月考化学试题2015-2016学年江西省金溪一中高一下期中化学试卷2015-2016学年中国石油天然气管道局中学高一下第二次月考化学试卷2016-2017学年辽宁省庄河高级中学高二上开学测化学试卷2018版化学(苏教版)高考总复习专题五课时跟踪训练--微粒之间的相互作用力与物质的多样性山西省运城市康杰中学2017-2018学年高一下学期期中考试化学试题新疆自治区和田地区和田县喀什塔什乡中学2019届高三年级四月调研考试理综化学试题百所名校联考-必修二模块综合检测黑龙江省哈尔滨市尚志市尚志中学2021届高三10月月考化学试题(已下线)第8单元 原子结构 元素周期律(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷海南省华中师范大学海南附属中学2021届高三上学期第四次月考化学试题河南省新野县第一高级中学校2021-2022学年高一下学期第三次考试化学试题四川省成都市树德中学2021-2022学年高一下学期5月阶段性测试化学试题
名校
解题方法
5 . 下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
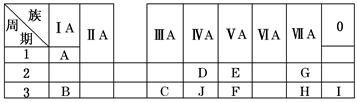
(1)表中元素,化学性质最不活泼的是________ ,只有负价而无正价的元素是________ 。
(2)C元素在元素周期表中的位置是第三周期第________ 族。
(3)最高价氧化物的水化物酸性最强的是________ ,呈两性的是________ 。
(4)A分别与E、G、H形成的化合物中,最稳定的是________ 。
(5)在B、C、E、F中,原子半径最大的是________ 。
(6)B、H两种元素所形成的化合物所含的化学键类型为________________ 。
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:__________________________ 。
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:________________________________________________________________________ 。

(1)表中元素,化学性质最不活泼的是
(2)C元素在元素周期表中的位置是第三周期第
(3)最高价氧化物的水化物酸性最强的是
(4)A分别与E、G、H形成的化合物中,最稳定的是
(5)在B、C、E、F中,原子半径最大的是
(6)B、H两种元素所形成的化合物所含的化学键类型为
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:
您最近一年使用:0次
2018-02-11更新
|
1887次组卷
|
5卷引用:北京市人大附中2017-2018学年下学期高一第一次月考 化学试卷
名校
6 . A、B、C、D、E为短周期元素,原子序数依次增大,有关信息如下:
(1)A、B组成的某种化合物和A的某种氢化物反应可生成A的单质,则A、B组成的该化合物所含有的化学键的类型为(填序号)_______ 。
①离子键 ②极性键 ③非极性键
(2)C的氧化物与B的最高价氧化物对应水化物反应的离子方程式是_______ 。
(3)E的单质制漂白粉的化学方程式是_______ 。
(4)0.2mol化合物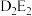 与水反应,其中一种产物为
与水反应,其中一种产物为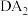 ,过程中转移电子数目为
,过程中转移电子数目为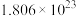 ,且只有一种元素化合价发生变化,该反应的化学方程式为
,且只有一种元素化合价发生变化,该反应的化学方程式为_______ 。
| 元素 | 有关信息 |
| A | 最外层电子数是电子层数的3倍 |
| B | M层有1个电子,单质须保存在煤油中 |
| C | 地壳中含量最多的金属元素 |
| D | 与A形成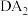 和 和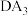 两种化合物 两种化合物 |
| E | 单质可用于生产漂白液、漂白粉 |
①离子键 ②极性键 ③非极性键
(2)C的氧化物与B的最高价氧化物对应水化物反应的离子方程式是
(3)E的单质制漂白粉的化学方程式是
(4)0.2mol化合物
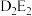 与水反应,其中一种产物为
与水反应,其中一种产物为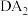 ,过程中转移电子数目为
,过程中转移电子数目为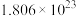 ,且只有一种元素化合价发生变化,该反应的化学方程式为
,且只有一种元素化合价发生变化,该反应的化学方程式为
您最近一年使用:0次
解题方法
7 . 元素周期表在学习、研究和生产实践中有很重要的作用。下表显示了元素周期表中的短周期,①〜⑤代表5种元素。
(1)②在元素周期表中的位置是_______ 。
(2)①分别与④、⑤形成的化合物中,稳定性强的是_______ (用化学式表示)。
(3)③和④分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是_______ 。
(4)③能与⑤形成AB型化合物,用原子结构解释原因:_______ 。
(5)元素Se的原子结构示意图为 。下列推断正确的是
。下列推断正确的是_______ (填序号)。
a.Se位于第4周期、与④同主族
b.Se的最低负化合价为-2价
c.SeO2具有还原性
d.H2SeO3的酸性强于H2SO4
| ① | |||||||
| ② | |||||||
| ③ | ④ | ⑤ |
(2)①分别与④、⑤形成的化合物中,稳定性强的是
(3)③和④分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是
(4)③能与⑤形成AB型化合物,用原子结构解释原因:
(5)元素Se的原子结构示意图为
 。下列推断正确的是
。下列推断正确的是a.Se位于第4周期、与④同主族
b.Se的最低负化合价为-2价
c.SeO2具有还原性
d.H2SeO3的酸性强于H2SO4
您最近一年使用:0次
2021-01-24更新
|
237次组卷
|
2卷引用:北京市东城区2020-2021学年高一上学期期末考试化学试题
解题方法
8 . 下图是元素周期表的一部分,根据① ~ ⑨在周期表中的位置按题目要求回答:
(1)在元素①~⑨中,金属性最强的元素是______ (填元素符号 )。
(2)画出元素④的原子结构示意图______ 。
(3)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,写出甲物质的电子式_____ 。
(4)元素③④⑤对应的最高价氧化物的水化物,写出它们相互之间能发生反应化学方程式__________________ 。
(5)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程_______ 。
(6)②与⑥形成两种氢化物中,稳定性较高的是______ (填化学式),请从原子结构的角度解释其原因:__________ 。
族 周期 | IA | 0 | ||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
4 | ⑧ | ⑨ | ||||||
(1)在元素①~⑨中,金属性最强的元素是
(2)画出元素④的原子结构示意图
(3)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,写出甲物质的电子式
(4)元素③④⑤对应的最高价氧化物的水化物,写出它们相互之间能发生反应化学方程式
(5)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程
(6)②与⑥形成两种氢化物中,稳定性较高的是
您最近一年使用:0次
2020-04-16更新
|
311次组卷
|
2卷引用:北京市密云区2019-2020学年高一上学期期末考试化学试题
9 . 元素周期表与元素周期律在学习、研究中有很重要的作用。下表是元素周期表中5种元素的相关信息,其中Q、W、X位于同一周期。
(1)Q的元素符号是___________ 。
(2)Q、W的最高价氧化物对应的水化物中,酸性较强的物质是___________
(3)金属性Y强于X,用原子结构解释原因:___________ ,失电子能力Y大于X。
(4)下列对于Z及其化合物的推断中,正确的是___________ (填序号)。
①Z的最低负化合价与W的最低负化合价相同
②Z的氢化物的稳定性弱于W的氢化物的稳定性
③Z的单质可与X和W形成的化合物的水溶液发生置换反应
| 元素 | 信息 |
| Q | 在元素周期表中位于第3周期、第ⅣA族 |
| W | 最高正化合价为+7价 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色反应为紫色 |
| Z | 原子结构示意图为 |
(2)Q、W的最高价氧化物对应的水化物中,酸性较强的物质是
(3)金属性Y强于X,用原子结构解释原因:
(4)下列对于Z及其化合物的推断中,正确的是
①Z的最低负化合价与W的最低负化合价相同
②Z的氢化物的稳定性弱于W的氢化物的稳定性
③Z的单质可与X和W形成的化合物的水溶液发生置换反应
您最近一年使用:0次
名校
10 . 元素周期律、表是我们研究、预测物质性质的重要工具。
I.新版化学元素周期表中113号、115号、117号、118号等新发现元素的英文及中文命名均已确定,七个周期已全部填满。
(1)第7周期元素在结构上的共同点是____ 。
(2)113号元素位于周期表第IIIA族,其最外层电子数是___ ,写出第3周期IIIA族元素的元素符号____ 。
II.如图为部分元素周期表示意图,根据该图回答问题:
(3)X最高价氧化物的电子式是____ 。
(4)Y的最高价氧化物对应的水化物的化学式是____ 。
(5)用电子式表示氯化钠的形成过程_____ 。
(6)Ga(镓)在周期表中的位置____ ,预测氢氧化镓是两性氢氧化物,已知:氢氧化镓难溶于水,请写出氢氧化镓与氢氧化钠溶液反应的离子方程式____ 。
I.新版化学元素周期表中113号、115号、117号、118号等新发现元素的英文及中文命名均已确定,七个周期已全部填满。
(1)第7周期元素在结构上的共同点是
(2)113号元素位于周期表第IIIA族,其最外层电子数是
II.如图为部分元素周期表示意图,根据该图回答问题:
| X | ||||
| Y | Cl | |||
| Ga | 锗 | Br | ||
| I |
(4)Y的最高价氧化物对应的水化物的化学式是
(5)用电子式表示氯化钠的形成过程
(6)Ga(镓)在周期表中的位置
您最近一年使用:0次



