名校
解题方法
1 . W、X、Y、Z、Q为原子序数依次增大的5种短周期元素,W的阴离子与锂离子具有相同电子层结构,X的气态氢化物可与其最高价含氧酸反应生成离子化合物,X、Y、Z的最高价氧化物对应水化物之间两两反应均可生成盐和水,Q的最高价氧化物对应的的水化物为最强含氧酸。下列说法错误的是
| A.W、Y均可以与氧原子形成1:1、1:2型化合物 |
| B.Y、Z、Q的简单离子半径大小关系:Q> Y >Z |
| C.Q元素单质具有强氧化性、漂白性 |
| D.X的氢化物稳定性比它同周期右边主族元素的氢化物稳定性差 |
您最近一年使用:0次
名校
解题方法
2 . 现有X、Y、Z三种属于元素周期表前18种的元素,X的单质可以在Z的单质中燃烧,生成XZ,燃烧时火焰为苍白色;X的单质也可以与Y的单质化合,生成常温下为液体的X2Y;Z的单质溶于X2Y中,生成一种含X、Y、Z三种元素的物质,具有强氧化性,可用于自来水的消毒。根据以上信息,完成下列问题:
(1)画出Z的原子结构示意图___ 。
(2)将XZ的水溶液滴入NaHCO3溶液中,有气泡产生,反应的离子方程式为___ 。
(3)实验室可用X、Y两种元素组成的另外一种化合物来制备Y的单质,试写出该反应的化学方程式___ ;若生成11.2L(标准状况)的Y的单质,则转移的电子的物质的量为___ 。
(4)试写出Z的单质溶于X2Y中反应的离子方程式___ 。
(5)XYZ在光照条件下不稳定,原因是___ (用化学方程式表示)。
(6)由Y与Z组成的化合物ZY2,已成为一种新型自来水消毒剂。从物质的分类角度分析,化合物ZY2属于___ 。
(1)画出Z的原子结构示意图
(2)将XZ的水溶液滴入NaHCO3溶液中,有气泡产生,反应的离子方程式为
(3)实验室可用X、Y两种元素组成的另外一种化合物来制备Y的单质,试写出该反应的化学方程式
(4)试写出Z的单质溶于X2Y中反应的离子方程式
(5)XYZ在光照条件下不稳定,原因是
(6)由Y与Z组成的化合物ZY2,已成为一种新型自来水消毒剂。从物质的分类角度分析,化合物ZY2属于
您最近一年使用:0次
解题方法
3 . 短周期主族元素X、Y、Z、W的原子序数依次增大,最外层电子数之和为17,其中X元素形成的单质在自然界中的硬度最大,Z元素的金属性在短周期元素中最强,W单质的水溶液具有酸性和漂白性。下列说法不正确的是
A.原子半径: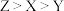 |
| B.Y的最简单气态氢化物的水溶液呈碱性 |
| C.H(氢)、Y、W三种元素形成的化合物中只含有共价键 |
| D.X的最高价氧化物与Z的最高价氧化物能化合生成盐 |
您最近一年使用:0次
名校
4 . X、Y、Z、M、Q五种短周期元素,原子序数依次增大,Y元素的最高正价为+4价,Y元素与Z、M元素相邻,且与M元素同主族;化合物Z2X4的电子总数为18个,Q元素的原子最外层电子数比次外层少一个电子。下列说法不正确的是
| A.原子半径: Y<Z<M |
| B.最高价氧化物对应水化物的酸性: Z>Y>M |
| C.X2Z−ZX2易溶于水,其水溶液呈碱性 |
| D.X的非金属性强于Z |
您最近一年使用:0次
解题方法
5 . 现有部分短周期元素的性质或原子结构如表:
(1)元素X的一种同位元素可测定文物年代,这种同位素的符号是________ (用元素符号表示),元素Z的离子结构元素图为________________ 。
(2)元素Y与氢元素形成一离子YH ,则检验溶液中存在该离子的方法是
,则检验溶液中存在该离子的方法是____________ 。
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的方程式:__________ 。
(4)元素X与元素Y相比,非金属性较强的是________ (用元素符号表示)。下列表述中能证明这一事实的是________ 。
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(5)探寻物质的性质差异性是化学学习的重要方法之一。X、Y、Z 3种元素的单质中化学性质明显不同于其他两种单质的是__________ (用元素符号表示),理由是_____________ 。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
(2)元素Y与氢元素形成一离子YH
 ,则检验溶液中存在该离子的方法是
,则检验溶液中存在该离子的方法是(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的方程式:
(4)元素X与元素Y相比,非金属性较强的是
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(5)探寻物质的性质差异性是化学学习的重要方法之一。X、Y、Z 3种元素的单质中化学性质明显不同于其他两种单质的是
您最近一年使用:0次
2020-11-02更新
|
138次组卷
|
2卷引用:湖南省长沙县第九中学2019-2020学年高一上学期第一次月考化学试题
解题方法
6 . A、B、C、D四种短周期元素的原子序数依次增大,A的一种核素在考古时常用来鉴定一些文物的年代,B的气态氢化物的水溶液呈碱性;C为金属元素且有两种常见含氧化合物(都含两种元素);若往D单质的水溶液中滴加少量紫色石蕊溶液,可观察到先变红后褪色。下列说法中正确的是
| A.原子半径:D>A>B>C |
| B.简单氢化物的稳定性:A>B |
| C.最高价氧化物对应的水化物的酸性:B>D |
| D.C的两种含氧化合物中阴、阳离子个数比都为1:2 |
您最近一年使用:0次
名校
7 . 现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数是电子层数的2倍;Y与Z能形成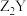 、
、 型离子化合物,Z与T形成的
型离子化合物,Z与T形成的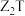 化合物能破坏水的电离平衡。五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
化合物能破坏水的电离平衡。五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是

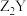 、
、 型离子化合物,Z与T形成的
型离子化合物,Z与T形成的 化合物能破坏水的电离平衡。五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
化合物能破坏水的电离平衡。五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
A.原子半径和离子半径均满足: |
B.简单的气态氢化物的沸点和稳定性排序均为: |
C.最高价氧化物对应的水化物的酸性: |
| D.由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性 |
您最近一年使用:0次
名校
解题方法
8 . 现有8种短周期元素的性质,数据如下表所列:
回答下列问题:
(1)③的元素符号是______ ,⑧的元素名称是________ ,①在元素周期表中的位置 是______ 。
(2)在这 8 种元素中,最高价氧化物对应的水化物中,酸性最强的化合物其分子式是______ ;碱性最强的化合物电子式是_________ ,它属于_________ 化合物(填 “离子”或“共价”)。
(3)比较④和⑦的氢化物的稳定性强弱___________ (用化学式表示)。
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:________ 。
(5)写出单质③在单质①中燃烧的化学方程式__________ 。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径 (10-10 m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)③的元素符号是
(2)在这 8 种元素中,最高价氧化物对应的水化物中,酸性最强的化合物其分子式是
(3)比较④和⑦的氢化物的稳定性强弱
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:
(5)写出单质③在单质①中燃烧的化学方程式
您最近一年使用:0次
名校
解题方法
9 . 元素周期表的形式多种多样,如图是扇形元素周期表的一部分,对比中学常见元素周期表,思考扇形元素周期表的填充规律,回答下列问题:
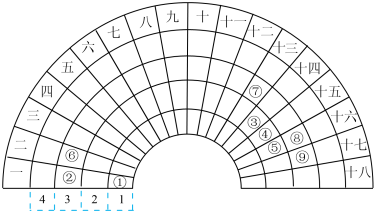
(1)元素④在“标准”长式周期表中的位置______________
(2)元素⑤的原子结构示意图__________________
(3)元素②⑤⑧形成的简单离子半径由小到大的顺序是_________ (用化学用语作答)
(4)在最高价氧化物的水化物中,酸性最强的化合物的名称是__________ ,碱性最强的化合物的电子式是__________
(5)元素①和元素⑨形成的化合物是由__________ 形成的(填“极性键”“非极性键”),该化合物属于__________ 化合物(填“离子”或“共价”),是__________ (填“强电解质”或“弱电解质”)。

(1)元素④在“标准”长式周期表中的位置
(2)元素⑤的原子结构示意图
(3)元素②⑤⑧形成的简单离子半径由小到大的顺序是
(4)在最高价氧化物的水化物中,酸性最强的化合物的名称是
(5)元素①和元素⑨形成的化合物是由
您最近一年使用:0次
名校
解题方法
10 . W、X、Y、Z为短周期原子序数依次增大的主族元素,其中W元素形成的单质密度最小,且W与X、Y、Z都能形成共价化合物,Y、W形成的常见化合物溶于水显碱性,Z、W形成的化合物溶于水显酸性。四种元素原子序数之和为30,可形成的某种化合物结构式为 。下列说法正确的是
。下列说法正确的是
| A.该化合物中所有原子均满足8电子稳定结构 |
| B.X和Z的最高价氧化物的水化物都是一元强酸 |
| C.简单氢化物的沸点:Y>Z |
| D.W与Y、Z三种元素形成的化合物中一定不含离子键 |
您最近一年使用:0次
2020-09-22更新
|
401次组卷
|
3卷引用:广东省广州市执信、广雅、六中三校2021届高三上学期8月联考化学试题



