名校
解题方法
1 . 部分短周期主族元素的原子半径和主要化合价的关系如图所示,其中E、G、T位于同一周期。回答下列问题:

(1)B位于第_______ 周期第______ 族。
(2)FDB的电子式为_______ ;T的原子结构示意图为_______ 。
(3)设计简单实验证明D的非金属性比C的强:________ 。
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是_______ 。
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同),碱性最强的是_______ ;上述非金属元素的简单氢化物中,沸点最高的是_______ ,还原性最强的是_______ 。
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为_______ 。

(1)B位于第
(2)FDB的电子式为
(3)设计简单实验证明D的非金属性比C的强:
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为
您最近一年使用:0次
2023-10-27更新
|
171次组卷
|
2卷引用:湖南省炎德·英才·名校联考联合体2023-2024学年高三上学期第三次联考化学试题
名校
2 . 2019年是元素周期表诞生150周年,元素周期表在学习、研究和生产实践中有很重要的作用。已知 、
、 、
、 、
、 是中学常见的四种元素.原子序数依次增大。
是中学常见的四种元素.原子序数依次增大。 的原子最外层电子数是次外层的2倍。
的原子最外层电子数是次外层的2倍。 的氧化物属于两性氧化物,
的氧化物属于两性氧化物, 、
、 位于同周期,
位于同周期, 、
、 、
、 的原子最外层电子数之和为14,
的原子最外层电子数之和为14, 是人体必需的微量元素,缺乏
是人体必需的微量元素,缺乏 会导致贫血症状。
会导致贫血症状。
(1)硒是人体必需的微量元素。人体内产生的活性氧能加速人体衰老,被称为“生命杀手”。化学家尝试用 及其他富硒物质清除人体内的活性氧,此时
及其他富硒物质清除人体内的活性氧,此时 表现出
表现出_______ 性。
(2)下列事实能用元素周期律解释的是_______ (填序号)。
a. 的最高价氧化物对应水化物的碱性弱于
的最高价氧化物对应水化物的碱性弱于
b. 的气态氢化物的稳定性小于
的气态氢化物的稳定性小于
c. 的溶液可用于刻蚀铜制的印刷电路板
的溶液可用于刻蚀铜制的印刷电路板
(3) 的单质可用于处理酸性废水中的
的单质可用于处理酸性废水中的 ,使其转换为
,使其转换为 ,同时生成有磁性的
,同时生成有磁性的 的氧化物
的氧化物 ,再进行后续处理。
,再进行后续处理。
①上述反应的离子方程式为_______ 。
② 的单质与
的单质与 在高温下反应的化学方程式为
在高温下反应的化学方程式为_______ 。
(4)铅和 元素同主族,可发生反应
元素同主族,可发生反应 。请写出草酸的电子式:
。请写出草酸的电子式:_______ 。 与
与 性质相似,
性质相似, 与氢氧化钠溶液反应的离子方程式是
与氢氧化钠溶液反应的离子方程式是_______ 。
(5)金属镓有“电子工业脊梁”的美誉,它与 同主族,其氧化物和氢氧化物均为两性化合物。工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含
同主族,其氧化物和氢氧化物均为两性化合物。工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含 、
、 、
、 杂质,以
杂质,以 水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:
水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为: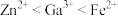 )下列有关电解精炼镓的说法正确的是_______(填序号)。
)下列有关电解精炼镓的说法正确的是_______(填序号)。
 、
、 、
、 、
、 是中学常见的四种元素.原子序数依次增大。
是中学常见的四种元素.原子序数依次增大。 的原子最外层电子数是次外层的2倍。
的原子最外层电子数是次外层的2倍。 的氧化物属于两性氧化物,
的氧化物属于两性氧化物, 、
、 位于同周期,
位于同周期, 、
、 、
、 的原子最外层电子数之和为14,
的原子最外层电子数之和为14, 是人体必需的微量元素,缺乏
是人体必需的微量元素,缺乏 会导致贫血症状。
会导致贫血症状。(1)硒是人体必需的微量元素。人体内产生的活性氧能加速人体衰老,被称为“生命杀手”。化学家尝试用
 及其他富硒物质清除人体内的活性氧,此时
及其他富硒物质清除人体内的活性氧,此时 表现出
表现出(2)下列事实能用元素周期律解释的是
a.
 的最高价氧化物对应水化物的碱性弱于
的最高价氧化物对应水化物的碱性弱于
b.
 的气态氢化物的稳定性小于
的气态氢化物的稳定性小于
c.
 的溶液可用于刻蚀铜制的印刷电路板
的溶液可用于刻蚀铜制的印刷电路板(3)
 的单质可用于处理酸性废水中的
的单质可用于处理酸性废水中的 ,使其转换为
,使其转换为 ,同时生成有磁性的
,同时生成有磁性的 的氧化物
的氧化物 ,再进行后续处理。
,再进行后续处理。①上述反应的离子方程式为
②
 的单质与
的单质与 在高温下反应的化学方程式为
在高温下反应的化学方程式为(4)铅和
 元素同主族,可发生反应
元素同主族,可发生反应 。请写出草酸的电子式:
。请写出草酸的电子式: 与
与 性质相似,
性质相似, 与氢氧化钠溶液反应的离子方程式是
与氢氧化钠溶液反应的离子方程式是(5)金属镓有“电子工业脊梁”的美誉,它与
 同主族,其氧化物和氢氧化物均为两性化合物。工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含
同主族,其氧化物和氢氧化物均为两性化合物。工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含 、
、 、
、 杂质,以
杂质,以 水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:
水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为: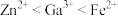 )下列有关电解精炼镓的说法正确的是_______(填序号)。
)下列有关电解精炼镓的说法正确的是_______(填序号)。A.阳极发生氧化反应,其主要电极反应式: |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
C.在阴极除了析出高纯度的镓之外,还可能有 产生 产生 |
D.电解后,电解槽底部的阳极泥中只有 和 和 |
您最近一年使用:0次
名校
解题方法
3 . 短周期元素 X、Y、Z、W 的原子序数依次增加。Y 的简单氢化物常温下呈液态,X 的简单氢化物溶于水,溶液显碱性,Z 是短周期中还原性最强的元素,W 元素的最高价氧 化物的对应水化物是短周期中酸性最强的无机含氧酸。下列说法正确的是
| A.原子半径:W<Z<Y |
| B.X 形成的含氧酸一定是强酸 |
| C.Z 的单质与 CuSO4 溶液反应,可置换出 Cu |
| D.W 元素可形成具有消毒作用的化合物 |
您最近一年使用:0次
2020-12-21更新
|
226次组卷
|
2卷引用:山西省运城市夏县第二中学2021届高三上学期11月联考化学试题
名校
4 . W、X、Y、Z 为原子序数依次增大的短周期元素, W 和 Y同族, X 和Z 同族, X 的简单离子和 Y 的简单离子具有相同的电子层结构, W 和 X、Z 能分别形成分子式为 XW3、 ZW3 的共价化合物,这两种共价化合物溶于水均呈碱性。下列说法不正确的是
| A.四种元素中Y 的金属性最强 |
| B.最高价氧化物对应水化物的酸性: Z > X |
| C.简单阳离子的氧化性: W>Y |
| D.化合物 YW 与水反应能生成还原性气体 |
您最近一年使用:0次
2020-07-03更新
|
195次组卷
|
3卷引用:四川省成都市第七中学家2019-2020学年高一下学期6月考试化学试题
名校
解题方法
5 . X、Y、Z、W是不同周期的四种主族元素,原子序数依次递增。其中X与W同主族,与Y能形成两种液态化合物P、Q,P分解时吸热、Q分解时放热。Y、W的最外层电子之和等于Z的最外层电子。下列说法中正确的是
| A.P具有强还原性,Q具有强氧化性 |
B.元素的非金属性强弱顺序为: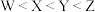 |
| C.W单质在空气中燃烧只生成碱性氧化物 |
| D.电解Z与W形成的化合物的溶液,可制得Z单质 |
您最近一年使用:0次
6 . X、Y为第三周期元素、Y最高正价与最低负价的代数和为6,二者形成的一种化合物能以[XY4]+[XY6]-的形式存在。下列说法错误的是
| A.原子半径:X>Y | B.简单氢化物的还原性:X>Y |
| C.同周期元素形成的单质中Y氧化性最强 | D.同周期中第一电离能小于X的元素有4种 |
您最近一年使用:0次
2021-06-29更新
|
13050次组卷
|
35卷引用:2021年新高考山东化学高考真题
2021年新高考山东化学高考真题(已下线)课时25 原子结构-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第36讲 原子结构与性质(精练)-2022年一轮复习讲练测(已下线)专题06 物质结构 元素周期律-备战2022年高考化学真题及地市好题专项集训【山东专用】江苏省如皋中学2021-2022学年高三上学期第一次阶段考试化学试题辽宁省渤海大学附属高级中学2021-2022学年高三上学期第二次月考化学试题辽宁省沈阳市第一二〇中学2021-2022学年高二上学期期中考试化学试题2021年湖北高考化学试题变式题11-192021年山东高考化学试题变式题1-10福建省福州第三中学2021-2022学年高三上学期第五次质量检测化学试题(已下线)查补易混易错点06 物质结构 元素周期律-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷06题 元素周期表元素周期律-备战2022年高考化学临考题号押题(新高考通版)浙江省温州新力量联盟2021-2022学年高二下学期期末联考化学试题(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第14讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(新教材新高考)北京市清华大学附属中学2022-2023学年高三9月月考化学试题四川省遂宁市射洪中学2022-2023学年高二上学期第一次月考(10月)化学试题湖南省长沙市卓华高级中学2021-2022学年高二下学期期末考试化学试题四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题四川省遂宁中学校2022-2023学年高二上学期期中考试化学试题山东省济宁市邹城市孟子湖中学2021-2022学年高三下学期开学考试化学试题(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破天津市第四十七中学2022—2023学年高三上学期期末 阶段性学习检测化学试题天津市第四十七中学2022-2023学年高三上学期期末考试化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第五章 物质结构与性质 元素周期律 第27讲 元素周期表和元素周期律湖北省武汉市洪山高级中学2022-2023学年高二下学期2月考试化学试题安徽省安庆市第一中学2022-2023学年高二下学期第一次月考化学试题黑龙江省哈尔滨市第三中学2022-2023学年高二下学期第一次验收考试化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题1-5)(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
名校
7 . 短周期主族元素W、X、Y、Z的原子半径依次增大。M、N、P是由这些元素组成的二元化合物,r、s、q是其中三种元素对应的单质,M与r均为淡黄色固体,W、X、Y位于不同周期。上述物质转化关系如图所示(部分生成物省略),下列说法错误的是
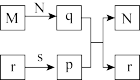

| A.物质熔沸点:N>P |
| B.X、Y可形成离子化合物 |
| C.单质氧化性:X>W |
| D.X、Y、Z三种元素组成的盐溶液可能呈中性或碱性 |
您最近一年使用:0次
2022-05-06更新
|
1492次组卷
|
5卷引用:广东省汕头市2022届普通高中毕业班第二次模拟试化学试题
广东省汕头市2022届普通高中毕业班第二次模拟试化学试题(已下线)2022年全国乙卷高考变式题(选择题)(已下线)微专题31 元素推断的破解-备战2023年高考化学一轮复习考点微专题福建省莆田第二十五中学2022-2023学年高三上学期期中考试化学试题学科特色5 元素“位–构–性”推断
解题方法
8 . 下列有关金属元素特征的叙述正确的是( )
| A.金属元素的原子只有还原性,离子只有氧化性 |
| B.金属元素在一般化合物中只显正价 |
| C.金属元素在不同的化合物中的化合价均不同 |
| D.金属元素的单质在常温下均为金属晶体 |
您最近一年使用:0次
2020-01-08更新
|
218次组卷
|
2卷引用:云南省耿马县民族中学2019-2020学年高二12月月考化学试题
名校
9 . 下列有关金属元素性质的叙述中正确的是
| A.金属元素的原子只有还原性,离子只有氧化性 |
| B.金属元素在化合物中一定显正化合价 |
| C.金属元素在自然界中全部以化合态存在 |
| D.金属元素的单质在常温下均为固体 |
您最近一年使用:0次
2016-12-28更新
|
109次组卷
|
2卷引用:2016-2017学年河北冀州中学高一12月月考文化学卷
名校
10 . 前四周期元素X、Y、Z、W核电荷数依次增大,核电荷数之和为58;Y原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2。
(1)写出Z元素在元素周期表中的位置:___________ 。
(2) 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是___________  写分子式
写分子式 。
。
(3) 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为___________ ;
(4) 单质
单质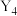 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为___________ ;
(5)含W元素的最高化合价的含氧酸根离子是___________ ,该含氧酸根离子在分析化学中有重要作用,在酸性条件下该含氧酸根离子可将 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式___________ 。
(1)写出Z元素在元素周期表中的位置:
(2)
 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是 写分子式
写分子式 。
。(3)
 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为(4)
 单质
单质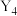 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为(5)含W元素的最高化合价的含氧酸根离子是
 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
2021-04-21更新
|
553次组卷
|
5卷引用:2015-2016学年重庆市第八中学高二下第三次月考化学试卷



