名校
1 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y最外层电子数是K层的3倍,Z与Y同主族。下列说法正确的是
| A.原子半径:X<Y<Z<W |
| B.X、Y可形成一种红棕色气体 |
| C.Z的简单气态氢化物的热稳定性比W的强 |
| D.X、Z、W形成的氧化物均为酸性氧化物 |
您最近一年使用:0次
2023-07-13更新
|
140次组卷
|
3卷引用:黑龙江省哈尔滨市2022-2023学年高一下学期学业质量检测化学试题
名校
2 . 如表为部分元素的特点
请回答下列问题:
(1)若火灾现场存放大量Y,需要用______ 灭火;化合物Y2X2中存在的化学键类型为______ 。
(2)向含+3价L离子的溶液中滴加KI溶液,再滴入淀粉溶液,溶液呈______ 色,说明还原性有:L2+______ I-(填“>”或“<”);
(3)混合物甲由两种常见化合物组成,每种化合物含X、Y、Z、Q四种元素中的至少三种元素,在向甲中逐滴滴加盐酸的过程中,产生的QX2气体的物质的量与滴加的盐酸体积关系如图所示:
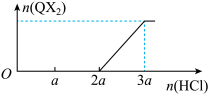
由此可知,混合物甲的组成为______ (填化学式),两者的物质的量之比为______ 。
(4)使用下列装置再添加合适的药品,可以证明R和Q两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸 ②稀硫酸 ③盐酸 ④Na2CO3固体 ⑤CaCO3⑥澄清石灰水 ⑦NaOH溶液
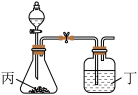
请选择装置丙、丁两处应该加入的药品代号:丙______ 、丁______ 。
| 特点 | 元素代号 |
| 地壳中含量最高的元素 | X |
| +1价阳离子L层充满电子 | Y |
| 原子半径最小的原子 | Z |
| 一种同位素可以用于考古 | Q |
| 与上述代号为Z的元素形成分子Z2R,其摩尔质量为34g/mol | R |
| 其合金用量最大,用途最广 | L |
(1)若火灾现场存放大量Y,需要用
(2)向含+3价L离子的溶液中滴加KI溶液,再滴入淀粉溶液,溶液呈
(3)混合物甲由两种常见化合物组成,每种化合物含X、Y、Z、Q四种元素中的至少三种元素,在向甲中逐滴滴加盐酸的过程中,产生的QX2气体的物质的量与滴加的盐酸体积关系如图所示:

由此可知,混合物甲的组成为
(4)使用下列装置再添加合适的药品,可以证明R和Q两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸 ②稀硫酸 ③盐酸 ④Na2CO3固体 ⑤CaCO3⑥澄清石灰水 ⑦NaOH溶液

请选择装置丙、丁两处应该加入的药品代号:丙
您最近一年使用:0次
2023-03-09更新
|
269次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2023-2024学年高一下学期开学化学试题
名校
3 . 某种净水剂由原子序数依次增大的R、W、X、Y、Z五种主族元素组成。五种元素分处三个短周期,且包含地壳中含量前三的三种元素。五种元素原子的最外层电子数之和为20。下列说法正确的是
A.简单离子半径: |
B.最简单氢化物的稳定性: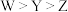 |
| C.R分别与W、Z形成的三原子分子均为V形分子 |
D.常见单质的熔点: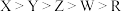 |
您最近一年使用:0次
4 . X、Y、Z、W四种短周期主族元素,原子序数依次递增,X原子中有3个能量相等且自旋方向相同的电子,Y是地壳中含量最多的元素,Y与W同主族,Z在短周期主族元素中金属性最强。回答下列问题:
(1)X、Y、Z、W四种元素的原子半径从大到小的顺序为_______ (填元素符号)。
(2)元素Y的原子轨道表示式为_______ 。
(3)元素X与元素Y的简单气态氢化物中,稳定性较强的是_______ (填电子式)。
(4)Z原子的结构示意图为_______ 。
(5)W元素在元素周期表中的位置为_______ ,其价电子排布式为_______ 。
(1)X、Y、Z、W四种元素的原子半径从大到小的顺序为
(2)元素Y的原子轨道表示式为
(3)元素X与元素Y的简单气态氢化物中,稳定性较强的是
(4)Z原子的结构示意图为
(5)W元素在元素周期表中的位置为
您最近一年使用:0次
名校
5 . A、B、C、D、E、F六种元素均位于元素周期表的前四周期,且原子序数依次增大。元素A是原子半径最小的元素;B元素基态原子的核外电子占据四个原子轨道:D元素原子的成对电子总数是未成对电子总数的3倍;E与D位于同一主族;F位于第VIII族,在地壳中含量排金属中第二位。
(1) 的价电子排布图为
的价电子排布图为___________ 。
(2)B、C、D的某些氢化物的分子中都含有18个电子,B的这种氢化物的中心原子杂化方式为___________ ,等物质的量B、C、D的这种氢化物的分子中含有 键的个数之比为
键的个数之比为___________ 。
(3)D常见的两种单质D2和D3,其中___________ (填化学式)在水中的溶解度更大。
(4)D、E可形成分子式为ED3的化合物,其空间构型为___________ 。
(5)实验室合成一种由B和C两种元素形成的化合物,该化合物具有三维骨架结构,其中每个B原子与4个C原子形成共价键,每个C原子与3个B原子形成共价键。其化学式为___________ ,预测该化合物熔点___________ 金刚石(填“高于”或“低于”)。
(1)
 的价电子排布图为
的价电子排布图为(2)B、C、D的某些氢化物的分子中都含有18个电子,B的这种氢化物的中心原子杂化方式为
 键的个数之比为
键的个数之比为(3)D常见的两种单质D2和D3,其中
(4)D、E可形成分子式为ED3的化合物,其空间构型为
(5)实验室合成一种由B和C两种元素形成的化合物,该化合物具有三维骨架结构,其中每个B原子与4个C原子形成共价键,每个C原子与3个B原子形成共价键。其化学式为
您最近一年使用:0次
名校
解题方法
6 . X、Y、Z、W、Q为前四周期元素,原子序数依次增大。X元素核外L层只有一个空轨道;Y元素的L层有三个未成对电子;Z的单质是常温下为黄色固体,难溶于水,易溶于CS2;W元素是人体中含量最多的金属元素;Q元素M层全满且N层只有1个电子。
(1)写出基态W原子的电子排布式_______ 。
(2)Q元素位于第_______ 周期第_______ 族。
(3)WXY2是离子化合物,各原子均满足8电子稳定结构,WXY2的电子式是_______ ,W、X、Y三种元素的电负性由大到小顺序是_______ (写元素符号)。
(4)图(a)为Z单质分子的结构,其分子式为_______ ,Z原子的杂化方式为_______ 。

①其单质难溶于水,易溶于CS2的原因为_______ 。
②其熔沸点要比SO2的熔沸点高很多,主要原因为_______ 。
(5)WX2俗称电石,与水反应可以生成强碱以及一直线形有机物,写出该反应的化学方程式_______ 。
(6)Q与镍元素合金的立方晶胞结构如图所示。

①在该晶胞中镍原子与Q原子的数量比为_______ 。
②若该晶胞的棱长为anm,ρ=_______ gcm-3(NA表示阿伏加德罗常数,列出计算式)
(1)写出基态W原子的电子排布式
(2)Q元素位于第
(3)WXY2是离子化合物,各原子均满足8电子稳定结构,WXY2的电子式是
(4)图(a)为Z单质分子的结构,其分子式为

①其单质难溶于水,易溶于CS2的原因为
②其熔沸点要比SO2的熔沸点高很多,主要原因为
(5)WX2俗称电石,与水反应可以生成强碱以及一直线形有机物,写出该反应的化学方程式
(6)Q与镍元素合金的立方晶胞结构如图所示。

①在该晶胞中镍原子与Q原子的数量比为
②若该晶胞的棱长为anm,ρ=
您最近一年使用:0次
7 . 现有A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大。A与C形成的化合物能使湿润的红色石蕊试纸变蓝;D是地壳中含量最多的元素;D、F原子的最外层电子数相等;E的焰色反应呈黄色;B元素的一种同位素在考古时可用于测定一些文物的年代。请回答下列问题:(注意回答问题时均用元素符号表示)
(1)元素B在周期表中的位置:___________ 。
(2)元素A与C组成的10电子的阳离子的电子式:___________ 。元素A与D组成的18电子分子的结构式:___________ 。
(3) 和
和 形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:
形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:___________ 。
(4)D和F的简单气态氢化物沸点比较高的是:___________ (写分子式),原因:______ 。
(5)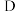 、
、 、
、 、G的简单离子半径由小到大的顺序为
、G的简单离子半径由小到大的顺序为___________ (用离子符号表示)。
(6)用电子式表示化合物E2D的形成过程:___________ 。
(1)元素B在周期表中的位置:
(2)元素A与C组成的10电子的阳离子的电子式:
(3)
 和
和 形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:
形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:(4)D和F的简单气态氢化物沸点比较高的是:
(5)
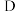 、
、 、
、 、G的简单离子半径由小到大的顺序为
、G的简单离子半径由小到大的顺序为(6)用电子式表示化合物E2D的形成过程:
您最近一年使用:0次
名校
8 . X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)___________ 。
(2)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A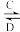 B(在水溶液中进行)其中,C是CO2;D是淡黄色固体。写出D的电子式:
B(在水溶液中进行)其中,C是CO2;D是淡黄色固体。写出D的电子式:___________ 。
①如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式为___________ 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:___________ 。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是___________ ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有___________ 。
(1)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)
(2)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
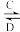 B(在水溶液中进行)其中,C是CO2;D是淡黄色固体。写出D的电子式:
B(在水溶液中进行)其中,C是CO2;D是淡黄色固体。写出D的电子式:①如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式为
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:
您最近一年使用:0次
2021-12-09更新
|
347次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2021-2022学年高三上学期期中考试化学试题
9 . 短周期主族元素X、Y、Z、W的原子半径依次增大。X、Y位于同一主族,Z在第三周期中离子半径最小,Z和W的原子序数之和是X的原子序数的4倍。下列说法错误的是
| A.最简单气态氢化物的热稳定性:X>Y |
| B.YX属于共价化合物 |
| C.含Z元素的盐溶液可能显碱性,也可能显酸性 |
| D.Y为地壳中含量最多的非金属元素 |
您最近一年使用:0次
2021-12-23更新
|
397次组卷
|
6卷引用:黑龙江省大庆市2021-2022学年高三上学期第二次教学质量检测理科综合化学试题
解题方法
10 . .短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)E2D2的电子式:___ 。
(2)B与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为___ ,Q与水反应的化学方程式为___ 。
(3)A,C,D,E的原子半径由大到小的顺序是___ (用元素符号表示)。
(4)元素B和F的非金属性强弱,B的非金属性___ 于F(填“强”或“弱”),并用化学方程式证明上述结论___ 。
(1)E2D2的电子式:
(2)B与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为
(3)A,C,D,E的原子半径由大到小的顺序是
(4)元素B和F的非金属性强弱,B的非金属性
您最近一年使用:0次



