解题方法
1 . 下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是: (填具体元素符号或化学式,下同),非金属性最强的元素是: 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:_______,碱性最强的化合物的化学式是:_____________。
(3)最高价氧化物是两性氧化物的元素是:_________;写出它的最高价氧化物与氢氧化钠反应的离子方程式:____________________________________。
(4)④与⑧形成的化合物的电子式是: ,该化合物所含化学键类型是: (填“共价键”或“离子键”)。
(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:_______,碱性最强的化合物的化学式是:_____________。
(3)最高价氧化物是两性氧化物的元素是:_________;写出它的最高价氧化物与氢氧化钠反应的离子方程式:____________________________________。
(4)④与⑧形成的化合物的电子式是: ,该化合物所含化学键类型是: (填“共价键”或“离子键”)。
(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 实验步骤 | 实验现象与结论 |
您最近一年使用:0次
10-11高一下·山东德州·期中
解题方法
2 . 已知A、B、C、D、E是短周期的5种元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出B、D元素的名称:B______________ ,D______________ 。
(2)画出C元素的离子结构示意图_____________________________ 。
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式_________ 。
(4)A、B、C三种元素形成的化合物为_____________________ , 所含的化学键类型为_______________________ 。
(5)B、C、D三种元素的离子半径由大到小的排列顺序为__________________ (用离子符号表示)。
(1)请写出B、D元素的名称:B
(2)画出C元素的离子结构示意图
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式
(4)A、B、C三种元素形成的化合物为
(5)B、C、D三种元素的离子半径由大到小的排列顺序为
您最近一年使用:0次
2016-12-09更新
|
1095次组卷
|
5卷引用:2010—2011学年山东省德州一中高一下学期期中考试化学试卷
(已下线)2010—2011学年山东省德州一中高一下学期期中考试化学试卷(已下线)2011-2012学年广东省罗定市高一下学期期中质检理综化学试卷2015-2016学年福建省清流一中高一下期中理科化学试卷四川省自贡市田家炳中学2019-2020学年高一下学期期中考试化学试题四川省自贡市田家炳中学2020-2021学年高一下学期期中考试化学试题
10-11高二下·安徽滁州·阶段练习
解题方法
3 . 有V、W、X、Y、Z五种元素,它们是核电荷数依次增大的前四周期元素;X、Z是金属元素;V和X元素原子的最外层电子都只有一个;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;Z是一种常见金属元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。由此可知:
(1)X在元素周期表中的位置是_______ ,Z的元素符号是_______
(2)V-W和V—Y属于极性共价键,其中极性较强的键是_______ (V、W、Y用元素符号表示)。
(3)w与X形成原子个数之比为1:1的化合物的电子式为_______
(4)工业上冶炼Z单质的化学方程式为_______
(1)X在元素周期表中的位置是
(2)V-W和V—Y属于极性共价键,其中极性较强的键是
(3)w与X形成原子个数之比为1:1的化合物的电子式为
(4)工业上冶炼Z单质的化学方程式为
您最近一年使用:0次
10-11高二下·黑龙江·期中
解题方法
4 . 已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z、W四种元素的符号:X_______ 、Y_______ 、Z_______ 、W_______
(2)X与Y所形成的化合物的化学式为_______ ,是_______ 化合物。用电子式表示其形成过程_______ 。
(1)X、Y、Z、W四种元素的符号:X
(2)X与Y所形成的化合物的化学式为
您最近一年使用:0次
10-11高一下·吉林·开学考试
解题方法
5 . 短周期元素X、Y、Z组成的化合物Y2X和ZX2 ,Y2X溶于水形成的水溶液能与ZX2反应生成一种化合物Y2ZX3,已知三种元素原子的电子总数为25,且Z与Y的原子序数之和比X的原子序数的2倍还多1,Z原子的最外层电子数是次外层电子数的2倍。试回答:
①X、Y、Z元素名称及符号:X_______ Y_______ Z_______
②写出ZX2的化学式_______
③Y2X对应水化物的电子式为_______ ,其中存在的化学键有_______ ,_______ 。④用电子式表示Y2X的形成过程:_______ 。
①X、Y、Z元素名称及符号:X
②写出ZX2的化学式
③Y2X对应水化物的电子式为
您最近一年使用:0次
10-11高一下·湖北黄冈·阶段练习
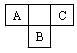
6 . A、B、C均为短周期元素,在元素周期表中的相对位置如下图所示,A、C两种元素的原子核外电子数之和等于B原子的核电荷数。请完成下列填空:
(1)A的原子结构示意图为__________________ ,A的最高价氧化物对应水化物的的分子式为_______________________ 。
(2)B的简单离子的电子式为_____________________ 。
(3)用电子式表示C的氢化物分子的形成过程:
__________________________________________________________ 。
(4)C单质与水反应的化学方程式为_____________________________________ 。

(1)A的原子结构示意图为
(2)B的简单离子的电子式为
(3)用电子式表示C的氢化物分子的形成过程:
(4)C单质与水反应的化学方程式为
您最近一年使用:0次
9-10高二下·吉林延边·期末
解题方法
7 . A、B、C均为短周期元素,可形成A2C和BC2两种化合物。A、B、C的原子序数依次递增,A原子的K层的电子数只有一个,B原子2p能级有一个空轨道,而C原子M 层只有两对电子对。
(1)它们的元素符号分别为:A________ ;B________ ;C_________ ;
(2)用电子式表示A2C的形成过程__________________________________ ;
(3)BC2是由______ 键组成的________ (填“极性”或“非极性”)分子;BC2分子中B原子采用______ 杂化类型。
(1)它们的元素符号分别为:A
(2)用电子式表示A2C的形成过程
(3)BC2是由
您最近一年使用:0次
9-10高一下·山东德州·期末
8 . 有A、B、C、D、E5种元素,已知:
①A原子最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子第三层上的电子比第一层多5个。
②常温下B2是气体,相同条件下,它的密度是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。D在DB2中的含量为50%。根据以上情况回答:
(1)D是____________ ,其在周期表中的位置为______________ 。
(2)E的原子结构示意图为____________ ,C的离子结构示意图为___________ 。
(3)F和AB2反应的化学方程式为________________________________________ 。
(4)F中含有的化学键为__________________ 。
①A原子最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子第三层上的电子比第一层多5个。
②常温下B2是气体,相同条件下,它的密度是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。D在DB2中的含量为50%。根据以上情况回答:
(1)D是
(2)E的原子结构示意图为
(3)F和AB2反应的化学方程式为
(4)F中含有的化学键为
您最近一年使用:0次
9-10高一下·河南·期中
解题方法
9 . 下表为元素周期表的一部分,表中列出11种元素在周期表中的位置,按要求回答下列各题。

 (1)这11种元素中,化学性质最不活泼的元素是 (用元素符号或化学式表示,下同),得电子能力最强的原子对应的单质是 ,失电子能力最强的原子对应的单质与水反应的化学方程式是 。常温下为液态的非金属单质是 。
(1)这11种元素中,化学性质最不活泼的元素是 (用元素符号或化学式表示,下同),得电子能力最强的原子对应的单质是 ,失电子能力最强的原子对应的单质与水反应的化学方程式是 。常温下为液态的非金属单质是 。
(2)元素④的离子结构示意图为 。
(3)⑥、⑦、⑧气态氢化物的化学式分别为 、 、 ,其中以 最稳定。⑦、⑨两种元素最高价氧化物对应水化物的化学式分别为: 、 ;其中以 酸性最强。
(4)③和⑨两种元素形成的化合物属于 (填“离子化合物”或“共价化合物”),请用电子式表示其形成过程 。
(5)写出③的单质置换出⑥的单质的化学方程式 。

| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
| 4 | ② | ④ | 11 |
 (1)这11种元素中,化学性质最不活泼的元素是 (用元素符号或化学式表示,下同),得电子能力最强的原子对应的单质是 ,失电子能力最强的原子对应的单质与水反应的化学方程式是 。常温下为液态的非金属单质是 。
(1)这11种元素中,化学性质最不活泼的元素是 (用元素符号或化学式表示,下同),得电子能力最强的原子对应的单质是 ,失电子能力最强的原子对应的单质与水反应的化学方程式是 。常温下为液态的非金属单质是 。(2)元素④的离子结构示意图为 。
(3)⑥、⑦、⑧气态氢化物的化学式分别为 、 、 ,其中以 最稳定。⑦、⑨两种元素最高价氧化物对应水化物的化学式分别为: 、 ;其中以 酸性最强。
(4)③和⑨两种元素形成的化合物属于 (填“离子化合物”或“共价化合物”),请用电子式表示其形成过程 。
(5)写出③的单质置换出⑥的单质的化学方程式 。
您最近一年使用:0次



