名校
解题方法
1 . 孔雀石是一种碳酸盐矿物,主要成分为Cu2(OH)2CO3,其形成过程的主要化学方程式为2CuSO4+2CaCO3+H2O= Cu2(OH)2CO3+2CaSO4+CO2↑。NA是阿伏加德罗常数的值,下列说法正确的是
| A.0.1mol/L的CuSO4溶液中所含Cu2+的数目小于0.1NA |
| B.常温常压下,18gH2O中所含共用电子对的数目为2NA |
C.1molCaCO3晶体中所含 的数目小于NA 的数目小于NA |
| D.44gCO2溶于水所得溶液中所含H2CO3分子的数目为NA |
您最近一年使用:0次
名校
解题方法
2 . 价类二维图是学习化学的一种有效归纳方法,关于下图中所涉及物质的说法或推断错误的是
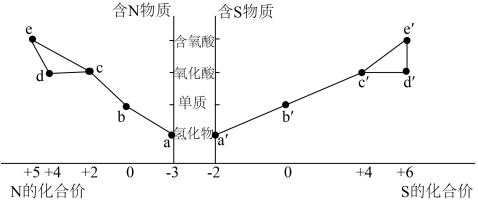
A.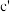 是一种常用的食品添加剂,应合理使用 是一种常用的食品添加剂,应合理使用 |
| B.物质a、c、d全属于非电解质 |
C.液态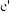 比较粘稠,是因为分子间有氢键 比较粘稠,是因为分子间有氢键 |
| D.a和e反应得到的白色固体中只有极性键 |
您最近一年使用:0次
2024-04-05更新
|
210次组卷
|
2卷引用:湖北省云学名校联盟2023-2024学年高二下学期3月联考化学试卷
名校
3 . 1869年门捷列夫提出元素周期表,根据元素周期表和周期律,回答问题。
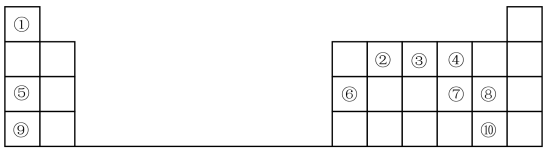
(1)元素⑦在周期表中的位置_______ 。
(2)元素①和⑤形成的化合物中化学键类型是_______ 。
(3)在①~⑧元素中,原子半径最大的是_______ (填元素名称);其某种氧化物可用于潜水艇中的供氧剂,该氧化物中阴离子与阳离子个数比为_______ 。
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是_______ (用离子符号表示),元素⑨的最高价氧化物对应水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(5)元素的非金属性⑩_______ ⑧(填“>”或“<”);下列事实不能证明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的氢化物的还原性比元素⑩的弱
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
E.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
(6)⑤的最高价氧化物对应的水化物的电子式为_______ ,用电子式表示氯化钠的形成过程_______ 。

(1)元素⑦在周期表中的位置
(2)元素①和⑤形成的化合物中化学键类型是
(3)在①~⑧元素中,原子半径最大的是
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是
(5)元素的非金属性⑩
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的氢化物的还原性比元素⑩的弱
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
E.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
(6)⑤的最高价氧化物对应的水化物的电子式为
您最近一年使用:0次
名校
4 . A、B、C、D、E、F、G为短周期元素,原子序数依次增大。A、B两元素最高正价和最低负价代数和为零;D是地壳中含量最高的非金属元素;E和A同主族,G与D同主族;E、F、G的最高价氧化物的水化物两两之间可以反应。
(1)G元素的名称是__________ ,其在周期表中的位置是_____________ ,其离子结构示意图为_____________ 。
(2) 的电子式
的电子式_____________ ;由A、C原子个数比为5∶1组成的一种化合物,其中各原子均达到稳定结构,该化合物中所含化学键类型为_____________ 。
(3)B、C形成的最高价氧化物的水化物,酸性由强到弱的顺序为_____________ (用分子式表示,下同);D和G的简单氢化物沸点的由高到低的顺序为_____________ 。
(4)E和F分别对应的最高价氧化物的水化物相互反应的离子方程式________________ 。
(5)由C、E组成的一种离子化合物的化学式为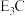 ,该化合物中两种离子的半径由大到小的顺序是(用离子符号表示)
,该化合物中两种离子的半径由大到小的顺序是(用离子符号表示)_________________________ ;该化合物遇水剧烈反应,有刺激性气味的气体生成,该反应的化学方程式为___________________________ 。
(1)G元素的名称是
(2)
 的电子式
的电子式(3)B、C形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(4)E和F分别对应的最高价氧化物的水化物相互反应的离子方程式
(5)由C、E组成的一种离子化合物的化学式为
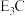 ,该化合物中两种离子的半径由大到小的顺序是(用离子符号表示)
,该化合物中两种离子的半径由大到小的顺序是(用离子符号表示)
您最近一年使用:0次
5 . 下列各组物质中既含有离子键又含有共价键的是
| A.NaOH、H2O、NH4Cl | B.KOH、Na2O2、(NH4)2SO4 |
| C.MgO、CaBr2、NaCl | D.Na2SO4、HCl、MgCl2 |
您最近一年使用:0次
2024-04-03更新
|
304次组卷
|
2卷引用:新疆阿克苏市实验中学2022-2023学年高一下学期第一次月考化学试题
6 . 化学助力蓝天保卫战。工业上可利用氨水吸收SO2尾气,生成NH4HSO3,再将其氧化得到(NH4)2SO4化肥。设NA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4LNH3所含的分子数目为NA |
| B.64gSO2中所含的σ键数目为2NA |
C.2mol 完全氧化生成 完全氧化生成 ,转移的电子数目为2NA ,转移的电子数目为2NA |
D.1L0.1mol/L(NH4)2SO4溶液中所含的 数目为0.2NA 数目为0.2NA |
您最近一年使用:0次
7 . 下列各物质的晶体中,化学键类型完全相同,晶体类型也相同的是
| A.SiF4与SiC | B.HCOOCH3与NH4NO3 |
| C.CaO与Na2O2 | D.NF3与CS2 |
您最近一年使用:0次
名校
8 . 尿素 和氰酸铵(
和氰酸铵( )互为同分异构体,下列说法正确的是
)互为同分异构体,下列说法正确的是
 和氰酸铵(
和氰酸铵( )互为同分异构体,下列说法正确的是
)互为同分异构体,下列说法正确的是| A.二者均可发生氧化反应 |
| B.二者均仅含极性共价键 |
| C.可通过质谱法初步判断氰酸铵中具有哪些基因 |
| D.在核磁共振氢谱中,尿素分子中存在两种处于不同化学环境的氢原子 |
您最近一年使用:0次
2024-04-02更新
|
110次组卷
|
2卷引用:河北省保定市清苑中学等校2023-2024学年高二下学期3月月考化学试题
9 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.含0.4molHCl的盐酸与足量MnO2加热反应生成氯气,转移电子数为0.2NA |
| B.标准状况下,2.24LH2O中含有H-O数目为0.2NA |
| C.0.1mol·L-1的Na2CO3溶液中阴离子数目一定小于0.1NA |
| D.常温下1LpH=2的硫酸溶液中H+的数目为0.01NA |
您最近一年使用:0次
名校
解题方法
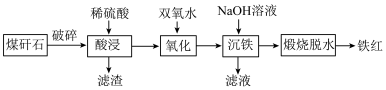
10 . 由煤矸石(主要成分为 及铁铝的氧化物,还含有少量
及铁铝的氧化物,还含有少量 )制备铁红的工艺流程如图,下列说法错误的是
)制备铁红的工艺流程如图,下列说法错误的是
 及铁铝的氧化物,还含有少量
及铁铝的氧化物,还含有少量 )制备铁红的工艺流程如图,下列说法错误的是
)制备铁红的工艺流程如图,下列说法错误的是
| A.使用硝酸酸浸会产生污染环境的气体 |
B.氧化过程的反应为 |
C. 溶液中存在的化学键有离子键、共价键、氢键 溶液中存在的化学键有离子键、共价键、氢键 |
| D.煅烧氢氧化铁前,需洗去表面吸附的杂质 |
您最近一年使用:0次
2024-04-01更新
|
333次组卷
|
2卷引用:辽宁省锦州市渤海大学附属高级中学2023-2024学年高三下学期3月摸底考试化学试题



