1 . 下列只含共价键的化合物是
| A.HClO4 | B.NaCl | C.KOH | D.MgCl2 |
您最近半年使用:0次
2 . 几种氧化物的化学键中离子键成分的百分数如下表所示:
根据表格信息,可推知:前四周期元素组成的离子晶体中,离子键成分的百分数最高的是
氧化物 |
|
|
|
|
离子键成分的百分数/ | 62 | 50 | 41 | 33 |
A.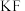 | B. | C. | D. |
您最近半年使用:0次
名校
解题方法
3 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。
(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
(2)第三周期元素的原子中,未成对电子不可能有_______。
(3)基态F原子的轨道表示式为_______ ,四氟乙烯的电子式为_______ 。
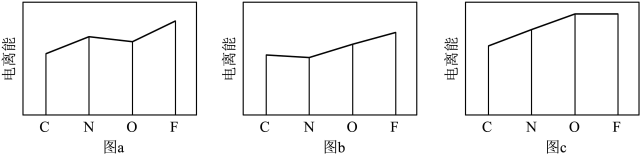
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填字母),第三电离能的变化图是_______ (填字母)。
(5) 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为_______ 和_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(6)比较甲醚和乙醇的沸点高低,并说明理由_______ 。
 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
| A.原子与原子之间 | B.分子与分子之间 | C.离子与离子之间 | D.离子与电子之间 |
(2)第三周期元素的原子中,未成对电子不可能有_______。
| A.4个 | B.3个 | C.2个 | D.1个 |
(3)基态F原子的轨道表示式为
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(5)
 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为(6)比较甲醚和乙醇的沸点高低,并说明理由
您最近半年使用:0次
4 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.含0.4molHCl的盐酸与足量MnO2加热反应生成氯气,转移电子数为0.2NA |
| B.标准状况下,2.24LH2O中含有H-O数目为0.2NA |
| C.0.1mol·L-1的Na2CO3溶液中阴离子数目一定小于0.1NA |
| D.常温下1LpH=2的硫酸溶液中H+的数目为0.01NA |
您最近半年使用:0次
名校
5 . 无机物可根据其组成和性质进行分类。现有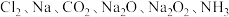 六种物质,完成下列填空:
六种物质,完成下列填空:
(1)由分子构成的单质是
(2)既有离子键又有共价键的物质的电子式为
(3)上述化合物中组成元素的原子半径由大到小的顺序是
(4)
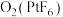 是离子化合物,其中
是离子化合物,其中 为
为 价。正确判断是___________。
价。正确判断是___________。| A.常温下为固体 | B.不存在共价键 | C.属于极性分子 | D.由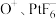 构成 构成 |
您最近半年使用:0次
解题方法
6 . 下列物质中只含有离子键的是
| A.CO2 | B.KCl | C.NaOH | D.CH4 |
您最近半年使用:0次
名校
7 . 如图所示为元素周期表的一部分,其中X、Y、Z、W为四种短周期元素。Z元素原子核外K层与M层上的电子数相等。下列说法中正确的是
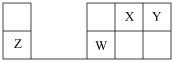

A.Y元素的最高价氧化物对应的水化物的化学式为 |
B.最高价氧化物对应水化物的酸性: |
C.原子半径由小到大的顺序为 |
| D.X、Z两种元素的氧化物中所含化学键的类型相同 |
您最近半年使用:0次
名校
解题方法
8 . 下列物质中既含有离子键又含有共价键的是
| A.NH3·H2O | B.CH3COONa | C.CO2 | D.MgCl2 |
您最近半年使用:0次
名校
9 . 下列分子的结构式、化学键类型、空间构型的说法均正确的有
| 分子化学式 | 结构式 | 化学键类型 | 空间构型 | |
| A | HClO | H—Cl—O | 极性键 | 直线形 |
| B | CO2 | O=C=O | 极性键 | 直线形 |
| C | H2O | H—O—H | 非极性键 | 直线形 |
| D | CH4 | H—H—C—H—H | 非极性键 | 正方形 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
10 . 下列说法正确的有
| A.硫酸氢钠晶体加热至熔融态破坏了离子键 |
| B.干冰升华破坏了共价键 |
| C.冰融化破坏了氢键和离子键 |
| D.氯化氢溶于水破坏了离子键 |
您最近半年使用:0次








