名校
1 . Z、Y、X、W、Q为五种原子序数依次增大的短周期主族元素。其中Z、Y、W分别位于三个不同周期,Y、Q位于同一主族,Y原子的最外层电子数是W原子的最外层电子数的2倍,Y、X、W三种简单离子的核外电子排布相同。由Z、Y、X、W形成的某种化合物的结构如图所示。下列说法不正确 的是
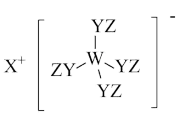
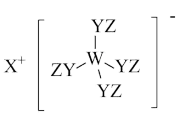
A.简单氢化物的稳定性: |
B.该物质中所有原子均满足最外层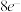 的稳定结构 的稳定结构 |
| C.X与Y、Y与Z均可形成含非极性共价键的化合物 |
| D.W与X两者的最高价氧化物对应的水化物之间可发生反应 |
您最近半年使用:0次
2022-01-25更新
|
842次组卷
|
8卷引用:浙江省宁波市九校2021-2022学年高一上学期期末联考化学试题
名校
解题方法
2 . X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的s电子数比p电子数多3个,Y、Z间形成的某种化合物是一种常用的漂白剂、供氧剂,R和Z位于同一周期且基态原子中有3个电子能量最高,M2+与过量氨水作用先得到蓝色沉淀,后转化为深蓝色溶液Q。请回答下列问题:
(1)基态M2+的核外电子排布式为__ ,Y、Z、R、M四种元素的第一电离能由大到小的顺序为__ (用元素符号表示)。
(2)化合物XCl3的中心原子的杂化类型为__ ,RCl3的立体构型为__ ,XCl3、RCl3分子中属于非极性分子的是__ ;导致Q溶液显色的粒子中存在的化学键类型有__ 与配位键。
(3)已知H2Y2的熔点为-0.43℃、沸点为158℃,RH3的熔点为-133℃、沸点为-87.7℃,但H2Y2、RH3的相对分子质量相同,其主要原因是__ 。
(4)X、R两元素可形成一种具体立体网状结构的化合物,其晶胞结构如图所示。

①该化合物的晶体类型是__ ,该晶体的化学式为___ 。
②设两个X原子最近距离为apm,列式计算该晶胞的密度ρ=__ g·cm-3。
(1)基态M2+的核外电子排布式为
(2)化合物XCl3的中心原子的杂化类型为
(3)已知H2Y2的熔点为-0.43℃、沸点为158℃,RH3的熔点为-133℃、沸点为-87.7℃,但H2Y2、RH3的相对分子质量相同,其主要原因是
(4)X、R两元素可形成一种具体立体网状结构的化合物,其晶胞结构如图所示。

①该化合物的晶体类型是
②设两个X原子最近距离为apm,列式计算该晶胞的密度ρ=
您最近半年使用:0次
11-12高二下·四川成都·阶段练习
解题方法
3 . A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物;B与Z的最外层电子数之比为2︰3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。请回答下列问题。
(1)X在周期表中的位置是_______
(2)化合物Y2X2的电子式为_______ ;它含有的化学键类型有 _______
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成Z的化学方程式为_______ 。
(4)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为_______ 。
(5)写出化合物Y2X2与水反应的离子方程式_______ 。
(6)B的最高价氧化物的结构式为_______ 。
(1)X在周期表中的位置是
(2)化合物Y2X2的电子式为
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成Z的化学方程式为
(4)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为
(5)写出化合物Y2X2与水反应的离子方程式
(6)B的最高价氧化物的结构式为
您最近半年使用:0次
名校
解题方法
4 . A、B、C、X是中学化学常见的物质,A、B、C均由短周期元素组成,转化关系如图。
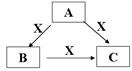
请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,向C的水溶液中通入过量的CO2可得B的白色胶状沉淀。
①A中含有的金属元素为_________ (写元素名称),它在周期表中的位置为_____________ 。
②写出B → C反应的离子方程式为___________________________________ 。
(2)若A为稀HNO3,X为常见黑色金属单质,写出A→B反应的离子方程式__________ 。
(3)若A、B、C三种化合物的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生。
①A中所含有的化学键是________________
②自然界中存在B、C和H2O按一定比例结晶而成的固体,取一定量该固体溶于水配成一定物质的量浓度的溶液100mL,所用到的玻璃仪器有玻璃棒、烧杯、________ 、_________ 。
③若测得上述溶液中金属阳离子的浓度为0.5mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为____________ g 。

请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,向C的水溶液中通入过量的CO2可得B的白色胶状沉淀。
①A中含有的金属元素为
②写出B → C反应的离子方程式为
(2)若A为稀HNO3,X为常见黑色金属单质,写出A→B反应的离子方程式
(3)若A、B、C三种化合物的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生。
①A中所含有的化学键是
②自然界中存在B、C和H2O按一定比例结晶而成的固体,取一定量该固体溶于水配成一定物质的量浓度的溶液100mL,所用到的玻璃仪器有玻璃棒、烧杯、
③若测得上述溶液中金属阳离子的浓度为0.5mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为
您最近半年使用:0次
名校
解题方法
5 . A、B、C、D、E五种主族元素的原子序数依次增大,且均小于18,A原子的最外层电子比B原子的最外层电子少2个,B原子的质子数是其电子层数的4倍。A、B、C三种元素能结合成化合物C2AB3,在lmolC2AB3中共有52mol电子。D元素的单质0.5mol与酸全部反应时,有9.03×1023个电子转移。E元素的单质是一种黄绿色气体,水溶液具有漂白性。试填写下列空白:
(1)写出元素A 和E的名称:A_______ ,E_______ 。
(2)元素B在周期表中的位置为第二周期_______ 族。
(3)由元素B、C形成的一种化合物可以作为呼吸面具的供氧剂,该化合物为含有_______ 键(填“极性”或“非极性”)的_______ 化合物(填“离子”或“共价”) ,写出该化合物的电子式_______ 。
(4)写出C、D两种元素对应的最高价氧化物的水化物相互反应的离子方程式_______ 。
(1)写出元素A 和E的名称:A
(2)元素B在周期表中的位置为第二周期
(3)由元素B、C形成的一种化合物可以作为呼吸面具的供氧剂,该化合物为含有
(4)写出C、D两种元素对应的最高价氧化物的水化物相互反应的离子方程式
您最近半年使用:0次
2016-12-09更新
|
595次组卷
|
4卷引用:2015-2016学年江苏省泰州中学高一下第一次月考化学试卷
2015-2016学年江苏省泰州中学高一下第一次月考化学试卷2016-2017学年湖南省株洲市第二中学高一下学期第一次月考化学试卷《课时同步君》2017-2018学年高一化学人教必修2-1.3 化学键(已下线)精做03 化学键——《大题精做》2017-2018学年高一化学人教必修2



