名校
1 . 几种氧化物的化学键中离子键成分的百分数如下表所示:
根据表格信息,可推知:前四周期元素组成的离子晶体中,离子键成分的百分数最高的是
氧化物 |
|
|
|
|
离子键成分的百分数/ | 62 | 50 | 41 | 33 |
A.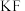 | B. | C. | D. |
您最近一年使用:0次
2024-04-21更新
|
245次组卷
|
3卷引用:江西省赣州市上进联考2023-2024学年高二下学期3月第一次阶段性考试化学试题
名校
解题方法
2 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。
(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
(2)第三周期元素的原子中,未成对电子不可能有_______。
(3)基态F原子的轨道表示式为_______ ,四氟乙烯的电子式为_______ 。
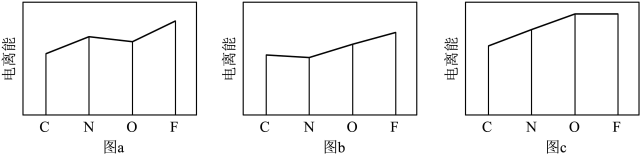
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填字母),第三电离能的变化图是_______ (填字母)。
(5) 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为_______ 和_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(6)比较甲醚和乙醇的沸点高低,并说明理由_______ 。
 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
| A.原子与原子之间 | B.分子与分子之间 | C.离子与离子之间 | D.离子与电子之间 |
(2)第三周期元素的原子中,未成对电子不可能有_______。
| A.4个 | B.3个 | C.2个 | D.1个 |
(3)基态F原子的轨道表示式为
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(5)
 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为(6)比较甲醚和乙醇的沸点高低,并说明理由
您最近一年使用:0次
3 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.含0.4molHCl的盐酸与足量MnO2加热反应生成氯气,转移电子数为0.2NA |
| B.标准状况下,2.24LH2O中含有H-O数目为0.2NA |
| C.0.1mol·L-1的Na2CO3溶液中阴离子数目一定小于0.1NA |
| D.常温下1LpH=2的硫酸溶液中H+的数目为0.01NA |
您最近一年使用:0次
解题方法
4 . 下列物质中只含有离子键的是
| A.CO2 | B.KCl | C.NaOH | D.CH4 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法不正确的是
| A.离子化合物和金属单质的构成粒子中均含有阳离子 |
| B.离子键和金属健本质上都是静电作用,都没有方向性和饱和性 |
| C.熔点:MgO>NaCl>Hg>HBr |
| D.NaHSO4在水溶液中和熔融状态下都能导电,电离方程式相同 |
您最近一年使用:0次
2023-12-30更新
|
227次组卷
|
3卷引用:北京市第一○一中学2021-2022学年高二下学期期末考试化学试卷
6 . 反应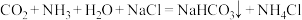 应用于侯氏制碱。下列说法正确的是
应用于侯氏制碱。下列说法正确的是
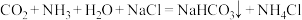 应用于侯氏制碱。下列说法正确的是
应用于侯氏制碱。下列说法正确的是A. 的电子式为: 的电子式为: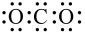 |
B. 中含有离子键和共价键 中含有离子键和共价键 |
C. 易液化是由于 易液化是由于 与 与 分子之间存在氢键 分子之间存在氢键 |
D. 的电离方程式为 的电离方程式为 |
您最近一年使用:0次
2023-12-14更新
|
256次组卷
|
2卷引用:江苏省南通市2023-2024学年高二上学期期中考试化学试题
7 . 下列各过程中需要破坏化学键的是
| A.氯化钠熔化 | B.液溴挥发 | C.碘单质升华 | D.冰融化 |
您最近一年使用:0次
解题方法
8 . 下列关于共价键的说法正确的是
| A.键能是衡量化学键强度的物理量 |
| B.键长是指形成共价键的两个原子之间的间距 |
| C.两个原子形成共价键时,原子轨道重叠程度越大,键能越大 |
| D.单键一般比双键的键能更大 |
您最近一年使用:0次
解题方法
9 . 判断化学键的类型。
(1)一般来说,如果两种成键元素的电负性差值大于1.7,它们之间通常形成__________ 。
(2)一般来说,如果两种成键元素的电负性差值小于1.7,它们之间通常形成__________ 。
(1)一般来说,如果两种成键元素的电负性差值大于1.7,它们之间通常形成
(2)一般来说,如果两种成键元素的电负性差值小于1.7,它们之间通常形成
您最近一年使用:0次
10 . 在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是
| A.范德华力、范德华力、范德华力 | B.范德华力、范德华力、共价键 |
| C.范德华力、共价键、共价键 | D.共价键、共价键、共价键 |
您最近一年使用:0次
2023-07-11更新
|
540次组卷
|
51卷引用:2015-2016学年辽宁沈阳市第二中学高二下期末考化学卷
2015-2016学年辽宁沈阳市第二中学高二下期末考化学卷2016-2017学年黑龙江大庆实验中学高二上开学考化学卷(已下线)同步君 选修3 第二章 第三节 范德华力和氢键及其对物质性质的影响2016-2017学年河北省衡水中学高二上学期五调考试化学试卷【全国百强校】宁夏银川唐徕回民中学2017-2018学年高二下学期期中考试化学试题吉林省汪清县第六中学2018-2019学年高二6月月考化学试题四川省武胜烈面中学校2019-2020学年高二下学期期中考试化学试题河南省新乡市辉县市第二高级中学2019-2020学年高二下学期期中考试化学试题新疆喀什地区巴楚县第一中学2020-2021学年高二上学期期中考试化学试题(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第4节 分子间作用力(已下线)第二章 分子结构与性质【过关测试基础卷】-2020-2021学年高二化学单元复习(新教材人教版选择性必修2)黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高二4月月考化学试题黑龙江省鸡西市英桥高级中学2021-2022学年高二下学期期中考试化学试卷山东省泰安市2022-2023学年高二下学期期末考试化学试题广东省云浮市罗定中学2022-2023学年高二下学期第2周周测(分子结构与性质)化学试题(已下线)2.3.2 分子间作用力 分子的手性(巩固)山东省泰安第二中学2023-2024学年高二下学期3月月考化学试题海南省文昌中学2023-2024学年高二下学期第一次月考化学试题广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题山东省日照市五莲中学2023-2024学年高二3月月考化学试题2014年全国普通高等学校招生统一考试理科综合能力测试化学(上海卷)(已下线)2015届北京市重点中学高三上学期第一次月考化学试卷2015届河北省永年县第二中学高三12月月考化学试卷2016届湖南省益阳市箴言中学高三上学期第三次模拟化学试卷2016届上海市徐汇区高三上学期学习能力诊断化学试卷2017届浙江省台州中学高三上统考四化学试卷浙江省2018版考前特训(2017年10月)学考70快练:5 原子、分子中的概念辨析与判断山东省滕州市第一中学2015-2016学年高一4月竞赛化学试题高中化学人教版 选修三 第2章 分子结构与性质 范德华力及其对物质性质的影响(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)(已下线)考点06 原子结构 化学键——备战2019年浙江新高考化学考点上海市浦外教育集团2018-2019学年高三上学期月考化学试题上海市复旦大学附属中学2016-2017学年高一上学期期末考试化学试题2上海市建平中学2019届高三上学期期中考试化学试题上海市市东中学2019-2020学年高三上学期期中考试化学试题辽宁省实验中学东戴河分校2019-2020学年高一上学期12月月考化学试题上海市顾村中学2018-2019学年高三上学期期中考试化学试题上海市民本中学2016-2017学年高三上学期第一次月考化学试题湖北省武汉市钢城第四中学2019-2020高一下学期期中考试化学试题河北省沧州市泊头市第一中学2019-2020学年高一下学期期末考试化学试题(已下线)5.2.2 共价键 分子间作用力练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)专题05 元素周期律(元素框图推断、“位、构、性”、化学键)-2021年高考化学必做热点专题四川省成都市实验外国语学校(西区)2019-2020 学年高一下学期期中考试化学试题(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点08 微粒间相互作用力-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)4.3化学键-同步学习必备知识上海市嘉定区2023届高三一模化学试题(已下线)专题09 原子结构及性质(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型20 物质结构与性质基础-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)








