名校
1 . 冰晶石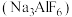 是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是
是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是
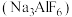 是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是
是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是| A.离子键 | B.配位键 | C. 键 键 | D. 键 键 |
您最近一年使用:0次
2023-05-21更新
|
119次组卷
|
2卷引用:安徽皖北省示范高中2022--2023学年高二下学期5月联考化学试题
2 . 下列描述中错误的是
A.在 晶体中除存在离子键外,还存在共价键和配位键 晶体中除存在离子键外,还存在共价键和配位键 |
B.分子中键角的大小顺序: |
C.杯酚可与 形成超分子,这一过程被称为“分子识别” 形成超分子,这一过程被称为“分子识别” |
D.《中华本草》中记载了炉甘石( )入药, )入药, 中阴离子的空间结构为三角锥形 中阴离子的空间结构为三角锥形 |
您最近一年使用:0次
3 .  和
和 是重要的工业产品,下图为合成氨以及氨氧化制硝酸的流程。
是重要的工业产品,下图为合成氨以及氨氧化制硝酸的流程。

(1)从氨分离器中又回到合成塔中的物质是___________ 。
(2)在催化剂和加热条件下氧化炉中发生反应的化学方程式是___________ ,从氧化炉中出来的气体,先降温再进入吸收塔,吸收塔中通入空气的作用是___________ 。
(3)若要实现 ,从氧化还原反应原理上看,下列试剂可行的是___________。
,从氧化还原反应原理上看,下列试剂可行的是___________。
(4)氮及其化合物在催化剂a和催化剂b作用下发生转化的过程如图所示,下列分析合理的是___________。

 和
和 是重要的工业产品,下图为合成氨以及氨氧化制硝酸的流程。
是重要的工业产品,下图为合成氨以及氨氧化制硝酸的流程。
(1)从氨分离器中又回到合成塔中的物质是
(2)在催化剂和加热条件下氧化炉中发生反应的化学方程式是
(3)若要实现
 ,从氧化还原反应原理上看,下列试剂可行的是___________。
,从氧化还原反应原理上看,下列试剂可行的是___________。A. | B. | C. | D. |

A. 与 与 反应属于氮的固定过程 反应属于氮的固定过程 |
| B.催化剂a表面发生了非极性共价键的断裂和极性共价键的形成 |
| C.在催化剂b表面形成氮氧键时需要吸收能量 |
| D.催化剂a作用下的转化涉及电子转移,催化剂b作用下的转化不涉及电子转移 |
您最近一年使用:0次
4 . 下列说法中不正确的是
A. 晶体溶于水时,离子键被破坏,共价键不受影响 晶体溶于水时,离子键被破坏,共价键不受影响 |
| B.“天宫课堂”中过饱和乙酸钠溶液析晶放热与形成新的化学键有关 |
| C.将熔融状态下的HCl和NaCl进行导电性实验可证明HCl由共价键形成而NaCl由离子键形成 |
| D.H元素与其他元素化合可能形成共价化合物也可能形成离子化合物 |
您最近一年使用:0次
2023-04-27更新
|
193次组卷
|
2卷引用:山东省德州市2022-2023学年高一下学期4月期中考试化学试题
名校
解题方法
5 . 六氟磷酸盐离子液体可用于有机合成的溶剂和催化剂,其结构如图所示,下列说法错误的是
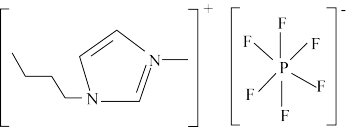

A.阳离子中碳原子有 和 和 两种杂化方式 两种杂化方式 |
| B.阴、阳离子体积较大,离子之间作用力较弱,晶体的熔点较低 |
| C.该物质中存在的化学键类型:离子键、共价键 |
| D.所有原子均符合8电子稳定结构 |
您最近一年使用:0次
2023-04-27更新
|
1148次组卷
|
2卷引用:广东省大湾区2023届普通高中毕业班下学期联合模拟考试(二)化学试题
6 . 汽车已成为现代社会的重要交通工具之一,化学物质在汽车的动力安全等方面有着极为重要的作用。回答下列问题:
I.
(1)某汽车安全气囊的气体发生剂主要含有 、
、 、
、 、
、 等物质。当汽车发生较严重的碰撞时,
等物质。当汽车发生较严重的碰撞时, 分解为Na和
分解为Na和 ,同时释放出大量的热,
,同时释放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
① 是助氧剂,其含有的化学键类型是
是助氧剂,其含有的化学键类型是________________________ 。
② 的作用为
的作用为__________________ 。
③汽车受到猛烈碰撞时,点火器点火引发 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是_______ (填字母)。
A.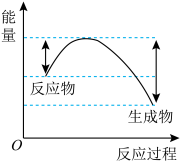 B.
B.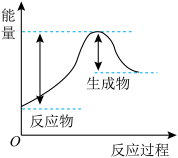 C.
C.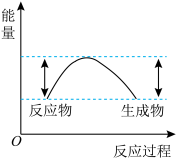
II.汽车尾气主要为 、CO、
、CO、 、NO等物质,是造成城市空气污染主要在因素之一。
、NO等物质,是造成城市空气污染主要在因素之一。
(2)科学家以 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
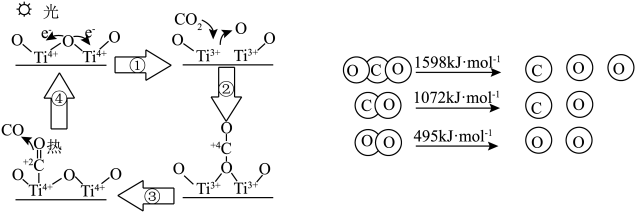
根据数据计算,分解2 mol 需吸收
需吸收_______ kJ的能量。
(3)一定条件下,用CO与NO反应生成 和
和 ,反应的化学方程式:
,反应的化学方程式:
 。
。
为提高该反应的速率,下列措施可行的是_______(填标号)。
(4)为了测定在催化剂作用下, 的反应速率,在某温度下用气体传感器测得不同时间的NO浓度如表:
的反应速率,在某温度下用气体传感器测得不同时间的NO浓度如表:
①前4 s内的平均反应速率
______ 。
②一定温度下,在固定容积的密闭容器中,通入1 mol CO和1 mol NO,在催化剂作用下发生反应。下列能作为反应达到平衡状态的依据的是______ (填序号)。
a.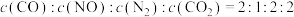
b.单位时间内生成2 mol CO,同时生成1 mol
c.NO的浓度与CO浓度相等
d.容器内总压强不再改变
e.单位时间内断裂1 mol的 键,同时生成2 mol的
键,同时生成2 mol的 键
键
I.
(1)某汽车安全气囊的气体发生剂主要含有
 、
、 、
、 、
、 等物质。当汽车发生较严重的碰撞时,
等物质。当汽车发生较严重的碰撞时, 分解为Na和
分解为Na和 ,同时释放出大量的热,
,同时释放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。①
 是助氧剂,其含有的化学键类型是
是助氧剂,其含有的化学键类型是②
 的作用为
的作用为③汽车受到猛烈碰撞时,点火器点火引发
 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是A.
 B.
B. C.
C.
II.汽车尾气主要为
 、CO、
、CO、 、NO等物质,是造成城市空气污染主要在因素之一。
、NO等物质,是造成城市空气污染主要在因素之一。(2)科学家以
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
根据数据计算,分解2 mol
 需吸收
需吸收(3)一定条件下,用CO与NO反应生成
 和
和 ,反应的化学方程式:
,反应的化学方程式: 。
。为提高该反应的速率,下列措施可行的是_______(填标号)。
| A.扩大容器体积 | B.升高温度 | C.使用合适催化剂 | D.移出 |
 的反应速率,在某温度下用气体传感器测得不同时间的NO浓度如表:
的反应速率,在某温度下用气体传感器测得不同时间的NO浓度如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 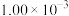 | 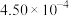 | 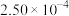 | 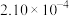 | 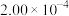 | 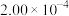 |

②一定温度下,在固定容积的密闭容器中,通入1 mol CO和1 mol NO,在催化剂作用下发生反应。下列能作为反应达到平衡状态的依据的是
a.
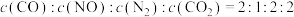
b.单位时间内生成2 mol CO,同时生成1 mol

c.NO的浓度与CO浓度相等
d.容器内总压强不再改变
e.单位时间内断裂1 mol的
 键,同时生成2 mol的
键,同时生成2 mol的 键
键
您最近一年使用:0次
解题方法
7 . 下列说法错误的是
| A.非金属单质中一定不含离子键,一定只含共价键 |
| B.化学键是相邻原子之间的强相互作用 |
| C.酸雨后钢铁易发生析氢腐蚀,日常铁锅存留盐液时易发生吸氧腐蚀 |
| D.电热水器有镁棒防止内胆腐蚀是牺牲阳极保护法 |
您最近一年使用:0次
8 . 化合物“E7974”具有抗肿瘤活性,其结构简式如图所示,下列有关“E7974”的说法错误的是
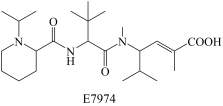

| A.1个“E7974”分子中含有3个N原子 |
| B.所含碳元素的质量分数最大 |
| C.含有化学键的类型为共价键、氢键和范德华力 |
| D.所有碳原子一定不位于同一平面上 |
您最近一年使用:0次
2023-04-24更新
|
139次组卷
|
2卷引用:河南省创新发展联盟2022-2023学年高二下学期第二次联考(期中)化学试题
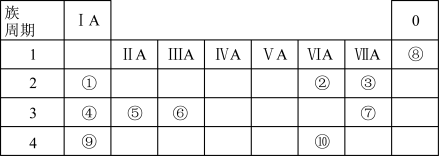
9 . 1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一、元素周期表与元素周期律在化学学习研究中有很重要的作用。下表是元素周期表的一部分,列出了①~⑩10种元素在周期表中的位置。
回答下列问题:
(1)①~⑩元素性质最不活泼的元素是___________ (填元素符号)。
(2)①④⑤⑥中最高价氧化物的水化物碱性最强的是___________ (填化学式),该水化物所含的化学键类型有___________ 。
(3)元素③⑥⑦的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)元素②的简单氢化物的电子式为___________ ,该氢化物常温下和元素④的单质反应的离子方程式是___________ 。
(5)元素⑩[硒(Se)]被誉为“生命元素”,科学补硒可以减少疾病的发生。铜仁市“富硒”耕地丰富,产出的“富硒”农产品受市场青睐,为“黔货出山”和“乡村振兴”作出了重要贡献。下列推断正确的是___________(填字母)。

回答下列问题:
(1)①~⑩元素性质最不活泼的元素是
(2)①④⑤⑥中最高价氧化物的水化物碱性最强的是
(3)元素③⑥⑦的简单离子半径由大到小的顺序是
(4)元素②的简单氢化物的电子式为
(5)元素⑩[硒(Se)]被誉为“生命元素”,科学补硒可以减少疾病的发生。铜仁市“富硒”耕地丰富,产出的“富硒”农产品受市场青睐,为“黔货出山”和“乡村振兴”作出了重要贡献。下列推断正确的是___________(填字母)。
A. 既有氧化性又有还原性 既有氧化性又有还原性 |
B. 的稳定性比 的稳定性比 强 强 |
C. 的酸性强于 的酸性强于 |
D. 在一定条件下可与NaOH溶液反应 在一定条件下可与NaOH溶液反应 |
您最近一年使用:0次
10 . 下列说法正确的是
A. 分子的空间构型是直线型 分子的空间构型是直线型 |
B. 分子中所有原子最外电子层都具有8电子的稳定结构 分子中所有原子最外电子层都具有8电子的稳定结构 |
| C.非极性键不仅存在于双原子的单质分子中,还可能存在于化合物中 |
| D.离子键是阴、阳离子之间通过静电吸引作用形成的 |
您最近一年使用:0次



