1 . 目前,全世界镍(Ni)的消费量仅次于铜、铝、铅、锌,居有色金属第五位,镍行业发展蕴藏着巨大的潜力。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于___________ 晶体;基态Ni原子的电子排布式为___________ 。
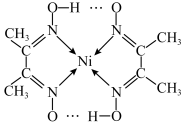
(2)某配合物结构如图所示,分子内含有的作用力有___________ (填编号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键___________ 。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
(2)某配合物结构如图所示,分子内含有的作用力有
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
您最近半年使用:0次
2 . 下列化合物中既存在离子键,又存在极性键的是
| A.H2O | B.NH4Cl | C.Na2O | D.Na2O2 |
您最近半年使用:0次
名校
3 . 下列各组物质中,含有化学键类型都相同的是
| A.HI和NaI | B.NaI和KOH |
| C.CO2和HCl | D.Cl2和NaBr |
您最近半年使用:0次
2024-04-05更新
|
200次组卷
|
2卷引用:江苏省盐城市响水县清源高级中学2023-2024学年高二上学期期中化学试卷(必修)
4 . 完成下列问题
(1)氨气极易溶于水,原因是___________
(2) 的VSEPR理想模型名称为
的VSEPR理想模型名称为___________ ,离子空间结构名称为___________ ,中心原子有___________ 个杂化轨道;
(3) 中存在的化学键类型有
中存在的化学键类型有___________
①离子键 ②极性共价键 ③非极性共价键 ④氢键
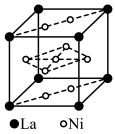
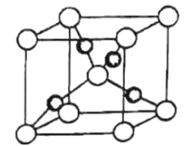
(4)一个 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为___________ 。
(1)氨气极易溶于水,原因是
(2)
 的VSEPR理想模型名称为
的VSEPR理想模型名称为(3)
 中存在的化学键类型有
中存在的化学键类型有①离子键 ②极性共价键 ③非极性共价键 ④氢键
(4)一个
 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为
您最近半年使用:0次
5 . 下列各组物质中既含有离子键又含有共价键的是
| A.NaOH、H2O、NH4Cl | B.KOH、Na2O2、(NH4)2SO4 |
| C.MgO、CaBr2、NaCl | D.Na2SO4、HCl、MgCl2 |
您最近半年使用:0次
2024-04-03更新
|
297次组卷
|
2卷引用:新疆阿克苏市实验中学2022-2023学年高一下学期第一次月考化学试题
6 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.含0.4molHCl的盐酸与足量MnO2加热反应生成氯气,转移电子数为0.2NA |
| B.标准状况下,2.24LH2O中含有H-O数目为0.2NA |
| C.0.1mol·L-1的Na2CO3溶液中阴离子数目一定小于0.1NA |
| D.常温下1LpH=2的硫酸溶液中H+的数目为0.01NA |
您最近半年使用:0次
名校
解题方法
7 . 已知下列物质:
①He;②NH4Cl;③AlCl3;④NaOH;⑤Cl2;⑥H2O2;⑦H2S;⑧CaC2;⑨K2S;⑩NaHSO4。
回答下列问题:
(1)共价化合物有___________ (填序号,下同),既含离子键又含共价键的有___________ 。
(2)含有非极性共价键的有___________ 。
(3)没有化学键的有___________ 。
(4)所有组成元素均满足8电子稳定结构的有___________ 。
(5)加热②使其分解,破坏的化学键是___________ 。
(6)用电子式表示⑨的形成过程___________ 。
①He;②NH4Cl;③AlCl3;④NaOH;⑤Cl2;⑥H2O2;⑦H2S;⑧CaC2;⑨K2S;⑩NaHSO4。
回答下列问题:
(1)共价化合物有
(2)含有非极性共价键的有
(3)没有化学键的有
(4)所有组成元素均满足8电子稳定结构的有
(5)加热②使其分解,破坏的化学键是
(6)用电子式表示⑨的形成过程
您最近半年使用:0次
8 . 下列化合物分子中既含 键又含
键又含 键的是
键的是
 键又含
键又含 键的是
键的是A. | B.HClO | C. | D. |
您最近半年使用:0次
9 . 实验室用电石(主要成分为 )与水反应制备的
)与水反应制备的 中混有
中混有 ,可用
,可用 溶液净化,反应的化学方程式为
溶液净化,反应的化学方程式为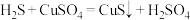 。下列说法正确的是
。下列说法正确的是
 )与水反应制备的
)与水反应制备的 中混有
中混有 ,可用
,可用 溶液净化,反应的化学方程式为
溶液净化,反应的化学方程式为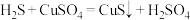 。下列说法正确的是
。下列说法正确的是A. 仅含有离子键 仅含有离子键 | B. 中碳原子的杂化轨道类型为 中碳原子的杂化轨道类型为 |
C. 中心原子上有孤电子对 中心原子上有孤电子对 | D.上述反应原理为强酸制备弱酸 |
您最近半年使用:0次
10 . Ⅰ.食品添加剂能改善食物色香味、延长保质期、调整营养结构。我国对食品添加剂的品种、适用范围、最大用量及残留量都制定了严格的标准。
(1)下列关天食品添加剂的说法正确的是________ 。
A制作豆腐时,加入石膏做凝固剂
B.制作糕点时,加入小苏打做防腐剂
C.生产加碘食盐时,加入碘单质作补碘剂
Ⅱ.SO2是葡萄、荔枝等水果储存时常用的保鲜剂,能降低水果腐烂率,提高维生素C留存率。
(2)硫原子的结构示意图为________ 。
(3)与SO2所含化学键类型相同的是________。
(4)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是________(双选)。
(5)保鲜时若SO2不慎用量过大,会使水果表面明显褪色,上述现象说明SO2________ 。
A.易溶于水B.是酸性氧化物C.具有漂白作用
Ⅲ.《食品安全国家标准·食品添加剂使用标准》(GB 2760-2014)中规定,水果中SO2残留量不得高于0.05g/kg。某种测定水果中残留SO2的方法所涉及的主要反应有:SO2+ H2O2=H2SO4、 +Ba2+=BaSO4↓。
+Ba2+=BaSO4↓。
已知:ω(SO2残留量) =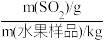 。
。
(6)称取某水果样品2 kg,经过一系列处理后,最终得到BaSO4,沉淀的质量为0.233 g。通过计算,判断该水果样品中SO2残留量是否超标______ (写出计算过程)。
(1)下列关天食品添加剂的说法正确的是
A制作豆腐时,加入石膏做凝固剂
B.制作糕点时,加入小苏打做防腐剂
C.生产加碘食盐时,加入碘单质作补碘剂
Ⅱ.SO2是葡萄、荔枝等水果储存时常用的保鲜剂,能降低水果腐烂率,提高维生素C留存率。
(2)硫原子的结构示意图为
(3)与SO2所含化学键类型相同的是________。
| A.NH4Cl | B.CaCl2 | C.AlCl3 | D.NaOH |
| A.热稳定性:H2S>SiH4 | B.溶解度:SO2> SiO2 |
| C.单质的熔点:Si > S | D.酸性:H2SO4> H2SiO3 |
A.易溶于水B.是酸性氧化物C.具有漂白作用
Ⅲ.《食品安全国家标准·食品添加剂使用标准》(GB 2760-2014)中规定,水果中SO2残留量不得高于0.05g/kg。某种测定水果中残留SO2的方法所涉及的主要反应有:SO2+ H2O2=H2SO4、
 +Ba2+=BaSO4↓。
+Ba2+=BaSO4↓。已知:ω(SO2残留量) =
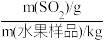 。
。(6)称取某水果样品2 kg,经过一系列处理后,最终得到BaSO4,沉淀的质量为0.233 g。通过计算,判断该水果样品中SO2残留量是否超标
您最近半年使用:0次



