1 . 五种前四周期的元素X、Y、Z、Q、T。已知X元素基态原子的M层有6种运动状态不同的电子;Y原子的价电子构型为3d84s2,基态Z原子的L层p能级有一个空轨道;Q原子的L电子层的p能级只有一对成对电子;基态T原子的M电子层上p轨道半充满。下列说法错误的是
| A.Y、Q及氢三种元素形成的某化合物,能用于制作可充电电池的电极材料 |
| B.若X、T、Z的最高价的氧化物对应的水化物分别为u、v、w,则酸性为:u>v>w。理由是含氧酸酸性与非羟基氧原子数有关 |
| C.X、Y、T三种元素第一电离能的大小次序是:X>T>Y |
| D.化合物ZQ2、ZX2均是由极性键构成的非极性分子 |
您最近一年使用:0次
名校
2 . 下列两组命题中,M组命题能用N组命题加以解释的是
| M组 | N组 | |
| A |
| 因为 |
| B | 酸性 | 氟的电负性大于氯的电负性,导致 的羧基中的羟基的极性更大 的羧基中的羟基的极性更大 |
| C |  的稳定性大于 的稳定性大于 |  的分之间作用力更大 的分之间作用力更大 |
| D | HI的沸点比HCl的高 | H-I键的键能大于H-Cl键的键能 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列关于物质的结构或性质的描述及解释都正确的是
A.键角: ,是由于H3O+中O上孤电子对数比H2O分中O上的少 ,是由于H3O+中O上孤电子对数比H2O分中O上的少 |
| B.沸点:对羟基苯甲醛>邻羟基苯甲醛,是由于对羟基苯甲醛分子间范德华力更强 |
| C.溶解度:O3在水中溶解度比在CCl4中溶解度更大,是由于O3是弱极性分子 |
D.酸性: ,是由于 ,是由于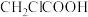 的羧基中羟基极性更小 的羧基中羟基极性更小 |
您最近一年使用:0次
2023-10-10更新
|
868次组卷
|
3卷引用:湖北省武汉市第十一中学2023-2024学年高三上学期10月月考化学试题
名校
4 . 硒( )是人体必需微量元素之一,含硒化合物在材料领域具有重要应用。一种具有聚集诱导发光效应的含
)是人体必需微量元素之一,含硒化合物在材料领域具有重要应用。一种具有聚集诱导发光效应的含 分子(IV)合成路线如下:
分子(IV)合成路线如下:

(1) 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为_______ 。
(2) 的沸点低于
的沸点低于 ,根据结构解释其原因:
,根据结构解释其原因:_______ 。
(3)关于I~Ⅳ四种物质中,下列说法正确的有_______ 。
a.I中仅有 键,其中的
键,其中的 键为非极性键
键为非极性键
b.Ⅱ易溶于水,其分子式为
c.Ⅲ、Ⅳ中C均为 杂化,S、N、
杂化,S、N、 均为
均为 杂化
杂化
d.I~Ⅳ含有的元素中,O电负性最大
(4)Ⅳ中具有孤对电子的原子有_______ 。
(5)推测硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(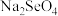 )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的空间结构为
的空间结构为_______ 。
(6)我国科学家发展了一种理论计算方法,可利用晶体衍射实验获得的结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为_______ 。
②设X的最简式的式量为 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为_______  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,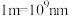 )。
)。
 )是人体必需微量元素之一,含硒化合物在材料领域具有重要应用。一种具有聚集诱导发光效应的含
)是人体必需微量元素之一,含硒化合物在材料领域具有重要应用。一种具有聚集诱导发光效应的含 分子(IV)合成路线如下:
分子(IV)合成路线如下:
(1)
 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为(2)
 的沸点低于
的沸点低于 ,根据结构解释其原因:
,根据结构解释其原因:(3)关于I~Ⅳ四种物质中,下列说法正确的有
a.I中仅有
 键,其中的
键,其中的 键为非极性键
键为非极性键b.Ⅱ易溶于水,其分子式为

c.Ⅲ、Ⅳ中C均为
 杂化,S、N、
杂化,S、N、 均为
均为 杂化
杂化d.I~Ⅳ含有的元素中,O电负性最大
(4)Ⅳ中具有孤对电子的原子有
(5)推测硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(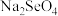 )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的空间结构为
的空间结构为(6)我国科学家发展了一种理论计算方法,可利用晶体衍射实验获得的结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为
②设X的最简式的式量为
 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,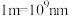 )。
)。
您最近一年使用:0次
5 . 关于分子结构和性质的说法不正确 的是
| A.干冰和AlCl3升华,所克服的作用力相同 |
| B.邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点低 |
| C.碘易溶于浓碘化钾溶液、甲烷难溶于水,都可用“相似相溶”规律解释 |
| D.氟的电负性大于氯,导致三氟乙酸的酸性强于三氯乙酸 |
您最近一年使用:0次
名校
解题方法
6 . 下列说法错误的是
A.键能: ,因此 ,因此 比 比 稳定 稳定 |
B.沸点: ,因为 ,因为 分子间范德华力更强 分子间范德华力更强 |
C.键角: ,因为NH3的成键电子对间的排斥力更大 ,因为NH3的成键电子对间的排斥力更大 |
D.极性: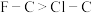 ,因此酸性 ,因此酸性 |
您最近一年使用:0次
名校
7 . 下列关于分子的结构和性质的描述中,错误的是
| A.冠醚利用不同大小的空穴适配不同大小的碱金属离子进行“分子识别” |
B.乳酸(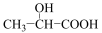 )分子中含有一个手性碳原子 )分子中含有一个手性碳原子 |
| C.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释 |
| D.氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性 |
您最近一年使用:0次
2023-04-11更新
|
372次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2022-2023学年高二下学期4月月考化学试题
8 . 氮族元素包括氮、磷、砷、锑、铋等元素,其单质及其化合物在研究和生产中有广泛的应用。试回答下列问题:
(1)N2H4是火箭发射常用的燃料,N2H4的电子式为_______ 。
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子的价电子排布式为_______ ,最高能级的电子云形状为_______ ,N、Ga、As第一电离能由大到小的顺序是_______ 。
(3)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性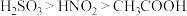 。
。
①亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其结构式为_______ ,其水解会生成两种酸,写出水解的化学方程式_______ 。
②往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是_______ (填序号)。
a.二氧化硫 b.二氧化碳 c.稀硫酸 d.醋酸
(4)已知含氧酸的酸性与结构中非羟基氧的数目有关,强酸一般有两个非羟基氧(如硫酸: ),中强酸一般有一个非羟基氧(如磷酸:
),中强酸一般有一个非羟基氧(如磷酸: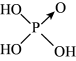 )。已知亚磷酸(H3PO3)是一种二元中强酸。请写出亚磷酸的结构式
)。已知亚磷酸(H3PO3)是一种二元中强酸。请写出亚磷酸的结构式_______ 。
(1)N2H4是火箭发射常用的燃料,N2H4的电子式为
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子的价电子排布式为
(3)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性
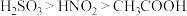 。
。①亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其结构式为
②往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是
a.二氧化硫 b.二氧化碳 c.稀硫酸 d.醋酸
(4)已知含氧酸的酸性与结构中非羟基氧的数目有关,强酸一般有两个非羟基氧(如硫酸:
 ),中强酸一般有一个非羟基氧(如磷酸:
),中强酸一般有一个非羟基氧(如磷酸: )。已知亚磷酸(H3PO3)是一种二元中强酸。请写出亚磷酸的结构式
)。已知亚磷酸(H3PO3)是一种二元中强酸。请写出亚磷酸的结构式
您最近一年使用:0次
名校
9 . 下列叙述正确的是
| A.配位键在形成时,是由成键双方各提供一个电子形成共用电子对 |
| B.最外层电子排布式为ns1的原子一定属于ⅠA族元素,也一定属于s区 |
| C.(HO)2HPO为二元弱酸 |
| D.CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的 |
您最近一年使用:0次
名校
解题方法
10 . 下列叙述中正确的是
| A.能电离出H+的化合物除水外都是酸,分子中含有几个氢原子它就是几元酸 |
| B.非金属性越强,其对应的含氧酸的酸性越强 |
| C.同一元素的含氧酸,该元素的化合价越高,其酸性越强,氧化性也越强 |
| D.H3PO4和H2CO3分子中非羟基氧的个数均为1,但它们的酸性不相近,H3PO4是中强酸而H2CO3是弱酸 |
您最近一年使用:0次

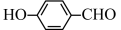 的沸点高于
的沸点高于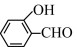
 分子间范德华力更大
分子间范德华力更大

