名校
1 . 下列对分子性质的解释中,不正确的是
| A.BF3为平面三角形分子 |
B.乳酸(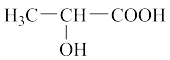 )分子中含有两个手性碳原子 )分子中含有两个手性碳原子 |
| C.H3PO4分子中P原子采取sp3杂化 |
| D.酸性:H3PO4>HClO,因为H3PO4中非羟基氧原子数大于次氯酸中非羟基氧原子数 |
您最近一年使用:0次
2021-04-12更新
|
151次组卷
|
3卷引用:吉林省长春市第二十九中学2020-2021学年高二下学期第一学程考试化学试题
名校
解题方法
2 . 下列物质酸性大小比较正确的是
| A.HClO>HClO2>HClO3>HClO4 | B.H2SO4>HClO4 |
| C.H3AsO3>HNO2 | D.HI>HCl>HF |
您最近一年使用:0次
名校
3 . 下列对分子性质的解释中,不正确的是
| A.甲硫醇(CH3SH)比甲醇的熔点低的原因是甲醇分子间易形成氢键 |
B.乳酸( )分子中含有一个手性碳原子 )分子中含有一个手性碳原子 |
| C.碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”原理解释 |
| D.SO2易溶于水只是因为相似相溶原理 |
您最近一年使用:0次
2021-04-07更新
|
200次组卷
|
2卷引用:山西省太原市第五中学2020-2021学年高二下学期4月阶段性检测化学试题
名校
4 . 下列说法中不正确的是
| A.乳酸分子CH3CH(OH)COOH含有一个手性碳原子 |
| B.酸性强弱:H2SO4>H2SO3 |
| C.水稳定是因为水能形成分子间氢键 |
| D.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低 |
您最近一年使用:0次
2021-03-29更新
|
143次组卷
|
2卷引用:湖北省枣阳市第一中学2020-2021学年高二下学期3月月考化学试题
名校
解题方法
5 . (1)氨易溶于水的原因是__ 。(写出两点即可)
(2)化学上有一种见解,认为含氧酸的通式可写成(HO)mROn,如果成酸元素R相同,则n值越大,酸性越__ (填“强”或“弱”)。以下各种含氧酸HClO、HClO3、H2SO3、HClO4的酸性由强到弱排列为___ 。
(3)熔点、沸点HF__ HI(填“>”或“<”);原因:__ 。
(4)下列4种物质熔点沸点由高到低排列为__ (填序号)。
①金刚石(C—C)②锗(Ge—Ge)③晶体硅(Si—Si)④金刚砂(Si—C)
(5)为了减缓温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。若有1molCH4生成,则有__ molσ键和__ molπ键断裂。
(2)化学上有一种见解,认为含氧酸的通式可写成(HO)mROn,如果成酸元素R相同,则n值越大,酸性越
(3)熔点、沸点HF
(4)下列4种物质熔点沸点由高到低排列为
①金刚石(C—C)②锗(Ge—Ge)③晶体硅(Si—Si)④金刚砂(Si—C)
(5)为了减缓温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。若有1molCH4生成,则有
您最近一年使用:0次
名校
6 . 磷化氢( PH3)是常见的储物熏蒸杀虫剂,广泛应用于粮食、烟草、中草药等行业的杀虫作业。回答下列问题:
(1) NH3、 PH3、AsH3的组成和结构相似,但NH3、AsH3的沸点均高于PH3,原因分别是____
(2)在密闭粮仓内放置磷化铝(AIP)片剂,与水蒸气反应产生PH3气体,该反应的化学方程式为____ 。
(3) PH3有剧毒,熏蒸杀虫的同时可被粮食吸附,并发生下列变化(未配平):
①PH3+O2→P2H4+H2O ②P2H4+O2+H2O→H3PO2 ③H3PO2+O2→H3PO3 ④H3PO3+O2→H3PO4(无毒)
P2H4的电子式为_____ ; H3PO3的名称为亚磷酸,H3PO2的名称为______ ; 反应②中氧化剂与还原剂的物质的量之比为_____ ;H3PO2、H3PO3能与过量NaOH反应分别生成NaH2PO2、Na2HPO3说明H3PO2为一元酸,分子中仅有1个H原子能被电离成为H+,可推断其结构式为 ,同理,可推断亚磷酸H3PO3的结构式为
,同理,可推断亚磷酸H3PO3的结构式为______ 。
(4) PH3杀虫的机理尚不够清楚,研究发现PH3能断裂虫体内HOOCCH(NH2)CH2S- SCH2CH(NH2 )COOH(胱氨酸)或多肽链或酶中的二硫键,将其转化为巯基(—SH), 可能是其杀虫机理之一、假定PH3与胱氨酸(用RS—SR 简化表示)按物质的量2: 1发生反应,产物之一为HSCH2CH( NH2)COOH(半胱氨酸,用RSH简化表示),则可推测反应的化学方程式为______ 。
(5) PH3能与硝酸银溶液反应生成黑色磷化银(Ag3P)沉淀和硝酸,据此可以用浸有5% AgNO3溶液的试纸检测熏蒸后的粮堆中是否存在PH3。PH3与硝酸银溶液反应的离子方程式为_______ 。
(1) NH3、 PH3、AsH3的组成和结构相似,但NH3、AsH3的沸点均高于PH3,原因分别是
(2)在密闭粮仓内放置磷化铝(AIP)片剂,与水蒸气反应产生PH3气体,该反应的化学方程式为
(3) PH3有剧毒,熏蒸杀虫的同时可被粮食吸附,并发生下列变化(未配平):
①PH3+O2→P2H4+H2O ②P2H4+O2+H2O→H3PO2 ③H3PO2+O2→H3PO3 ④H3PO3+O2→H3PO4(无毒)
P2H4的电子式为
 ,同理,可推断亚磷酸H3PO3的结构式为
,同理,可推断亚磷酸H3PO3的结构式为(4) PH3杀虫的机理尚不够清楚,研究发现PH3能断裂虫体内HOOCCH(NH2)CH2S- SCH2CH(NH2 )COOH(胱氨酸)或多肽链或酶中的二硫键,将其转化为巯基(—SH), 可能是其杀虫机理之一、假定PH3与胱氨酸(用RS—SR 简化表示)按物质的量2: 1发生反应,产物之一为HSCH2CH( NH2)COOH(半胱氨酸,用RSH简化表示),则可推测反应的化学方程式为
(5) PH3能与硝酸银溶液反应生成黑色磷化银(Ag3P)沉淀和硝酸,据此可以用浸有5% AgNO3溶液的试纸检测熏蒸后的粮堆中是否存在PH3。PH3与硝酸银溶液反应的离子方程式为
您最近一年使用:0次
19-20高三·浙江·阶段练习
解题方法
7 . (1)比较给出H+能力的相对强弱:Al(OH)3_______ NaHCO3 (填“<” “>”或者“=”) ;用一个离子方程式说明 和
和 结合H+能力的相对强弱
结合H+能力的相对强弱_______ 。
(2)CN2H4是离子化合物且各原子均满足稳定结构,写出CN2H4的电子式_______ 。
(3)相同条件下冰的密度比水小,主要原因是_______ 。
 和
和 结合H+能力的相对强弱
结合H+能力的相对强弱(2)CN2H4是离子化合物且各原子均满足稳定结构,写出CN2H4的电子式
(3)相同条件下冰的密度比水小,主要原因是
您最近一年使用:0次
19-20高三·浙江·阶段练习
解题方法
8 . 下图是磷酸、亚磷酸、次磷酸的结构式,其中磷酸为三元中强酸,亚磷酸为二元弱酸,则下列说法正确的是


| A.NaH2PO4、NaH2PO3、NaH2PO2 都是酸式盐 |
B.0.1 mol/L NaH2PO3溶液中c( )>c( )>c( ) ) |
C.NaH2PO4溶液呈酸性,是因为 的水解程度比电离程度大 的水解程度比电离程度大 |
| D.常温下,NaH2PO2溶液pH>7, 具有强还原性 |
您最近一年使用:0次
名校
解题方法
9 . 下列说法正确的是
| A.无机含氧酸分子中有几个氢原子,它就属于几元酸 |
| B.CH4、C2H2、HCN都是含有极性键的非极性分子 |
C. 和CH3-中所有原子都在同一平面 和CH3-中所有原子都在同一平面 |
| D.范德华力:HI>HBr>HCl |
您最近一年使用:0次
10 . 下列各项叙述中,正确的是
| A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| B.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
C.由图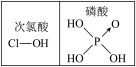 知酸性:H3PO4>HClO,因为H3PO4中非羟基氧原子数大于次氯酸中非羟基氧原子数 知酸性:H3PO4>HClO,因为H3PO4中非羟基氧原子数大于次氯酸中非羟基氧原子数 |
| D.元素周期表中s区、d区和ds区的元素都是金属元素 |
您最近一年使用:0次



