1 . 下列说法中正确的是
①充有氖气的霓虹灯管通电时会发出红色光的主要原因是电子由基态向激发态跃迁时吸收除红光以外的光线② 不符合泡利原理③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快④
不符合泡利原理③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快④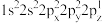 违反了洪特规则,是激发态原子的电子排布⑤钠离子的最高能级为3s⑥25℃时,将
违反了洪特规则,是激发态原子的电子排布⑤钠离子的最高能级为3s⑥25℃时,将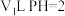 的盐酸与
的盐酸与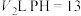 的氢氧化钠溶液混合后
的氢氧化钠溶液混合后 ,则
,则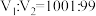 ⑦F的最高能级的电子云轮廓图:
⑦F的最高能级的电子云轮廓图: ⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释⑨氯乙酸、二氯乙酸、三氯乙酸、三氟乙酸的酸性依次增强
⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释⑨氯乙酸、二氯乙酸、三氯乙酸、三氟乙酸的酸性依次增强
①充有氖气的霓虹灯管通电时会发出红色光的主要原因是电子由基态向激发态跃迁时吸收除红光以外的光线②
 不符合泡利原理③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快④
不符合泡利原理③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快④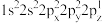 违反了洪特规则,是激发态原子的电子排布⑤钠离子的最高能级为3s⑥25℃时,将
违反了洪特规则,是激发态原子的电子排布⑤钠离子的最高能级为3s⑥25℃时,将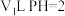 的盐酸与
的盐酸与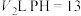 的氢氧化钠溶液混合后
的氢氧化钠溶液混合后 ,则
,则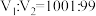 ⑦F的最高能级的电子云轮廓图:
⑦F的最高能级的电子云轮廓图: ⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释⑨氯乙酸、二氯乙酸、三氯乙酸、三氟乙酸的酸性依次增强
⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释⑨氯乙酸、二氯乙酸、三氯乙酸、三氟乙酸的酸性依次增强| A.①②③⑦ | B.②④⑥⑨ | C.②⑥⑨ | D.①②③⑦⑧ |
您最近半年使用:0次
2 . 2023年诺贝尔化学奖被授予蒙吉·巴文迪、路易斯,布鲁斯和阿列克谢·叶基莫夫三位科学家,以表彰他们“发现和合成了量子点,为纳米技术埋下了重要种子”。钙钛矿量子点是结构与钙钛矿( )相似的一种新型纳米材料,应用于量子点显示与照明、太阳能电池等领域。
)相似的一种新型纳米材料,应用于量子点显示与照明、太阳能电池等领域。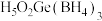 是钙钛矿型化合物,量子化学计算结果显示其具有良好的光电化学性能。下列说法错误的是
是钙钛矿型化合物,量子化学计算结果显示其具有良好的光电化学性能。下列说法错误的是
 )相似的一种新型纳米材料,应用于量子点显示与照明、太阳能电池等领域。
)相似的一种新型纳米材料,应用于量子点显示与照明、太阳能电池等领域。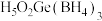 是钙钛矿型化合物,量子化学计算结果显示其具有良好的光电化学性能。下列说法错误的是
是钙钛矿型化合物,量子化学计算结果显示其具有良好的光电化学性能。下列说法错误的是A. 中B的杂化方式为 中B的杂化方式为 |
B.H、B、O的电负性大小顺序是 |
| C.基态Ge原子有32种不同运动状态的电子 |
| D.与Ti同周期且含有相同未成对电子数的主族元素有两种 |
您最近半年使用:0次
2024-04-08更新
|
64次组卷
|
2卷引用:河南省南阳市六校联考2023-2024学年高二下学期3月月考化学试卷
3 . 氟特加氟碳表面改性处理剂是前苏联根据航天器在太空恶劣环境需要无固体颗粒、化学稳定性和热稳定性高、耐受性强、减摩抗磨效果好、综合性能持续时间长的摩擦润滑材料而开发的一种全新的氟碳涂层材料,其全称为全氟聚氧烷基碳酸氮素衍生物。下列有关其组成元素的性质描述正确的是
| A.基态碳原子核外电子的空间运动状态有6种 |
| B.C、N、O、F的第一电离能由大到小的顺序为:F>O>N>C |
| C.C、N的第三电离能的大小顺序为:N>C |
| D.C、N、O、F的电负性由大到小的顺序为:F>O>N>C |
您最近半年使用:0次
2024-04-08更新
|
55次组卷
|
2卷引用:河南省南阳市六校联考2023-2024学年高二下学期3月月考化学试卷
4 . 下列关于原子轨道的叙述正确的是
A.p能级的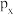 、 、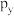 、 、 轨道相互垂直,其能量大小关系为 轨道相互垂直,其能量大小关系为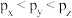 |
| B.2s电子能量比1s电子能量高,总是在比1s电子离核更远的地方运动 |
| C.1s、2s、3s、4s电子云轮廓图形状相同,但大小不同 |
| D.电子只能在电子云轮廓图的范围内运动 |
您最近半年使用:0次
2024-04-08更新
|
92次组卷
|
2卷引用:河南省南阳市六校联考2023-2024学年高二下学期3月月考化学试卷
解题方法
5 . 第三周期部分主族元素及 的氟化物的熔点如表所示,
的氟化物的熔点如表所示, 分子的空间结构为正八面体,结构如图所示。
分子的空间结构为正八面体,结构如图所示。
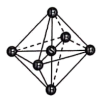
下列说法正确的是
 的氟化物的熔点如表所示,
的氟化物的熔点如表所示, 分子的空间结构为正八面体,结构如图所示。
分子的空间结构为正八面体,结构如图所示。
| 化合物 |  |  |  |  |
| 熔点/℃ | 993 | 1040 | -90 | -50.5 |
A. 为共价晶体 为共价晶体 | B.离子半径: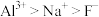 |
C.基态 原子核外电子运动状态有8种 原子核外电子运动状态有8种 | D. 的二氮代物 的二氮代物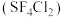 有2种 有2种 |
您最近半年使用:0次
解题方法
6 . 人们常将在同一原子轨道上运动、自旋方向相反的2个电子称为“电子对”;将在同一原子轨道上运动的单个电子称为“未成对电子”。以下有关第四周期元素原子的“未成对电子”的说法,错误的是
| A.4s电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子” |
| B.4p电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子” |
| C.3d电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子” |
| D.3d电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子” |
您最近半年使用:0次
解题方法
7 . 已知:NHCl2在水中产生几种化合物,其中一种物质M具有强氧化性且常用于自来水的消毒。下列有关说法错误的是
| A.基态N原子核外有3种不同能量的电子 |
| B.化合物M是次氯酸 |
| C.M分子的空间构型是直线形 |
| D.NHCl2分子中氮原子的杂化类型为sp3 |
您最近半年使用:0次
名校
解题方法
8 . 下列化学用语表达正确的是
A.NH3的VSEPR模型: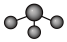 |
| B.As原子的简化电子排布式:[Ar]4s24p3 |
C.p-p σ键电子云轮廓图: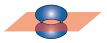 |
D.基态Mn原子价电子轨道表示式: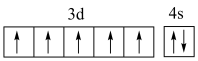 |
您最近半年使用:0次
2024-02-01更新
|
497次组卷
|
2卷引用:河南省沁阳一中2023—2024学年高二下学期开学考试 化学试卷
名校
解题方法
9 . 我国科学家研发的新型光学材料(Sn7Br10S2)可替代传统光学材料硫镓银(AgGaS2)和磷锗锌(ZnGeP2)。请回答下列问题:
(1)基态硫原子核外电子云轮廓图呈哑铃形的能级上占据的电子总数为___________ 。
(2)SF6可用作高压发电系统的绝缘气体,其分子呈正八面体结构,如图所示。
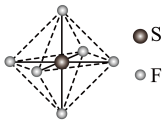
①SF6是___________ (填“极性”或“非极性”)分子。
②1molSF6分子中含___________ molσ键。
(3)HF、HCl、HBr的酸性由强到弱的顺序为___________ (填化学式,下同);沸点由高到低的顺序为___________ ;还原性由强到弱的顺序为___________ 。
(4)Ga(CH3)3和NH3在一定条件下可合成半导体材料GaN和CH4。Ga(CH3)3分子中Ga原子和C原子构成的空间构型是___________ ,碳原子的杂化类型是___________ 。
(5)四卤化锡的熔点如下表所示:
它们熔点递变的主要原因是___________ 。
(1)基态硫原子核外电子云轮廓图呈哑铃形的能级上占据的电子总数为
(2)SF6可用作高压发电系统的绝缘气体,其分子呈正八面体结构,如图所示。

①SF6是
②1molSF6分子中含
(3)HF、HCl、HBr的酸性由强到弱的顺序为
(4)Ga(CH3)3和NH3在一定条件下可合成半导体材料GaN和CH4。Ga(CH3)3分子中Ga原子和C原子构成的空间构型是
(5)四卤化锡的熔点如下表所示:
| 物质 | SnCl4 | SnBr4 | SnI4 |
| 熔点/℃ | ﹣33 | 31 | 144.5 |
您最近半年使用:0次
10 . 下列说法中正确的是
①原子光谱的特征谱线用于鉴定元素,从 2
2 s2
s2 1跃迁至
1跃迁至 2
2 s2
s2 4时释放能量
4时释放能量
②Cl2分子中,Cl-Cl键是p-pσ键
③铍原子最外层原子轨道的电子云图:
④ ,该电子排布图违背了泡利原理
,该电子排布图违背了泡利原理
⑤键能N-N>P-P、N-H>P-H,因此N2H4的沸点大于P2H4的沸点
⑥碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
⑦氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
⑧三氧化硫有单分子气体和三聚分子固体(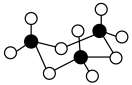 )两种存在形式,两种形式中S原子的杂化轨道类型不同
)两种存在形式,两种形式中S原子的杂化轨道类型不同
①原子光谱的特征谱线用于鉴定元素,从
 2
2 s2
s2 1跃迁至
1跃迁至 2
2 s2
s2 4时释放能量
4时释放能量②Cl2分子中,Cl-Cl键是p-pσ键
③铍原子最外层原子轨道的电子云图:

④
 ,该电子排布图违背了泡利原理
,该电子排布图违背了泡利原理⑤键能N-N>P-P、N-H>P-H,因此N2H4的沸点大于P2H4的沸点
⑥碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
⑦氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
⑧三氧化硫有单分子气体和三聚分子固体(
 )两种存在形式,两种形式中S原子的杂化轨道类型不同
)两种存在形式,两种形式中S原子的杂化轨道类型不同| A.①②④⑦ | B.①②⑤⑦ | C.①②⑦⑧ | D.①④⑥⑦ |
您最近半年使用:0次



