名校
解题方法
1 . 现有七种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题:
(1)B的元素符号为___________ ,基态原子价电子轨道表示式为___________ 。
(2)基态D原子中能量最高的电子所在的原子轨道的电子云在空间有___________ 个伸展方向,原子轨道呈___________ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子轨道表示式为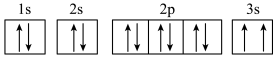 ,该同学所写的轨道表示式违反了
,该同学所写的轨道表示式违反了___________ 。
(4)E元素原子核外有___________ 种运动状态不同的电子。
(5)检验F元素的方法是___________ 。
| A | 元素原子半径在周期表中最小,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p轨道总电子数比s轨道总电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ·mol-1、I2=1 451 kJ·mol-1、I3=7 733 kJ·mol-1、I4=10 540 kJ·mol-1 |
| D | 原子核外所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为4,原子半径在同周期中最小 |
| F | 是前四周期中电负性最小的元素 |
(1)B的元素符号为
(2)基态D原子中能量最高的电子所在的原子轨道的电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子轨道表示式为
 ,该同学所写的轨道表示式违反了
,该同学所写的轨道表示式违反了(4)E元素原子核外有
(5)检验F元素的方法是
您最近半年使用:0次
名校
解题方法
2 . 下列有关说法错误的是

| A.[Zn(NH3)4]2+的球棍模型如图1所示,1个[Zn(NH3)4]2+中有4个配位键 |
| B.CaF2晶体的晶胞如图2所示,Ca2+的配位数与F-的配位数之比为1∶2 |
| C.氢原子的电子云图如图3所示,小黑点越密,表明1s电子在原子核外该处出现的概率越大 |
| D.金属Cu中铜原子的堆积模型如图4所示,该金属晶体为面心立方堆积 |
您最近半年使用:0次
名校
解题方法
3 . 氮及其化合物应用广泛。回答下列问题:
(1)基态N原子处于最高能级的电子云轮廓图为__________ 形。
(2)胍(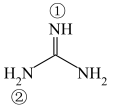 )为平面形分子,存在大π键
)为平面形分子,存在大π键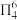 。胍属于
。胍属于__________ 分子(填“极性”或“非极性”),①号N原子H-N-C键角__________ ②号N原子H-N-C键角(填“>”“<”或“=”),胍易吸收空气中H2O和CO2,其原因是____________________________________ 。
(3)氮化钴属于立方晶系,经Cu掺杂得催化剂X,经Li掺杂得催化剂Y。
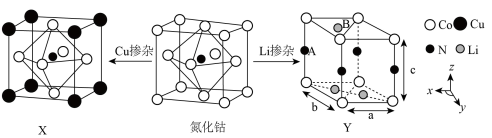
X属于立方晶系,晶胞参数为dpm,距离最近Co原子的核间距为__________ pm,Y属于六方晶系,晶胞参数为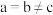 ,
, ,
,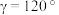 ,如A点原子的分数坐标为
,如A点原子的分数坐标为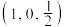 ,则B点Li原子的分数坐标为
,则B点Li原子的分数坐标为____________ ,1个N原子周围距离相等且最近的Li原子数目为_____________ 。
(1)基态N原子处于最高能级的电子云轮廓图为
(2)胍(
 )为平面形分子,存在大π键
)为平面形分子,存在大π键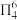 。胍属于
。胍属于(3)氮化钴属于立方晶系,经Cu掺杂得催化剂X,经Li掺杂得催化剂Y。

X属于立方晶系,晶胞参数为dpm,距离最近Co原子的核间距为
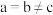 ,
, ,
,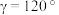 ,如A点原子的分数坐标为
,如A点原子的分数坐标为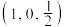 ,则B点Li原子的分数坐标为
,则B点Li原子的分数坐标为
您最近半年使用:0次
名校
解题方法
4 . 运用物质结构与性质的相关知识,回答下列问题:
(1) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是_______ 。基态 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有_____ 个伸展方向,原子轨道呈______ 形。
(2) 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为________ , 价电子轨道表示式为
价电子轨道表示式为________ 。
(3) 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
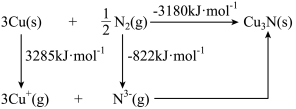
通过图中数据________ (填“能”或“不能”)计算出 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为________  。
。
(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。
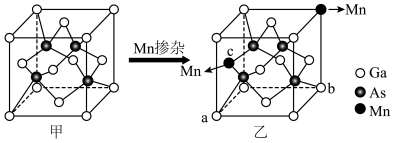
①GaAs晶胞中距离Ga原子最近As原子的个数为________ 。
②掺杂 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为________ (化为最简整数比)。
(1)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有(2)
 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为 价电子轨道表示式为
价电子轨道表示式为(3)
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
通过图中数据
 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为 。
。(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①GaAs晶胞中距离Ga原子最近As原子的个数为
②掺杂
 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为
您最近半年使用:0次
5 . 制取催化剂 的原理为:
的原理为: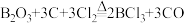 。下列说法错误的是
。下列说法错误的是
 的原理为:
的原理为: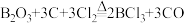 。下列说法错误的是
。下列说法错误的是A.基态碳原子价电子轨道表示式为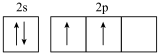 |
B. 中 中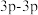 轨道重叠示意图为 轨道重叠示意图为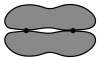 |
C. 分子的空间结构为平面三角形 分子的空间结构为平面三角形 |
D. 电子式为: 电子式为: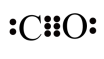 |
您最近半年使用:0次
6 . 在基态多电子原子中,下列有关叙述不正确的是
| A.第二能层的符号为L,有2s、2p共2个能级 |
| B.d能级上有5个原子轨道,最多可容纳10个电子 |
| C.p能级电子云有3种不同的空间伸展方向 |
| D.电子的能量是由能层、能级、电子云的空间伸展方向共同决定的 |
您最近半年使用:0次
2024-03-04更新
|
231次组卷
|
4卷引用:福建省永春第一中学2023-2024学年高二下学期3月月考化学试题
福建省永春第一中学2023-2024学年高二下学期3月月考化学试题安徽省淮南市第一中学2023-2024学年高二下学期开学考试化学试题(已下线)1.1.2 构造原理与电子排布式 电子云与原子轨道(基础)(已下线)1.1.2 构造原理与电子排布式 电子云与原子轨道(提高)
7 . 甲钴胺是神经元营养药物,由C、H、Co、N、O、P元素组成。下列说法正确的是
A.还原性: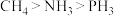 |
| B.基态P原子的最高能级轨道形状为球形 |
| C.同周期中第一电离能小于N的元素有5种 |
D.基态Co原子价层电子轨道表示式为 |
您最近半年使用:0次
2024-02-24更新
|
150次组卷
|
2卷引用:福建省漳州市华安县第一中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
8 . 下列化学用语表示正确的是
A. 分子的球棍模型: 分子的球棍模型: |
B. 的电子式: 的电子式: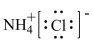 |
C.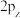 电子云轮廓图: 电子云轮廓图: |
D.邻羟基苯甲醛分子内氢键示意图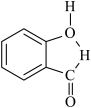 |
您最近半年使用:0次
名校
解题方法
9 . 下列化学用语或图示表达不正确的是
A.金刚石的晶体结构: |
B.基态溴原子电子占据最高能级的电子云轮廓图: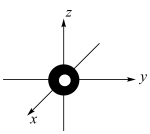 |
C.乙炔的球棍模型: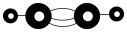 |
D. 的 的 模型为 模型为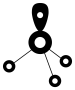 |
您最近半年使用:0次
名校
10 . 下列化学用语表示正确的是
A.基态 最高能级的电子云轮廓图: 最高能级的电子云轮廓图: |
B.2-甲基戊烷的键线式 |
C. 的空间结构: 的空间结构: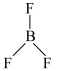 (平面三角形) (平面三角形) |
D.甲酸乙酯的结构简式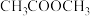 |
您最近半年使用:0次



