1 . 下列化学用语或图示表达正确的是
A. 的电子式为 的电子式为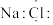 | B. 的VSEPR模型为 的VSEPR模型为 |
C.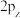 电子云图为 电子云图为 | D.基态 原子的价层电子轨道表示式为 原子的价层电子轨道表示式为 |
您最近一年使用:0次
2023-06-28更新
|
7284次组卷
|
16卷引用:上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题
上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题2023年高考北京卷化学真题(已下线)2023年北京卷高考真题变式题(选择题1-5)(已下线)第21讲分子结构与性质江西省吉安市宁冈中学2023-2024学年高三上学期开学考试化学试题(已下线)专题02 化学用语及其应用-2023年高考化学真题题源解密(新高考专用)新疆疏附县第一中学2023-2024学年高三上学期开学摸底测试化学试题北京市第一七一中学2023-2024学年高三上学期10月考化学试题北京师范大学第二附属中学2023-2024学年高二上学期12月月考化学试题 北京师范大学第二附属中学2023-2024学年高三上学期期中考试化学试题(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)北京师范大学附属中学2023-2024学年高二上学期期末考试化学试卷广东省珠海市第三中学2023-2024学年高二下学期3月月考化学试卷北京市第五十五中学2023-2024学年高二下学期(等级考)3月调研化学试卷海南省文昌中学2023-2024学年高二下学期第一次月考化学试题福建省福建师范大学附属中学2023-2024学年高三上学期开学考化学试题
名校
解题方法
2 . 下列表示正确的是
A.CH3Cl的电子式: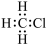 | B.镁原子最外层电子的电子云图: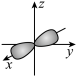 |
C.四氯化碳的比例模型: | D.乙酸甲酯的结构简式:CH3OOCCH3 |
您最近一年使用:0次
2023-04-03更新
|
583次组卷
|
11卷引用:上海市黄浦区2022届高三一模化学试题
上海市黄浦区2022届高三一模化学试题(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)上海市复旦大学附属中学2023届高三下学期开学阶段性集中练习化学试题上海市复旦大学附属中学2023届高三阶段性练习化学试题(已下线)卷05 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)卷02 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)化学(辽宁A卷)-学易金卷:2023年高考第一次模拟考试卷辽宁省葫芦岛市第一高级中学2022-2023学年高三上学期期末线上教学阶段检测化学试题辽宁省本溪市高级中学2023届高三下学期第一次摸底考试化学试题辽宁省大连市育明高级中学2023届高三下学期第1次模拟考试化学试题
解题方法
3 . 下列图示错误的是
A.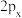 的电子云: 的电子云: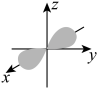 | B.金刚石晶体结构模型: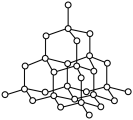 |
C. 形成过程: 形成过程: | D. 球棍模型: 球棍模型: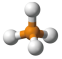 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的是
| A.3s2表示3s能级有2个轨道 |
| B.p能级的能量一定比s能级的能量高 |
| C.在离核越近区域内运动的电子,能量越低 |
| D.1个原子轨道里,最少要容纳2个电子 |
您最近一年使用:0次
2023-02-15更新
|
492次组卷
|
4卷引用: 上海交通大学附属中学2022-2023学年高三下学期开学摸底考试化学试题
上海交通大学附属中学2022-2023学年高三下学期开学摸底考试化学试题上海市南汇中学2023-2024学年高三上学期10月月考化学试题山西省名校2022-2023学年高二下学期联合考试化学试题(已下线)1.1.1 能层与能级 基态与激发态(提高)
名校
解题方法
5 . 锗、锡、铅均属于ⅣA族元素,它们的单质与化合物广泛应用于生活的各个领域。
Ⅰ.完成下列填空:
(1)锗元素原子核外能量最高的电子有_______ 个,它们运动所形成的电子云形状为_______ 形。
(2)氢化锗(GeH4)结构与甲烷类似,在常温常压下是具有刺激性气味的无色有毒气体。从结构角度比较GeH4与CH4沸点高低并说明理由_______ 。氢化锗的液氨溶液具有较好的导电性,主要是因为GeH4与NH3反应生成了 和
和_______ (填化学式)两种离子。
Ⅱ.三水锡酸钠(Na2SnO3·3H2O)是一种易溶于水的无色晶体,露置在空气中会逐渐转化成Na2CO3和Sn(OH)4。
(3)常温下,相同物质的量浓度的Na2SnO3溶液与Na2CO3溶液,前者pH_______ (填“大于”“小于”或“等于”)后者。
(4)写出三水锡酸钠露置在空气中发生反应的化学方程式_______ 。
Ⅲ.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、 、
、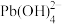 。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。
。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。

(5)Pb(NO3)2溶液中,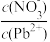
_______ 2(填“>”“=”或“<”);往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液中存在的阳离子除Na+外,还有_______ (填微粒符号)。
(6)科学家发现一种新型脱铅剂DH,能有效除去水中的痕量铅。已知DH脱铅过程中主要发生反应为:2DH(s)+Pb2+(aq) D2Pb(s)+2H+。则脱铅时最合适的pH约为
D2Pb(s)+2H+。则脱铅时最合适的pH约为_______ (选填编号)。
a.4~5 b.6~7 c.8~10 d.12~14
Ⅰ.完成下列填空:
(1)锗元素原子核外能量最高的电子有
(2)氢化锗(GeH4)结构与甲烷类似,在常温常压下是具有刺激性气味的无色有毒气体。从结构角度比较GeH4与CH4沸点高低并说明理由
 和
和Ⅱ.三水锡酸钠(Na2SnO3·3H2O)是一种易溶于水的无色晶体,露置在空气中会逐渐转化成Na2CO3和Sn(OH)4。
(3)常温下,相同物质的量浓度的Na2SnO3溶液与Na2CO3溶液,前者pH
(4)写出三水锡酸钠露置在空气中发生反应的化学方程式
Ⅲ.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、
 、
、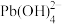 。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。
。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。
(5)Pb(NO3)2溶液中,
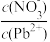
(6)科学家发现一种新型脱铅剂DH,能有效除去水中的痕量铅。已知DH脱铅过程中主要发生反应为:2DH(s)+Pb2+(aq)
 D2Pb(s)+2H+。则脱铅时最合适的pH约为
D2Pb(s)+2H+。则脱铅时最合适的pH约为a.4~5 b.6~7 c.8~10 d.12~14
您最近一年使用:0次
2022-05-29更新
|
273次组卷
|
4卷引用:上海市虹口区2022届高三下学期第二次模拟考试化学试题
上海市虹口区2022届高三下学期第二次模拟考试化学试题(已下线)2022年北京高考真题变式题1-14(已下线)2022年北京高考真题化学试题变式题(结构与性质)江西省吉安市永丰县永丰中学2022-2023学年高二上学期1月期末化学(B班)试题
名校
解题方法
6 . 硼及其化合物在工业中有很多用处。一些硼的卤化物的沸点如图所示:
(1)硼原子的核外共有____ 种形状不同的电子云;溴原子的最外层电子排布式为____ 。
(2)表中三种卤化物分子的空间构型均为平面正三角形,由此推断F—B—F的键角为____ ,BF3属于____ 分子(填“极性”或“非极性”)。
(3)解释表中三种卤化硼沸点存在差异的原因____ 。
CS2是一种重要的化工原料。
(4)工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g) CS2(g)+2H2S(g),CS2的结构式为
CS2(g)+2H2S(g),CS2的结构式为____ ,利用燃煤废气(含N2、O2、SO2、CO2、H2O、NOx等)使尾气中的H2S转化为单质硫,可实现废物利用,保护环境,写出其中一个反应的化学方程式____ 。
| 卤化物 | BF3 | BCl3 | BBr3 |
| 沸点/℃ | -100.3 | 12.5 | 90 |
(2)表中三种卤化物分子的空间构型均为平面正三角形,由此推断F—B—F的键角为
(3)解释表中三种卤化硼沸点存在差异的原因
CS2是一种重要的化工原料。
(4)工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g)
 CS2(g)+2H2S(g),CS2的结构式为
CS2(g)+2H2S(g),CS2的结构式为
您最近一年使用:0次
7 . 下列对化学用语的叙述正确的是
| A.碳原子最外层电子云有三种不同的伸展方向 | B.CCl4的比例模型: |
C.氮分子的结构式: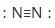 | D.溴化铵的电子式: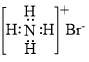 |
您最近一年使用:0次
2021-10-03更新
|
363次组卷
|
3卷引用:上海交通大学附属中学2020-2021学年高三上学期第一次月考化学试题
名校
解题方法
8 . 硼原子的2p电子和该原子的其它电子的相同之处可能是
| A.能量 | B.电子云的形状 | C.电子云的伸展方向 | D.电子自旋 |
您最近一年使用:0次
名校
解题方法
9 . 2020年9月科学家发现金星上有磷化氢( ),实验室制备
),实验室制备 的常用方法有两种:
的常用方法有两种:
①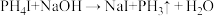
②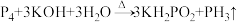
完成下列填空:
(1)P核外能量最高的电子具有相同的___________ (填写序号)。
A.轨道B.自旋方向C.电子云形状D.电子云伸展反应
(2)已知 与
与 的结构相似,
的结构相似, 的空间结构是
的空间结构是___________ 。 的分解温度比
的分解温度比
___________ (填“高”、“低”),判断的依据是___________ 。
(3)已知 为三元酸,其结构式为:
为三元酸,其结构式为: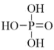 。
。
①次磷酸( 中的P的成键情况与
中的P的成键情况与 中的相同,则
中的相同,则 的结构式是
的结构式是___________ 。
②利用反应②制备 时,即使KOH过量,仍只生成
时,即使KOH过量,仍只生成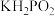 ,说明
,说明 是
是___________ 元酸。
(4)常温下, 在不同pH的溶液中,各种含磷微粒的质量分数如图所示。
在不同pH的溶液中,各种含磷微粒的质量分数如图所示。

①电离平衡常数与化学平衡常数意义相同,写出 第二步电离平衡常数表达式
第二步电离平衡常数表达式
___________ 。
(2)图中可推断 溶液呈
溶液呈___________ (填“酸”、“碱”、“中”)性,可能的原因是___________ 。 溶液中各含磷微粒以及
溶液中各含磷微粒以及 按浓度由大到小的顺序排列
按浓度由大到小的顺序排列___________ 。
 ),实验室制备
),实验室制备 的常用方法有两种:
的常用方法有两种:①
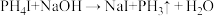
②
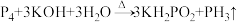
完成下列填空:
(1)P核外能量最高的电子具有相同的
A.轨道B.自旋方向C.电子云形状D.电子云伸展反应
(2)已知
 与
与 的结构相似,
的结构相似, 的空间结构是
的空间结构是 的分解温度比
的分解温度比
(3)已知
 为三元酸,其结构式为:
为三元酸,其结构式为: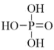 。
。①次磷酸(
 中的P的成键情况与
中的P的成键情况与 中的相同,则
中的相同,则 的结构式是
的结构式是②利用反应②制备
 时,即使KOH过量,仍只生成
时,即使KOH过量,仍只生成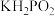 ,说明
,说明 是
是(4)常温下,
 在不同pH的溶液中,各种含磷微粒的质量分数如图所示。
在不同pH的溶液中,各种含磷微粒的质量分数如图所示。
①电离平衡常数与化学平衡常数意义相同,写出
 第二步电离平衡常数表达式
第二步电离平衡常数表达式
(2)图中可推断
 溶液呈
溶液呈 溶液中各含磷微粒以及
溶液中各含磷微粒以及 按浓度由大到小的顺序排列
按浓度由大到小的顺序排列
您最近一年使用:0次
2021-04-02更新
|
224次组卷
|
4卷引用:上海市杨浦区2020-2021学年度高三下学期高中等级考模拟质量调研(3月)化学试题
上海市杨浦区2020-2021学年度高三下学期高中等级考模拟质量调研(3月)化学试题上海市杨浦区2021届高三二模化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)河北省张家口宣化一中2021届高三下学期阶段模拟(六)化学试题
名校
10 . 铋(83Bi)为第V A族元素,常见化合价为+3和+5。化合物NaBiO3为黄色固体,常温下微溶于水,在空气中逐渐分解产生Bi2O3、NaOH等物质。
(1)铋元素最外层电子分布在_____ 种能级中,共有_____ 种运动状态。
(2)铋酸钠NaBiO3中属于短周期元素的离子半径大小关系为_________ 。
(3)元素Na、Bi、O的金属性依次减弱,非金属性依次增强,请列举判断依据:_______ 。
(4)铋酸钠NaBiO3在空气中分解所得到产物中,化学键类型是______ 。
A.金属键 B.离子键 C.极性键 D.非极性键
(5)将NaBiO3加入MnSO4和H2SO4的混合溶液里加热,发生如下反应:
[ ]NaBiO3+[ ]MnSO4+[ ]H2SO4→[ ]Na2SO4+[ ]Bi2(SO4)3+[ ]NaMnO4+[ ]H2O
①配平该化学方程式,将系数填写在对应位置上。
______ NaBiO3+______ MnSO4+______ H2SO4→______ Na2SO4+______ Bi2(SO4)3+______ NaMnO4+______ H2O
②若有2mol氧化剂在该反应中被还原,则生成的MnO 被还原为Mn2+时,能将
被还原为Mn2+时,能将____ mol HCl氧化成Cl2。
(6)写出NaBiO3固体溶于HCl时发生反应的离子方程式:_________ 。
(1)铋元素最外层电子分布在
(2)铋酸钠NaBiO3中属于短周期元素的离子半径大小关系为
(3)元素Na、Bi、O的金属性依次减弱,非金属性依次增强,请列举判断依据:
(4)铋酸钠NaBiO3在空气中分解所得到产物中,化学键类型是
A.金属键 B.离子键 C.极性键 D.非极性键
(5)将NaBiO3加入MnSO4和H2SO4的混合溶液里加热,发生如下反应:
[ ]NaBiO3+[ ]MnSO4+[ ]H2SO4→[ ]Na2SO4+[ ]Bi2(SO4)3+[ ]NaMnO4+[ ]H2O
①配平该化学方程式,将系数填写在对应位置上。
②若有2mol氧化剂在该反应中被还原,则生成的MnO
 被还原为Mn2+时,能将
被还原为Mn2+时,能将(6)写出NaBiO3固体溶于HCl时发生反应的离子方程式:
您最近一年使用:0次



