解题方法
1 . 下列化学用语表示正确的是
A. 分子的空间填充模型: 分子的空间填充模型: |
B.基态 的价层电子轨道表示式为: 的价层电子轨道表示式为: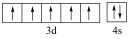 |
C. 分子中 分子中 键原子轨道电子云图: 键原子轨道电子云图: |
D.氯化铵的电子式: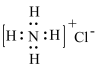 |
您最近一年使用:0次
2 . 硒化锌是一种重要的半导体材料,图甲为其晶胞结构,图乙为晶胞的俯视图。已知a点的坐标(0,0,0),b点的坐标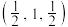 。下列说法正确的是
。下列说法正确的是
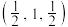 。下列说法正确的是
。下列说法正确的是
A. 的配位数为8 的配位数为8 | B.基态Se核外有34种不同空间运动状态的电子 |
C.晶胞中d点原子分数坐标为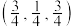 | D.若 换为 换为 ,则晶胞棱长保持不变 ,则晶胞棱长保持不变 |
您最近一年使用:0次
2023-12-26更新
|
631次组卷
|
4卷引用:湖南省衡阳市第八中学2023-2024学年高三上学期1月月考化学
湖南省衡阳市第八中学2023-2024学年高三上学期1月月考化学湖北省武汉市华中师范大学第一附属中学2023-2024学年高三上学期11月期中考试化学试题(已下线)微题型02 晶体结构及相关计算-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)重庆十八中两江实验中学校2023-2024学年高三下学期一诊模拟检测化学试题
名校
3 . 原子序数依次增大的5种短周期元素V、W、X、Y、Z形成的一种化合物的结构如图所示,该物质是生产药物诺氟沙星的中间体,也是制取农药的中间体。下列说法正确的是
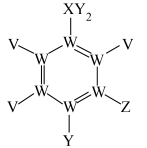

A.化合物VWX的电子式为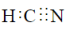 |
| B.基态Y原子核外电子具有5种不同的空间运动状态 |
C.沸点: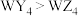 |
D.分子中的键角: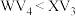 |
您最近一年使用:0次
2023-12-21更新
|
561次组卷
|
3卷引用:河北省沧州市部分学校2023-2024学年高三上学期12月联考化学试题
4 . 玻尔理论、量子力学理论都是对核外电子运动的描述方法,根据对它们的理解,下列叙述中正确的是
| A.因为s轨道的形状是球形的,所以s电子做的是圆周运动 |
B.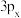 、 、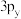 、 、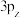 的轨道相互垂直,能量不同 的轨道相互垂直,能量不同 |
| C.各原子能级之间的能量差不一致,这是量子力学中原子光谱分析的理论基础 |
| D.同一能层的p轨道电子能量不一定高于s轨道电子能量 |
您最近一年使用:0次
2023-12-15更新
|
0次组卷
|
3卷引用:河北省保定市高碑店市崇德实验中学2023-2024学年高三上学期1月考试化学试题
解题方法
5 . 下列化学用语或图示表达正确的是
A. 的电子式为 的电子式为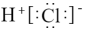 |
B. 的VSEPR模型: 的VSEPR模型: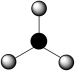 |
C.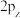 电子云轮廓图为: 电子云轮廓图为: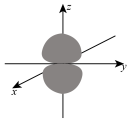 |
D.基态 的简化电子排布式: 的简化电子排布式: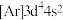 |
您最近一年使用:0次
名校
解题方法
6 . 下列图示正确的是
A. 的VSEPR模型: 的VSEPR模型: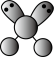 |
B.基态 价层电子的轨道表示式: 价层电子的轨道表示式: |
C.3p电子的电子云轮廓图: |
D. 的结构示意图: 的结构示意图: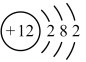 |
您最近一年使用:0次
7 . 按要求回答下列问题。
(1)基态硅原子核外电子的运动状态有___________ 种,价层电子轨道表示式为___________ 。
(2)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
(3)①钴位于元素周期表中___________ (填“s”、“p”、“d”或“ds”)区,与钴位于同一周期且含有相同未成对电子数的元素有___________ 种。
②钴元素可形成配合物[Co(NH3)6]Cl3,1mol该配合物含有σ键的数目为___________ 。该配合物中存在的化学键有___________ (填字母)。
A.离子键 B.极性键 C.非极性键 D.氢键 E.配位键
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
比较两元素的 、
、 可知,气态Mn2+再失去1个电子比气态
可知,气态Mn2+再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是___________ 。
(5)第四周期主族元素中,第一电离能介于Ga、As之间的元素有___________ 种。
(6)氯化铝熔点为194℃,会升华,熔融态不易导电。实验测得气态氯化铝分子组成为Al2Cl6,其结构式为___________ (已知Al2Cl6中原子均满足8e-稳定结构)。
(1)基态硅原子核外电子的运动状态有
(2)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
| A.1s22s22p43s1 | B.1s22s22p43d2 | C.1s22s22p5 | D.1s22s22p6 |
②钴元素可形成配合物[Co(NH3)6]Cl3,1mol该配合物含有σ键的数目为
A.离子键 B.极性键 C.非极性键 D.氢键 E.配位键
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
电离能/ | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
 、
、 可知,气态Mn2+再失去1个电子比气态
可知,气态Mn2+再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是(5)第四周期主族元素中,第一电离能介于Ga、As之间的元素有
(6)氯化铝熔点为194℃,会升华,熔融态不易导电。实验测得气态氯化铝分子组成为Al2Cl6,其结构式为
您最近一年使用:0次
名校
解题方法
8 . 下列说法正确的是
A.基态Be原子最外层电子的电子云轮廓图为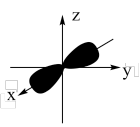 |
| B.基态Br原子的简化电子排布式为[Ar]4s24p5 |
| C.基态铝原子核外有5种能量不同的电子 |
| D.白磷分子空间构型为正四面体形,键角为109°28′ |
您最近一年使用:0次
名校
9 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。①~⑥表示元素在周期表中的位置,回答下列问题。
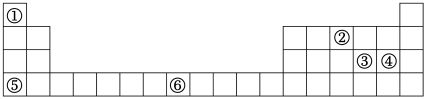
(1)①和④形成的化合物的化学式为_______ 。
(2)②的基态原子的轨道表示式为_______ ,其电子占据的最高能级的电子云轮廓是_______ 。
(3)⑤的基态原子占据的最高能层的符号是_______ ,其基态正一价离子占据的最高能级共有_______ 个原子轨道。
(4)⑥的基态正三价离子的价层电子排布式为_______ 。
(5)下列说法不正确 的是_______ 。
a.②的2px、2py、2pZ轨道互相垂直,但能量相等
b.④的p能级能量一定比s能级的能量高
c.⑥的2s、3s、4s能级的轨道数依次增多
(6)③和⑤形成的化合物的水溶液pH>7,结合离子方程式解释原因_______ 。

(1)①和④形成的化合物的化学式为
(2)②的基态原子的轨道表示式为
(3)⑤的基态原子占据的最高能层的符号是
(4)⑥的基态正三价离子的价层电子排布式为
(5)下列说法
a.②的2px、2py、2pZ轨道互相垂直,但能量相等
b.④的p能级能量一定比s能级的能量高
c.⑥的2s、3s、4s能级的轨道数依次增多
(6)③和⑤形成的化合物的水溶液pH>7,结合离子方程式解释原因
您最近一年使用:0次
名校
解题方法
10 . 下列化学用语或图示表达正确的是
A.CO2的电子式: | B.NH3的VSEPR模型为  |
C.由Na和Cl形成离子键的过程: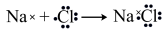 | D.2pz电子云图为  |
您最近一年使用:0次



