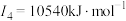元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。①~⑥表示元素在周期表中的位置,回答下列问题。
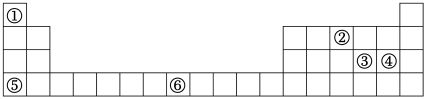
(1)①和④形成的化合物的化学式为_______ 。
(2)②的基态原子的轨道表示式为_______ ,其电子占据的最高能级的电子云轮廓是_______ 。
(3)⑤的基态原子占据的最高能层的符号是_______ ,其基态正一价离子占据的最高能级共有_______ 个原子轨道。
(4)⑥的基态正三价离子的价层电子排布式为_______ 。
(5)下列说法不正确 的是_______ 。
a.②的2px、2py、2pZ轨道互相垂直,但能量相等
b.④的p能级能量一定比s能级的能量高
c.⑥的2s、3s、4s能级的轨道数依次增多
(6)③和⑤形成的化合物的水溶液pH>7,结合离子方程式解释原因_______ 。

(1)①和④形成的化合物的化学式为
(2)②的基态原子的轨道表示式为
(3)⑤的基态原子占据的最高能层的符号是
(4)⑥的基态正三价离子的价层电子排布式为
(5)下列说法
a.②的2px、2py、2pZ轨道互相垂直,但能量相等
b.④的p能级能量一定比s能级的能量高
c.⑥的2s、3s、4s能级的轨道数依次增多
(6)③和⑤形成的化合物的水溶液pH>7,结合离子方程式解释原因
23-24高三上·北京房山·阶段练习 查看更多[2]
更新时间:2023-11-02 14:33:20
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】复分解反应是中学化学中常见的一种反应类型。
(1)已知在常温下测得浓度均为0.1 mol·L-1的下列6种溶液的pH值:
复分解存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3 = 2CH3COONa+CO2↑+H2O 若换个角度看,它同时揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该规律,请判断下列反应不能 成立的是___________(填编号)。
(2)根据前述信息判断,常温下,浓度均为0.05 mol·L-1的下列5种物质的溶液中,pH最小的是_________ (填编号),其pH值为_______ (填数值);pH最大的是________ (填编号)。
①HCN ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
(3)一些复分解反应的发生还遵循其它的规律。下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性钠溶液
②侯氏制碱法中,向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打晶体
请根据上述反应,总结出复分解反应发生的另一规律:_____________________ 。
(4)根据(3)中结论,现将KI溶液和AgCl固体混合搅拌,则可能会观察到的现象是____________________ ,反应的离子方程式为____________________________ 。
(1)已知在常温下测得浓度均为0.1 mol·L-1的下列6种溶液的pH值:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
复分解存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3 = 2CH3COONa+CO2↑+H2O 若换个角度看,它同时揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该规律,请判断下列反应
| A.CO2+H2O +2NaClO = Na2CO3+2HClO |
| B.CO2+H2O +NaClO = NaHCO3+HClO |
| C.CO2 +H2O +C6H5ONa→NaHCO3+C6H5OH |
| D.CO2 +H2O +2C6H5ONa→Na2CO3+2C6H5OH |
| E.Na2CO3+C6H5OH→NaHCO3+C6H5ONa |
| F.CH3COOH+NaCN = CH3COONa+HCN |
①HCN ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
(3)一些复分解反应的发生还遵循其它的规律。下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性钠溶液
②侯氏制碱法中,向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打晶体
请根据上述反应,总结出复分解反应发生的另一规律:
(4)根据(3)中结论,现将KI溶液和AgCl固体混合搅拌,则可能会观察到的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】磁选后的炼铁高钛炉渣,主要成分有 、
、 、
、 、MgO、CaO以及少量的
、MgO、CaO以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
已知:①“焙烧”中, 、
、 几乎不发生反应,
几乎不发生反应, 、MgO、CaO、
、MgO、CaO、 转化为相应的硫酸盐;②
转化为相应的硫酸盐;② 。回答下列问题:
。回答下列问题:
(1)为了加快“焙烧”速率,可采用的物理方法为______ (填一种即可)。
(2) “焙烧”时,转化为
“焙烧”时,转化为 ;在
;在 的
的 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为______ (填离子符号)。
(3)“水浸”后的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,最先析出的离子为______ (填离子符号)。
(4)水浸渣在160℃“酸溶”,最适合的加热方式为______ (填“水浴”或“油浴”)加热。
(5)“酸溶”后,将溶液适当稀释并加热, 水解析出
水解析出 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为______ 。
 、
、 、
、 、MgO、CaO以及少量的
、MgO、CaO以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。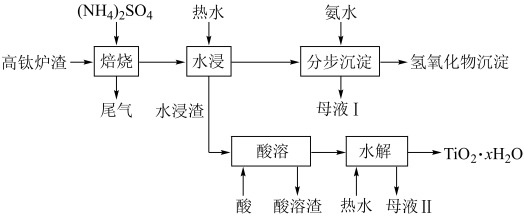
金属离子 |
|
|
|
|
开始沉淀( | 1.5 | 3.4 | 8.9 | 12.0 |
沉淀完全( | 2.8 | 4.7 | 10.9 | 13.8 |
 、
、 几乎不发生反应,
几乎不发生反应, 、MgO、CaO、
、MgO、CaO、 转化为相应的硫酸盐;②
转化为相应的硫酸盐;② 。回答下列问题:
。回答下列问题:(1)为了加快“焙烧”速率,可采用的物理方法为
(2)
 “焙烧”时,转化为
“焙烧”时,转化为 ;在
;在 的
的 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为(3)“水浸”后的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,最先析出的离子为
(4)水浸渣在160℃“酸溶”,最适合的加热方式为
(5)“酸溶”后,将溶液适当稀释并加热,
 水解析出
水解析出 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】亚磷酸( )是二元酸,与足量
)是二元酸,与足量 溶液反应生成
溶液反应生成 。
。
(1) 水解可得到亚磷酸的化学方程式为
水解可得到亚磷酸的化学方程式为___________
(2) 溶液中存在电离平衡:
溶液中存在电离平衡: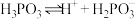
①某温度下, 的
的 溶液
溶液 ,即溶液中
,即溶液中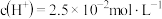 。求该温度下上述电离平衡的平衡常数
。求该温度下上述电离平衡的平衡常数
___________ 。 ( 的第二步电离忽略不计,结果保留两位有效数字。)
的第二步电离忽略不计,结果保留两位有效数字。)
②根据 的性质可推测
的性质可推测 稀溶液的
稀溶液的
___________ 7(填“>”、“=”或“<”)。
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式为___________ 。
(4)电解 溶液也可得到亚磷酸,装置示意图如图:
溶液也可得到亚磷酸,装置示意图如图:
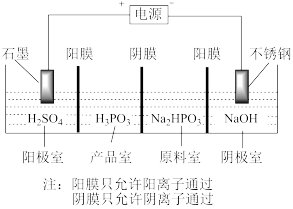
①阴极的电极反应式为___________ 。
②产品室中反应的离子方程式为___________ 。
 )是二元酸,与足量
)是二元酸,与足量 溶液反应生成
溶液反应生成 。
。(1)
 水解可得到亚磷酸的化学方程式为
水解可得到亚磷酸的化学方程式为(2)
 溶液中存在电离平衡:
溶液中存在电离平衡: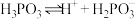
①某温度下,
 的
的 溶液
溶液 ,即溶液中
,即溶液中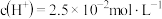 。求该温度下上述电离平衡的平衡常数
。求该温度下上述电离平衡的平衡常数
 的第二步电离忽略不计,结果保留两位有效数字。)
的第二步电离忽略不计,结果保留两位有效数字。)②根据
 的性质可推测
的性质可推测 稀溶液的
稀溶液的
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式为
(4)电解
 溶液也可得到亚磷酸,装置示意图如图:
溶液也可得到亚磷酸,装置示意图如图:
①阴极的电极反应式为
②产品室中反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】现有A、B、C、D、E、F、G、H八种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
A元素的核外电子数和电子层数相等,也是宇宙中含量最丰富的元素 |
B元素是形成化合物种类最多的元素 |
C元素基态原子的核外p电子数比s电子数少1 |
D元素基态原子的核外p轨道中有两个未成对电子 |
E元素的气态基态原子的第一至第四电离能分别如下:
|
F元素的主族序数与周期数的差为4 |
G元素是前四周期中电负性最小的元素 |
H元素位于元素周期表中的第八纵列 |
(1)C2A4的电子式为
(2)B元素的原子核外共有
(3)E元素基态原子的电离能I3远远大于I2,其原因是
(4)B、C、D、E四种元素的第一电离能由大到小的顺序是
(5)用惰性电极电解EF2的水溶液的离子方程式为
(6)H位于元素周期表中
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】太阳能的开发利用在新能源研究中占据重要地位,单品硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物的结构如图所示。请回答下列问题:_______ 区,最外层原子轨道呈_______ 形。
(2)基态二价铜离子的电子排布式为_______ ,已知高温下 比CuO更稳定,试从核外电子排布角度解释
比CuO更稳定,试从核外电子排布角度解释_______ 。
(3)在基态硼原子中,核外存在_______ 个运动状态不同的电子。
(4) 的价层电子排布图为
的价层电子排布图为_______ 。
(5)根据元素周期律,电负性O_______ Se(填“大于”“小于”或“等于”),N、O、Se三种元素中的第一电离能最大的为_______ 。
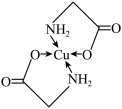
(2)基态二价铜离子的电子排布式为
 比CuO更稳定,试从核外电子排布角度解释
比CuO更稳定,试从核外电子排布角度解释(3)在基态硼原子中,核外存在
(4)
 的价层电子排布图为
的价层电子排布图为(5)根据元素周期律,电负性O
您最近一年使用:0次
【推荐3】磷酸亚铁锂( )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:
(1)基态Li原子核外电子所占据最高能级的电子云轮廓图为________ 形。
(2)Fe元素位于周期表_____ 周期_____ 族;原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为
表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为___________ 。
(3)基态Mn2+的价电子排布式为___________ ,锰的第三电离能高于铁的第三电离能,其原因是___________ 。
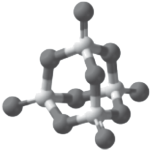
(4)P4S10的分子结构如图所示,其中含有________ 个六元环;______ g P4S10含有8molσ键。
 )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:(1)基态Li原子核外电子所占据最高能级的电子云轮廓图为
(2)Fe元素位于周期表
 和
和 表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为
表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为(3)基态Mn2+的价电子排布式为
(4)P4S10的分子结构如图所示,其中含有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】有X、Y、Z、Q、E、M、G原子序数依次递增的七种元素,除G元素外其余均为短周期主族元素。X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素原子的外围电子层排布式为nsnnpn+1,Q的基态原子核外成对电子数是成单电子数的3倍,E与Q同周期,M元素的第一电离能在同周期主族元素中从大到小排第三位,G原子最外电子层只有未成对电子,其内层所有轨道全部充满,但并不是第ⅠA族元素。回答下列问题:
(1)基态G原子的价电子排布式为____________ ,写出第三周期基态原子未成对电子数与G相同且电负性最大的元素是________ (填元素名称)。GQ受热分解生成G2Q和Q2,请从G的原子结构来说明GQ受热易分解的原因:__________________________________ 。
(2)Z、Q、M三种元素的第一电离能从大到小的顺序为_______________ (用元素符号表示)。
(3)M的氢化物(H2M)分子的立体构型为________ ,稳定性:H2Q____ H2M。 H2Q2中Q的杂化类型为________ ,为_______ 分子。
(4)Z、M、E所形成的简单离子的半径由大到小顺序为_________________ (用离子符号表示)。
(5)X、Y、Z、Q的电负性由大到小的顺序为________________________ (用元素符号表示)。
(6)G的氯化物与氨水反应可形成配合物[G(NH3)4]Cl2,1 mol该配合物中含有σ键的物质的量为________ mol。
(1)基态G原子的价电子排布式为
(2)Z、Q、M三种元素的第一电离能从大到小的顺序为
(3)M的氢化物(H2M)分子的立体构型为
(4)Z、M、E所形成的简单离子的半径由大到小顺序为
(5)X、Y、Z、Q的电负性由大到小的顺序为
(6)G的氯化物与氨水反应可形成配合物[G(NH3)4]Cl2,1 mol该配合物中含有σ键的物质的量为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】原子序数小于36的X、Y、Z、W、J、G六种元素,原子序数依次增大,其中X元素的原子在所有原子中半径最小,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,J元素原子核外的3p能级有两个电子,G元素原子核外有6个未成对电子。回答下列问题。
(1)写出G元素的基态原子的价电子排布式_____ ; 分子中σ键与π键数目之比为
分子中σ键与π键数目之比为_____ 。
(2)Y、Z、W三种元素第一电离能由小到大的顺序为_____ (用元素符号表示)。
(3) 在水中的溶解度较大,可能的原因有
在水中的溶解度较大,可能的原因有_____ 。
A.氨分子和水分子间可以形成氢键 B.NH3能与水反应 C.NH3与水都是极性分子
(4)判断J与W形成的化合物JW2是晶体还是非晶体,最科学的办法是_____ ;XYZ分子中Y原子轨道的杂化类型为_____ 。
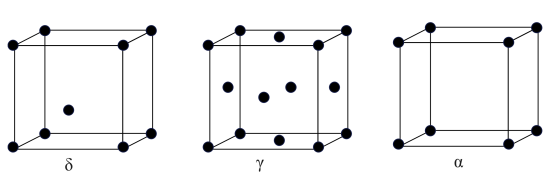
(5)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为_____ 。在γ晶胞结构中,设阿伏加德罗常数为NA,G原子半径为apm,G的相对原子质量为M,则该晶体的密度为_____ g/cm3.(用含NA、M和a的代数式表示)
(1)写出G元素的基态原子的价电子排布式
 分子中σ键与π键数目之比为
分子中σ键与π键数目之比为(2)Y、Z、W三种元素第一电离能由小到大的顺序为
(3)
 在水中的溶解度较大,可能的原因有
在水中的溶解度较大,可能的原因有A.氨分子和水分子间可以形成氢键 B.NH3能与水反应 C.NH3与水都是极性分子
(4)判断J与W形成的化合物JW2是晶体还是非晶体,最科学的办法是
(5)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】绿色化学在推动社会可持续发展中发挥着重要作用.某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了 的深度利用和
的深度利用和 内循环.工艺流程如下:
内循环.工艺流程如下:
(1)基态铬原子的电子排布式为____________ ,铬在元素周期表中的位置为____________ ;“高温连续氧化”过程中发生的氧化还原反应的化学方程式是____________ 。
(2)“固体Ⅲ”的主要成分是____________ (填化学式)。
(3)已知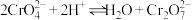 ,则“工序③”中通入
,则“工序③”中通入____________ (填“足量”或“少量”)的气体A更有利于得到重铬酸盐;气体A的固态属于____________ 晶体;流程中可以循环使用的物质除气体A外还有____________ (填化学式)。
(4)“工序④”中发生反应的离子方程式为____________ ;常温常压下,“工序④”的溶液中铝元素恰好完全转化为沉淀的 为8.37,则
为8.37,则

____________ 。(通常认为溶液中离子浓度小于 时沉淀完全)
时沉淀完全)
 的深度利用和
的深度利用和 内循环.工艺流程如下:
内循环.工艺流程如下: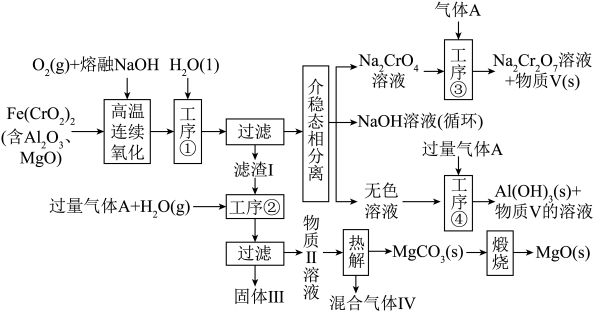
(1)基态铬原子的电子排布式为
(2)“固体Ⅲ”的主要成分是
(3)已知
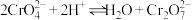 ,则“工序③”中通入
,则“工序③”中通入(4)“工序④”中发生反应的离子方程式为
 为8.37,则
为8.37,则

 时沉淀完全)
时沉淀完全)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】中医药学认为,雄黄(As4S4),外用可以治疗疥癣恶疮、蛇虫咬伤等;微量内服,可治惊痫、疮毒等症。雄黄遇热易氧化为As2O3(俗称砒霜),虽在古时常用做毒药,但科学家却发现它对治疗白血病有明显的作用。砷的其它化合物也在研究和生产中有着许多重要用途。____ ,核外电子占据的最高能级的电子云轮廓图形状为____ 。
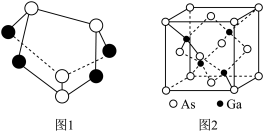
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为_____ 。
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括____ ;AsO43-的空间构型为_____ 。
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是____ ;砷化镓密度为 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为_____ 。
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是
 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知X、Y、Z、W四种元素是原子序数依次增大的短周期主族元素,Z原子最外层电子数是次外层电子数的3倍,X、W同主族,Y、Z为同周期的相邻元素;W原子的质子数等于Y、Z原子最外层电子数之和,Y与X形成的分子中有3个共价键,回答下列问题:
(1)Y、Z两种元素中第一电离能大的是___________ (填元素符号)。
(2)由X、Y、Z所形成的常见离子化合物是___________ (写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为___________ ;X与W形成的化合物与水反应时,水是___________ (填“氧化剂”或“还原剂”)。
(3)用电子式表示W与Z形成 化合物的过程:
化合物的过程:___________ 。
(4)Q与Z同主族,位于第4周期,其原子的价电子轨道表示式为___________ 。
(1)Y、Z两种元素中第一电离能大的是
(2)由X、Y、Z所形成的常见离子化合物是
(3)用电子式表示W与Z形成
 化合物的过程:
化合物的过程:(4)Q与Z同主族,位于第4周期,其原子的价电子轨道表示式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硒(Se)是一种有抗癌、抗氧化作用的元素,可形成多种化合物,含硒化合物在材料和药物等领域有重要应用。
(1)基态硒原子价电子轨道表达式为___________ 。
(2)硒所在的主族中,简单气态氢化物沸点最低的是___________ (填化学式)。
(3)硒、硅均能与氢元素形成气态氢化物,硅的氢化物中共用电子对偏向氢元素,而氢气与硒反应时单质硒是氧化剂,则电负性大小为Se___________ Si(填“>”或“<”)。
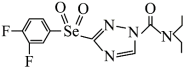
(4)某绿色农药的结构简式如图所示。C、N、O、F四种元素第一电离能由大到小的排列顺序为___________ ;该物质中,C原子的杂化轨道类型是___________ 。
(5)亚硒酸钠( )能消除加速人体衰老的活性氧,
)能消除加速人体衰老的活性氧, 的空间构型为
的空间构型为___________ ; 的键角
的键角___________ 气态分子 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是___________ 。
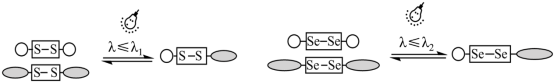
(6)二硫键与二硒键是重要的光响应动态共价键,其光响应原理可用下图表示。已知光的波长与其能量成反比,则图中实现光响应的波长
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(7)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
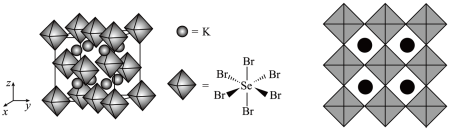
化合物X的晶体类型是___________ ,X的化学式为___________ 。
(1)基态硒原子价电子轨道表达式为
(2)硒所在的主族中,简单气态氢化物沸点最低的是
(3)硒、硅均能与氢元素形成气态氢化物,硅的氢化物中共用电子对偏向氢元素,而氢气与硒反应时单质硒是氧化剂,则电负性大小为Se
(4)某绿色农药的结构简式如图所示。C、N、O、F四种元素第一电离能由大到小的排列顺序为

(5)亚硒酸钠(
 )能消除加速人体衰老的活性氧,
)能消除加速人体衰老的活性氧, 的空间构型为
的空间构型为 的键角
的键角 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是(6)二硫键与二硒键是重要的光响应动态共价键,其光响应原理可用下图表示。已知光的波长与其能量成反比,则图中实现光响应的波长

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(7)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

化合物X的晶体类型是
您最近一年使用:0次




 )的pH
)的pH )的pH
)的pH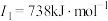 ,
,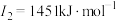 ,
,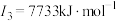 ,
,