1 . 回答下列问题。
(1)镍元素基态原子的核外电子排布式为___________ ,3d能级上的未成对电子数为___________ 。
(2)基态Ge原子的价层电子排布式为___________ ,有___________ 个未成对电子。
(3)Zn2+基态核外电子排布式为___________ 。
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态 14C原子中,核外存在___________ 对自旋相反的电子。
(5)基态Fe原子有___________ 个未成对电子。Fe3+的电子排布式为___________ 。
(1)镍元素基态原子的核外电子排布式为
(2)基态Ge原子的价层电子排布式为
(3)Zn2+基态核外电子排布式为
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(5)基态Fe原子有
您最近半年使用:0次
2 . 按要求回答下列问题:
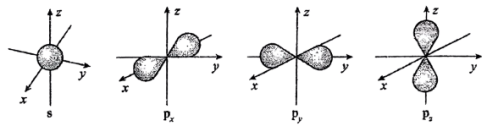
(1)如图是s能级和p能级的电子云轮廓图,试回答问题。______ 形,每个p能级有______ 个原子轨道。
(2)按要求作答:
①画出氯原子结构示意图______ ;
②写出基态O核外电子排布式为:______ ;
③写出基态N的原子轨道表示式:______ ;
(3)Sm的价层电子排布式为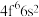 ,则
,则 价层电子排布式为
价层电子排布式为______ 。
(1)如图是s能级和p能级的电子云轮廓图,试回答问题。
(2)按要求作答:
①画出氯原子结构示意图
②写出基态O核外电子排布式为:
③写出基态N的原子轨道表示式:
(3)Sm的价层电子排布式为
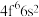 ,则
,则 价层电子排布式为
价层电子排布式为
您最近半年使用:0次
解题方法
3 . 下列描述原子结构的化学用语错误的是
A.氧原子核外能量最高的电子云的形状: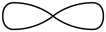 |
B. 的价层电子轨道表达式: 的价层电子轨道表达式: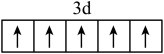 |
C.钛原子结构示意图为: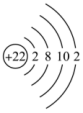 |
| D.基态铜原子的价层电子排布图:3d94s2 |
您最近半年使用:0次
解题方法
4 . 下列化学用语正确的是
| A.水晶的分子式:SiO2 |
B.Cl-Cl的 键电子云图形: 键电子云图形: |
C.CO 的空间结构: 的空间结构: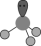 (正四面体形) (正四面体形) |
D.基态铜原子价电子的轨道表示式: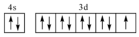 |
您最近半年使用:0次
解题方法
5 . 第三周期部分主族元素及 的氟化物的熔点如表所示,
的氟化物的熔点如表所示, 分子的空间结构为正八面体,结构如图所示。
分子的空间结构为正八面体,结构如图所示。
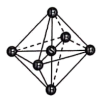
下列说法正确的是
 的氟化物的熔点如表所示,
的氟化物的熔点如表所示, 分子的空间结构为正八面体,结构如图所示。
分子的空间结构为正八面体,结构如图所示。
| 化合物 |  |  |  |  |
| 熔点/℃ | 993 | 1040 | -90 | -50.5 |
A. 为共价晶体 为共价晶体 | B.离子半径: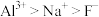 |
C.基态 原子核外电子运动状态有8种 原子核外电子运动状态有8种 | D. 的二氮代物 的二氮代物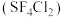 有2种 有2种 |
您最近半年使用:0次
解题方法
6 . 下列化学用语或表述正确的是
A.用电子式表示Na2S的形成: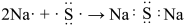 |
B.中子数为20的氯原子: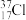 |
C.p轨道的电子云轮廓图: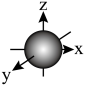 |
D.乙烯的空间填充模型: |
您最近半年使用:0次
名校
解题方法
7 . 运用物质结构与性质的相关知识,回答下列问题:
(1) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是_______ 。基态 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有_____ 个伸展方向,原子轨道呈______ 形。
(2) 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为________ , 价电子轨道表示式为
价电子轨道表示式为________ 。
(3) 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
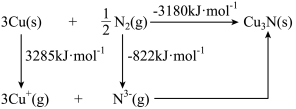
通过图中数据________ (填“能”或“不能”)计算出 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为________  。
。
(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。
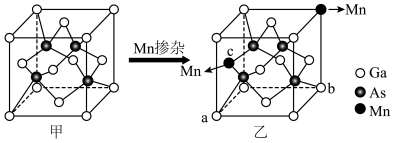
①GaAs晶胞中距离Ga原子最近As原子的个数为________ 。
②掺杂 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为________ (化为最简整数比)。
(1)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有(2)
 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为 价电子轨道表示式为
价电子轨道表示式为(3)
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
通过图中数据
 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为 。
。(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①GaAs晶胞中距离Ga原子最近As原子的个数为
②掺杂
 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为
您最近半年使用:0次
解题方法
8 . 已知:NHCl2在水中产生几种化合物,其中一种物质M具有强氧化性且常用于自来水的消毒。下列有关说法错误的是
| A.基态N原子核外有3种不同能量的电子 |
| B.化合物M是次氯酸 |
| C.M分子的空间构型是直线形 |
| D.NHCl2分子中氮原子的杂化类型为sp3 |
您最近半年使用:0次
9 . 下列化学用语错误的是
A.中子数为10的氧原子: |
B.Na2O2的电子式: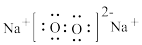 |
| C.次氯酸的结构式:H—Cl—O |
D.基态N原子2py轨道的电子云轮廓图: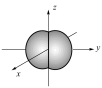 |
您最近半年使用:0次
10 . 回答下列问题
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为___________ ,电负性O___________ F;其中氧原子的杂化方式为___________ 。
(2)X、Y、Z为短周期元素且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成NH3;Z基态原子的M层与K层电子数相等。 空间结构是
空间结构是___________ ;X与Z形成化合物中含有的化学键是___________ 。
(3) 的空间结构为
的空间结构为___________ 。(用文字描述,下同): 的空间结构是
的空间结构是___________ 。
(4)在BF3分子中: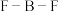 的键角是
的键角是___________ ,B原子的杂化轨道类型为___________ ,BF3和过量NaF作用可生成NaBF4, 的空间结构为
的空间结构为___________ 。
(5)钠在火焰上灼烧产生的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(6)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为___________ ;其中π键与σ键的个数比为___________ 。
(7)基态S原子价电子排布式___________ ;S原子的核外电子运动状态有___________ 种,空间运动状态有___________ 种:能量最高的轨道的电子云的形状是___________ 。
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为
(2)X、Y、Z为短周期元素且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成NH3;Z基态原子的M层与K层电子数相等。
 空间结构是
空间结构是(3)
 的空间结构为
的空间结构为 的空间结构是
的空间结构是(4)在BF3分子中:
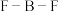 的键角是
的键角是 的空间结构为
的空间结构为(5)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(6)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为
(7)基态S原子价电子排布式
您最近半年使用:0次
2024-02-22更新
|
212次组卷
|
2卷引用:天津市耀华中学2023-2024学年高二上学期1月期末化学试题



