名校
解题方法
1 . 第四周期中的18 种元素具有重要的用途,在现代工业中备受青睐。
(1)其中,未成对电子数最多的元素名称为_______ ,该元素的基态原子中,电子占据的最高能层具有的原子轨道数为_______ 。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是_______ 。
(3)AsH3 中心原子杂化的类型为_______ ,分子构型为_______
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为_______ 。
(5)与CN-互为等电子体的一种分子为_______ (填化学式);1.5mol [Fe(CN)6]3-中含有键的数目为_______
(1)其中,未成对电子数最多的元素名称为
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是
(3)AsH3 中心原子杂化的类型为
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为
(5)与CN-互为等电子体的一种分子为
您最近半年使用:0次
2021-05-29更新
|
112次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2020-2021学年高二下学期期中考试化学试题
名校
解题方法
2 . 氮、磷、砷、铁等元素及其化合物在现代农业、科技、国防建设中有着许多独特的用途。
(1)基态砷原子中核外电子占据最高能层的符号为__ ,该能层的原子轨道数有__ 个。
(2)氮的一种氢化物N2H4是一种良好的火箭发射燃料,传统制备肼的方法是:NaClO+2NH3=N2H4+NaCl+H2O,又知肼的熔点、沸点分别为1.4℃、113.5℃,氨气的熔点、沸点分别为-77.7℃、-33.5℃。
①N2H4中氮原子的杂化轨道类型为__ 杂化,基态N原子电子占据最高能级的电子云轮廓图为___ 形。
②肼与氨气熔点、沸点差异最主要的原因是__ 。
(3)氨分子是一种常见配体,配离子[Co(NH3)6]3+中存在的化学键有__ (填序号)。
A.离子键 B.极性键 C.配位键 D.氢键
(1)基态砷原子中核外电子占据最高能层的符号为
(2)氮的一种氢化物N2H4是一种良好的火箭发射燃料,传统制备肼的方法是:NaClO+2NH3=N2H4+NaCl+H2O,又知肼的熔点、沸点分别为1.4℃、113.5℃,氨气的熔点、沸点分别为-77.7℃、-33.5℃。
①N2H4中氮原子的杂化轨道类型为
②肼与氨气熔点、沸点差异最主要的原因是
(3)氨分子是一种常见配体,配离子[Co(NH3)6]3+中存在的化学键有
A.离子键 B.极性键 C.配位键 D.氢键
您最近半年使用:0次
解题方法
3 . 由N、P、Ti等元素组成的新型材料有着广泛的用途,请回答下列问题。
(1)钛元素基态原子未成对电子数为__ 个,能量最高的电子占据的能级符号为___ 。
(2)磷的一种同素异形体—白磷(P4)的立体构型为__ ,推测其在CS2中的溶解度__ (填“大于”或“小于”)在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因:__ 。
(4)工业上制金属钛采用金属还原四氯化钛。先将TiO2(或天然的金红石)和足量炭粉混合加热至1000~1100K,进行氯化处理,生成TiCl4。写出生成TiCl4的化学反应方程式:___ 。
(5)有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为__ ,已知晶体的密度为ρg·cm-3,阿伏加 德罗常数为NA,则晶胞边长为__ cm(用含ρ、NA的式子表示)。

(1)钛元素基态原子未成对电子数为
(2)磷的一种同素异形体—白磷(P4)的立体构型为
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因:
(4)工业上制金属钛采用金属还原四氯化钛。先将TiO2(或天然的金红石)和足量炭粉混合加热至1000~1100K,进行氯化处理,生成TiCl4。写出生成TiCl4的化学反应方程式:
(5)有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为

您最近半年使用:0次
4 . 硼(B)及其化合物是用途广泛的化工原料,硼可与多种元素形成化合物。
(1)B的价电子轨道表示式为________ 。
(2)BF3与NH3可以通过配位键形成NH3·BF3。
① 基态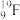 原子的核外电子有
原子的核外电子有________ 种不同的运动状态
② NH3 的键角________ CH4的键角(填“大于”、“小于”或“等于”)。BF3为________ 分子(填“极性”或“非极性”)。
③ 在NH3·BF3所形成的配位键中,________ 原子提供空轨道。
(3)氮化硼(BN)晶体有多种结构。六方氮化硼与石墨相似,具有层状结构;立方氮化硼与金刚石相似,具有空间网状结构。它们的晶体结构如下图所示。
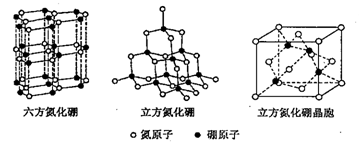
① 六方氮化硼和立方氮化硼中,B原子的杂化方式分别为_______ 、_______ 。
② 六方氮化硼能像石墨一样做润滑剂,原因是_______ ;但它不能像石墨一样导电,可能的原因是_______ .
③ 已知立方氮化硼的晶胞参数(即晶胞的边长)为acm,则立方氮化硼的密度为_______ g/cm3(只要求列算式,不必计算出结果,阿伏伽德罗常数为NA)。
(1)B的价电子轨道表示式为
(2)BF3与NH3可以通过配位键形成NH3·BF3。
① 基态
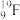 原子的核外电子有
原子的核外电子有② NH3 的键角
③ 在NH3·BF3所形成的配位键中,
(3)氮化硼(BN)晶体有多种结构。六方氮化硼与石墨相似,具有层状结构;立方氮化硼与金刚石相似,具有空间网状结构。它们的晶体结构如下图所示。

① 六方氮化硼和立方氮化硼中,B原子的杂化方式分别为
② 六方氮化硼能像石墨一样做润滑剂,原因是
③ 已知立方氮化硼的晶胞参数(即晶胞的边长)为acm,则立方氮化硼的密度为
您最近半年使用:0次



