名校
1 . 硅是典型的半导体元素,在电子、材料等领域应用广泛。请回答下列问题:
(1)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为_______ ;基态C原子核外电子的空间运动状态有_______ 种。
②基态Si原子的核外电子占据_______ 个能层,_______ 个能级。
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的相互作用是_______ 。
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原⼦结构⻆度分析,原因是_______ 。
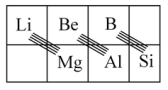
(2)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式__________ 。
(1)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为
②基态Si原子的核外电子占据
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原⼦结构⻆度分析,原因是
(2)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式

您最近一年使用:0次
名校
解题方法
2 . 过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是_______ 。
A.价层原子轨道处于半充满时体系总能量低,核外电子排布应为
B.4s是电子能量较高,一定是在比3d电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子分别是
中提供电子对形成配位键的原子分别是_______ (填元素符号),中心离子的配位数为_______ 。
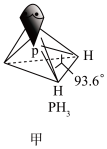
(3)PH3的空间结构和相应的键角如图甲所示。_______ ,NH3的沸点比PH3的沸点_______ ,原因是_______ 。
(4)在金属材料中添加 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图乙所示,其中处于顶角位置的是
具有体心四方结构,如图乙所示,其中处于顶角位置的是_______ 原子(填元素符号)。
(1)对于基态Cr原子,下列叙述正确的是
A.价层原子轨道处于半充满时体系总能量低,核外电子排布应为

B.4s是电子能量较高,一定是在比3d电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子分别是
中提供电子对形成配位键的原子分别是(3)PH3的空间结构和相应的键角如图甲所示。
(4)在金属材料中添加
 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图乙所示,其中处于顶角位置的是
具有体心四方结构,如图乙所示,其中处于顶角位置的是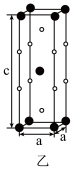
您最近一年使用:0次
名校
3 . A、B、C、D、E为短周期元素且它们的原子序数依次增大,A的核外电子总数与其周期序数相同;其中D原子的L电子层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L电子层中未成对电子数与D相同,但还有空轨道;D与E同族。请回答下列问题:
(1)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为___________ ,其中心原子的杂化方式为___________ ;A分别与B、C、D形成的共价化合物中既含有极性共价键,又含有非极性共价键的化合物是___________ (填化学式,任意写出三种)。
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离子是___________ (填化学式,下同);酸根离子呈三角锥形结构的是___________ 。
(3) 分子的空间结构为
分子的空间结构为___________ ;根据电子云重叠方式的不同,该分子中共价键的类型为___________ 。
(4)B的一种氢化物相对分子质量是26,其分子中 键和
键和 键的数目之比为
键的数目之比为___________ 。
(1)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离子是
(3)
 分子的空间结构为
分子的空间结构为(4)B的一种氢化物相对分子质量是26,其分子中
 键和
键和 键的数目之比为
键的数目之比为
您最近一年使用:0次
2021-02-06更新
|
447次组卷
|
3卷引用:黑龙江省佳木斯市第十二中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
4 . 2019年8月13日中国科学家合成了首例缺陷诱导的晶态无机硼酸盐单一组分白光材料Ba2[Sn(OH)6][B(OH)4]2并获得了该化合物的LED器件,该研究结果有望为白光发射的设计和应用提供一个新的有效策略。
(1)基态Sn原子价电子排布式为_______ ,基态氧原子的价层电子排布式不能表示为2s22px22py2,因为这违背了_______ 原理(规则)。
(2)[B(OH)4]-中硼原子的杂化轨道类型为______ ,氧原子的价层电子对互斥模型是_____ 。[Sn(OH)6] 2-中,Sn与O之间的化学键不可能是_____ 。
a.π键 b.σ键 c.配位键 d.极性键
(3)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,写出氨硼烷的结构式_______ ,并写出一种与氨硼烷互为等电子体的分子_______ (填化学式)。
(4)已知硼酸(H3BO3)为一元弱酸,写出硼酸表现一元弱酸性的电离方程式________ 。
(5)碳酸钡、碳酸镁分解得到的金属氧化物中,熔点较高的是_______ (填化学式),其原因是___________ 。
(6)超高热导率半导体材料——砷化硼(BAs)的晶胞结构如图所示,则2号砷原子的坐标为______ 。已知阿伏加 德罗常数的值为NA,若晶胞中As原子到B原子最近距离为a pm,则该晶体的密度为______ g·cm-3(列出含a、NA的计算式即可)。

(1)基态Sn原子价电子排布式为
(2)[B(OH)4]-中硼原子的杂化轨道类型为
a.π键 b.σ键 c.配位键 d.极性键
(3)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,写出氨硼烷的结构式
(4)已知硼酸(H3BO3)为一元弱酸,写出硼酸表现一元弱酸性的电离方程式
(5)碳酸钡、碳酸镁分解得到的金属氧化物中,熔点较高的是
(6)超高热导率半导体材料——砷化硼(BAs)的晶胞结构如图所示,则2号砷原子的坐标为

您最近一年使用:0次



