解题方法
1 . 完成下列问题
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利原理?_______ ;哪些违反了洪特规则?_______ 。
① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤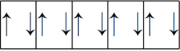 ;⑥
;⑥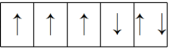
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为_______ ;其最高价氧化物对应水化物的化学式是_______ 。
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列。轨道能量由低到高排列顺序是_______ (填序号)。
①2s ②3d ③4s ④3s ⑤4p ⑥3p
(4)在HX(X为F、Cl、Br、I)分子中,键长最短的是_______ ;
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利原理?
①
 ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列。轨道能量由低到高排列顺序是
①2s ②3d ③4s ④3s ⑤4p ⑥3p
(4)在HX(X为F、Cl、Br、I)分子中,键长最短的是
您最近一年使用:0次
名校
解题方法
2 . 氮原子可以形成σ键、π键、大π键和配位键,成键的多样性使其形成了多种具有独特组成的物质。回答下列问题:
(1)基态氮原子价电子排布图不是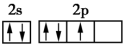 ,是因为该排布方式违背了
,是因为该排布方式违背了_______ 。
(2)肼(H2N−NH2)的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是_______ 。
(3)正硝酸钠(Na3NO4)为白色晶体,是一种重要的化工原料。
①Na3NO4阴离子的中心原子杂化方式为_______ 。
②在573K条件下,实验室中用NaNO3和Na2O在银皿中反应制得Na3NO4,Na2O的立方晶胞如图所示:
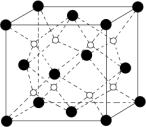
如图中“●”表示O2−, Na2O晶胞边长为apm,则晶胞密度_______ g•cm−3(列出计算式即可,Na相对原子质量:23NA为阿伏加德罗常数的值)。
(1)基态氮原子价电子排布图不是
 ,是因为该排布方式违背了
,是因为该排布方式违背了(2)肼(H2N−NH2)的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是
(3)正硝酸钠(Na3NO4)为白色晶体,是一种重要的化工原料。
①Na3NO4阴离子的中心原子杂化方式为
②在573K条件下,实验室中用NaNO3和Na2O在银皿中反应制得Na3NO4,Na2O的立方晶胞如图所示:

如图中“●”表示O2−, Na2O晶胞边长为apm,则晶胞密度
您最近一年使用:0次
名校
3 . 硅是典型的半导体元素,在电子、材料等领域应用广泛。请回答下列问题:
(1)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为_______ ;基态C原子核外电子的空间运动状态有_______ 种。
②基态Si原子的核外电子占据_______ 个能层,_______ 个能级。
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的相互作用是_______ 。
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原⼦结构⻆度分析,原因是_______ 。
(2)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式__________ 。
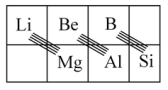
(1)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为
②基态Si原子的核外电子占据
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原⼦结构⻆度分析,原因是
(2)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式

您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的是
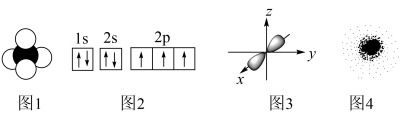

| A.图1为CH4分子的球棍模型 |
| B.图2为氮原子的电子轨道表示式 |
| C.图3为铍原子最外层的电子云图 |
| D.图4为H原子的电子云图,由图可见H原子核外靠近核运动的电子多 |
您最近一年使用:0次
5 . 下列说法不正确的是
| A.ls与2s的原子轨道都呈球形 |
| B.3p与2p的原子轨道都是纺缍形 |
| C.同一能层中,p电子能量比s电子能量大 |
| D.电子云表示的是电子在原子核外空间的运动轨道 |
您最近一年使用:0次
2022-06-01更新
|
100次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
6 . 在核电荷数为25的Mn的价层电子排布中,处于基态的是
A.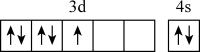 | B.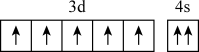 |
C.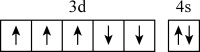 | D.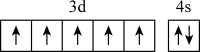 |
您最近一年使用:0次
2022-05-20更新
|
214次组卷
|
2卷引用:黑龙江省哈尔滨市第三十二中学校2021-2022学年高二下学期期中考试化学试题
7 . 正确掌握化学用语是学好化学的基础。下列化学用语正确的是
A.Cr原子的价电子排布图: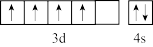 |
B.硝基苯的结构简式为: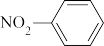 |
C.NaH的电子式: |
D.2-甲基戊烷的键线式: |
您最近一年使用:0次
8 . 下列有关氮原子的轨道中违反洪特规则的是
A.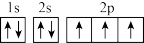 | B. | C.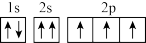 | D.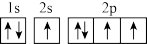 |
您最近一年使用:0次
2022-04-04更新
|
334次组卷
|
4卷引用:黑龙江省绥化市绥棱县第一中学2022-2023学年高二上学期期中考试化学试题
21-22高二·全国·课后作业
名校
解题方法
9 . 下列原子的轨道表示式正确的是
A. | B. |
C.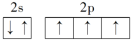 | D.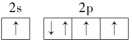 |
您最近一年使用:0次
2021-12-25更新
|
801次组卷
|
11卷引用:黑龙江省大庆市第五十六中学2021-2022学年高二学年下学期期中考试化学试题
黑龙江省大庆市第五十六中学2021-2022学年高二学年下学期期中考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2021-2022学年高二下学期开学考试化学试题(已下线)1.1.3 电子云与原子轨道 泡利原理与洪特规则 能量最低原理-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)1.1.3 电子云与原子轨道 泡利原理与洪特规则 能量最低原理(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)云南省昭通市第一中学2021-2022学年高二下学期开学考试化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高二3月月考化学试题广东省潮州湘桥区南春中学2021-2022学年高二下学期第一次月考化学试题北京教育学院附属中学2022-2023学高三上学期10月测试 化学试题吉林省吉林松花江中学2022-2023学年高二上学期1月期末考试化学试题江苏省苏州市南京航空航天大学苏州附属中学2023-2024学年高二下学期3月月考化学试题湖南省娄底市涟源市行知高级中学2023-2024学年高二上学期1月期末化学试题
9-10高二下·黑龙江·期末
名校
解题方法
10 . 下列说法中,正确的是
| A.处于最低能量的原子叫做基态原子 |
B. 表示 表示 能级有两个轨道 能级有两个轨道 |
| C.同一原子中,1s、2s、3s电子的能量逐渐减小 |
| D.2p、3p、4p能级的轨道数依次增多 |
您最近一年使用:0次
2021-12-03更新
|
1660次组卷
|
47卷引用:黑龙江省哈尔滨市阿城区第二中学2018-2019学年高二下学期期中考试化学试题
黑龙江省哈尔滨市阿城区第二中学2018-2019学年高二下学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高二下学期期中考试化学试题(已下线)09—10年哈三中高二下学期期末考试化学卷(已下线)2014-2015学年四川省邛崃市高二上学期半期考试化学试卷2015-2016学年河北邢台一中高二上学期期中测试化学试卷河南省郑州市八校2016-2017学年高二下学期期中联考化学试题黑龙江省齐齐哈尔市第八中学2017-2018学年高二3月月考化学试题【全国百强校】辽宁省鞍山市第一中学2017-2018学年高二下学期期中考试化学试题【全国百强校】辽宁省葫芦岛市第一高级中学2017-2018学年高二下学期期中考试化学试题黑龙江省鸡西市鸡东县第二中学2018-2019学年高二5月月考化学试题新疆兵团八师一四三团一中2018-2019学年高二下学期期中考试化学试题云南省玉溪市江川二中2019-2020学年高二上学期期中考试化学试题新疆昌吉市教育共同体2019-2020学年高二下学期期中考试化学试题福建省泉州市四校(晋江磁灶中学等)2019-2020学年高二下学期期中联考化学试题黑龙江省齐齐哈尔市第一中学2020-2021学年高二下学期4月月考化学试题甘肃省酒泉市青海油田第一中学2020-2021学年高二下学期期中考试化学试题新疆博尔塔拉蒙古自治州蒙古中学2020-2021学年高二下学期期中考试化学试题 福建省永春美岭中学2021-2022学年高二下学期期中测试化学试题广东省广州市白云中学2022-2023学年高二下学期期中考试化学试题黑龙江省齐齐哈尔市第八中学校2023-2024学年高二下学期三月月考化学试题(已下线)2011-2012学年陕西省宝鸡中学高二下学期期末考试化学试卷(已下线)2014学年高二鲁科版选修3化学规范训练 1章原子结构练习卷吉林省东北师范大学附属中学2017-2018学年高二上学期期末考试化学试题湖北省宜昌市第一中学2017-2018学年高二上学期期末考试化学试题河北省邢台市第一中学2017-2018学年高二下学期第一次月考化学试题贵州省习水县一中2018-2019学年高二上学期12月份月考化学试题新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题云南省昭通市绥江县二中2019-2020学年高二上学期期末考试化学试题安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题新疆维吾尔自治区喀什巴楚县第一中学2020-2021学年高二上学期第一次月考化学试题天津市滨海新区2020-2021学年高二上学期期末考试化学试题陕西省西安中学2020-2021学年高二上学期期末考试化学试题(已下线)第一单元 原子结构(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)(已下线)1.1 原子结构(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)福建省福州市福清西山学校2020-2021学年高二下学期3月月考化学试题人教2019选择性必修2第一章 原子结构与性质复习与提高(已下线)1.1.3 电子云与原子轨道 泡利原理与洪特规则 能量最低原理(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)山西省晋城市第一中学2021-2022学年高二上学期第五次调研化学试题湖北省黄冈市麻城市第二中学2021-2022学年高二下学期3月月考化学试题 新疆新源二中2021-2022学年高二下学期期末测试化学试题新疆生产建设兵团第六师芳草湖农场中学2021-2022学年高二上学期期末考试化学试题2019鲁科版高中化学选择性必修2第1章本章自我评价课后习题天津市南开大学附属中学2022-2023学年高二上学期期末考试化学试卷贵州省贵阳清镇北大培文学校2022-2023学年高二下学期3月月考化学试题甘肃省张掖市 高台县第一中学2022-2023学年高二下学期3月月考化学试题新疆博湖县奇石中学2022-2023学年高二下学期期末考试化学试题新疆喀什市2022-2023学年高二下学期普通高中期末质量监测化学试题



