解题方法
1 . 第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线图。请回答以下问题:
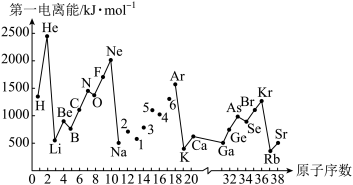
(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象____ 。
(2)从图分析可知,同一主族元素原子第一电离能I1变化规律____ 。
(3)图中5号元素在周期表中的位置是____ 、电子排布____ 。
(4)图中N元素比O元素第一电离能高的原因是____ 。
(5)C、H元素形成的化合物分子中共有14个电子,该分子中____ 个σ键,____ 个π键,中心原子杂化模式____ ,分子空间构型____ 。

(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象
(2)从图分析可知,同一主族元素原子第一电离能I1变化规律
(3)图中5号元素在周期表中的位置是
(4)图中N元素比O元素第一电离能高的原因是
(5)C、H元素形成的化合物分子中共有14个电子,该分子中
您最近一年使用:0次
名校
解题方法
2 . 已知A、B、C、D都是短周期元素,它们的原子半径大小顺序为B>C>D>A。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体。E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满。
试回答下列问题(用元素符号或化学式表示):
(1)基态B原子中,核外存在___________ 个未成对电子。
(2)基态E2+的核外电子排布式为___________ 。
(3)基态D原子的最高能层的电子排布图为___________
(4)M分子中B原子轨道的杂化类型为___________ 。
(5)B、C、D三种元素的第一电离能由小到大的顺序为___________ 。
试回答下列问题(用元素符号或化学式表示):
(1)基态B原子中,核外存在
(2)基态E2+的核外电子排布式为
(3)基态D原子的最高能层的电子排布图为
(4)M分子中B原子轨道的杂化类型为
(5)B、C、D三种元素的第一电离能由小到大的顺序为
您最近一年使用:0次
2021-10-26更新
|
290次组卷
|
5卷引用:四川省巴中市恩阳区2022-2023学年高二下学期4月期中考试化学试题
3 . 下图是元素周期表的简略框架图。

(1)请在上图所示的元素周期表中画出金属元素与非金属元素的分界线__ 。元素周期表的5个区中,不全是金属元素的区为__ 。
(2)根据氢元素最高正化合价与最低负化合价的绝对值相等,你认为还可把氢元素放在元素周期表中的_____ 族;有人建议将氢元素排在元素周期表的ⅦA族,请你写出支持这一观点的1个化学事实:____ 。
(3)上图中元素①②的原子价电子排布式分别为___ 、____ 。比较元素①与元素②的下列性质(填“>”或“<”)。原子半径:①_____ ②;电负性:①____ ②;金属性:①_____ ②;第一电离能:①_____ ②。
(4)某短周期元素最高正化合价为+7,其电子排布式为____

(1)请在上图所示的元素周期表中画出金属元素与非金属元素的分界线
(2)根据氢元素最高正化合价与最低负化合价的绝对值相等,你认为还可把氢元素放在元素周期表中的
(3)上图中元素①②的原子价电子排布式分别为
(4)某短周期元素最高正化合价为+7,其电子排布式为
您最近一年使用:0次
4 . A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的价电子排布式3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的价电子排布式3d64s2。回答下列问题:
(1)写出下列元素的符号:B_____ 、C_____ 。
(2)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是____ ,电负性最大的元素是____ 。
(3)已知元素周期表可按电子排布分为s区、p区等,则E元素在____ 区。
(4)写出A的核外电子排布式_____ 。
 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的价电子排布式3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的价电子排布式3d64s2。回答下列问题:(1)写出下列元素的符号:B
(2)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
(3)已知元素周期表可按电子排布分为s区、p区等,则E元素在
(4)写出A的核外电子排布式
您最近一年使用:0次
2020-10-24更新
|
287次组卷
|
3卷引用:四川省平昌县驷马中学2020-2021学年高二上学期10月月考化学试题
四川省平昌县驷马中学2020-2021学年高二上学期10月月考化学试题四川省巴中市平昌县驷马中学2020-2021学年高二上学期 十一月月考化学试题(已下线)第01章 原子结构与元素性质(B卷能力提升篇)-2020-2021学年高二化学选择性必修2同步单元AB卷(新教材鲁科版)
解题方法
5 . 第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线图。
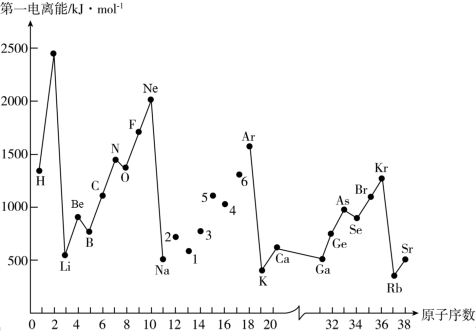
请回答以下问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象______ 。
(2)从图中分析可知,同一主族元素原子的第一电离能I1变化规律是_______ ;
(3)图中5号元素在周期表中的位置是_________ ;
(4)同周期内,随原子序数增大,I1值增大。但个别元素的I1值出现反常现试预测下列关系式中正确的是_______ 。
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)

请回答以下问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象
(2)从图中分析可知,同一主族元素原子的第一电离能I1变化规律是
(3)图中5号元素在周期表中的位置是
(4)同周期内,随原子序数增大,I1值增大。但个别元素的I1值出现反常现试预测下列关系式中正确的是
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
您最近一年使用:0次
2020-09-30更新
|
189次组卷
|
3卷引用:四川省平昌县驷马中学2020-2021学年高二上学期九月月考化学试题
四川省平昌县驷马中学2020-2021学年高二上学期九月月考化学试题(已下线)1.2 原子结构与元素的性质(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)广东省韶关实验中学2021-2022学年高二下学期第一次月考化学试题



