名校
解题方法
1 . Ti、Na、Mg、C、N、O、Fe等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种_______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_______ ,能量最低的是_______ (填序号)
a.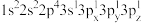 b.
b. c.
c. d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子核外共有_______ 种运动状态不同的电子,最高能层电子的电子云轮廓形状为_______ 。与Ti同周期的所有过渡元素的基态原子中,写出任意一种最外层电子数与钛不同的元素外围电子排布式_______ 。
(4)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是_______ ,判断理由是_______ 。
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是_______ 。Fe3+与Fe2+的离子半径大小关系为:Fe3+_______ Fe2+(填“大于”或“小于”),原因为:_______ 。
(1)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
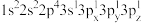 b.
b. c.
c. d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子核外共有
(4)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是
| 元素 | I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 |
| X | 737.7 | 1 450.7 | 7 732.7 |
| Y | 1 313.9 | 3 388.3 | 5 300.5 |
| Z | 1 402.3 | 2 856.0 | 4 578.1 |
您最近一年使用:0次
名校
解题方法
2 . 白铜是以镍为主要添加元素的铜基合金,呈银白色,有金属光泽,故名白铜。云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1) 的核外电子排布式为
的核外电子排布式为_______ ,3d能级上的未成对的电子数为_______ 。
(2)硫酸镍溶于氨水形成蓝色的 溶液。
溶液。
①在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为_______ ,提供孤电子对的成键原子是_______ (用元素符表示)。
②氨极易溶于 ,除因为它们都是极性分子外,还因为
,除因为它们都是极性分子外,还因为_______ 。
(3)单质铜的堆积方式为_______ ;元素铜与镍的第二电离能分别为: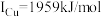 ,
,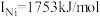 ,
,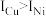 的原因是
的原因是_______ 。
(1)
 的核外电子排布式为
的核外电子排布式为(2)硫酸镍溶于氨水形成蓝色的
 溶液。
溶液。①在
 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为②氨极易溶于
 ,除因为它们都是极性分子外,还因为
,除因为它们都是极性分子外,还因为(3)单质铜的堆积方式为
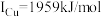 ,
,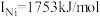 ,
,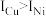 的原因是
的原因是
您最近一年使用:0次
3 . “张亭栋研究小组”受民间中医启发,发现As2O3对白血病有明显的治疗作用。氮(N)、磷(P)、砷(As)为第VA族元素,该族元素的化合物在研究和生产中有着许多重要用途。
(1)N原子的价电子排布式为______ ,N、P、As原子的第一电离能由大到小的顺序为______ 。
(2)NH3的沸点比AsH3的沸点高,原因是____________ 。
(3)立方氮化硼晶体(BN),是一种超硬材料,有优异的耐磨性,其晶胞如图所示。

①立方氮化硼是_________ 晶体,晶体中N原子的杂化轨道类型为_________ ,B原子的配位数为_________ 。
②立方氮化硼晶体中“一般共价键”与配位键的数目之比为_________ 。
(4)若立方氮化硼晶胞的边长为362 pm,则立方氮化硼的密度为_________ g/cm3(只要求列算式,不必计算出数值,阿伏伽德罗常数的值为NA)。
(1)N原子的价电子排布式为
(2)NH3的沸点比AsH3的沸点高,原因是
(3)立方氮化硼晶体(BN),是一种超硬材料,有优异的耐磨性,其晶胞如图所示。

①立方氮化硼是
②立方氮化硼晶体中“一般共价键”与配位键的数目之比为
(4)若立方氮化硼晶胞的边长为362 pm,则立方氮化硼的密度为
您最近一年使用:0次
4 . 第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。请回答以下问题:
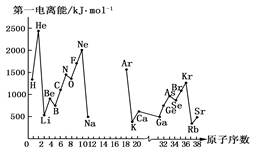
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小(最小)范围为________ <Al<________ (填元素符号)。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是________ 。
(3)上图中第一电离能最小的元素在周期表中的位置是________ 。
(4)根据对角线规则,Be、Al元素最高氧化物的水化物性质相似,它们都具有________ ,其中Be(OH)2显示这种性质的离子方程式是 __________________________ 、_____________________________ 。

(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小(最小)范围为
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是
(3)上图中第一电离能最小的元素在周期表中的位置是
(4)根据对角线规则,Be、Al元素最高氧化物的水化物性质相似,它们都具有
您最近一年使用:0次
2017-11-04更新
|
156次组卷
|
2卷引用:四川省乐山沫若中学2017-2018学年高二上学期第一次月考化学试题



