1 . 根据信息回答下列问题:
I.元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出10种元素的电负性:
已知:
i.两成键元素间电负性差值大于1.7时,形成离子键;两成键元素间电负性差值小于1.7时,形成共价键。
ii.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一。水化物M−O−H结构中,成键原子电负性差异越大,所成化学键越容易断裂,电离出OH−或H+。
(1)通过分析电负性的变化规律,确定Mg元素电负性的最小范围___________ 。
(2)判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是___________ (填字母)。
②请设计实验方案证明其为离子化合物___________ 。
(3)HClO水溶液显酸性而不显碱性的依据是___________ 。
II.元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
(4)Na的第一电离能小于Li,从原子结构的角度解释其原因___________ 。
(5)S的第一电离能小于P,结合价电子排布式解释其原因___________ 。
I.元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出10种元素的电负性:
| 元素 | Al | Be | Mg | C | Cl | Na | Li | N | Si | O | H |
| 电负性 | 1.5 | 1.5 | 2.5 | 3.0 | 0.9 | 1.0 | 3.0 | 1.8 | 3.5 | 2.1 |
i.两成键元素间电负性差值大于1.7时,形成离子键;两成键元素间电负性差值小于1.7时,形成共价键。
ii.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一。水化物M−O−H结构中,成键原子电负性差异越大,所成化学键越容易断裂,电离出OH−或H+。
(1)通过分析电负性的变化规律,确定Mg元素电负性的最小范围
(2)判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是
②请设计实验方案证明其为离子化合物
(3)HClO水溶液显酸性而不显碱性的依据是
II.元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
(4)Na的第一电离能小于Li,从原子结构的角度解释其原因
(5)S的第一电离能小于P,结合价电子排布式解释其原因
您最近一年使用:0次
2 . 下表为长式周期表的一部分,其中的编号代表对应的元素。
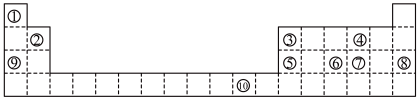
请回答下列问题:
(1)表中元素⑩的二价离子的外围电子排布图为:___________ ,该元素属于___________ 区元素。
(2)基态原子⑦核外电子总共有___________ 种能量,电子占据的能量最高的能级符号为___________
(3)在标号的主族元素中,第一电离能最小的是___________ (填元素符号,下同),电负性最大的是___________
(4)写出由①④⑨三种元素组成的化合物的电子式___________ ,将该化合物溶于水,破坏的作用力有___________ ;
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与 溶液反应的化学方程式:
溶液反应的化学方程式:___________

请回答下列问题:
(1)表中元素⑩的二价离子的外围电子排布图为:
(2)基态原子⑦核外电子总共有
(3)在标号的主族元素中,第一电离能最小的是
(4)写出由①④⑨三种元素组成的化合物的电子式
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与
 溶液反应的化学方程式:
溶液反应的化学方程式:
您最近一年使用:0次
2021-11-13更新
|
540次组卷
|
3卷引用:第1.2.2讲 元素周期律-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
(已下线)第1.2.2讲 元素周期律-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)四川省绵阳南山中学2021-2022学年高二上学期半期考试化学试题黑龙江省肇东市第四中学2021-2022学年高二下学期期中考试化学试题
名校
3 . 按要求完成下列各题。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(2) 成为阳离子时首先失去
成为阳离子时首先失去___________ 轨道电子, 的价层电子排布式为
的价层电子排布式为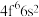 ,
, 价层电子排布式为
价层电子排布式为___________ 。
(3) 基态核外电子排布式为
基态核外电子排布式为___________ 。
(4)下列 原子电子排布图表示的状态中,能量最低和最高的分别为
原子电子排布图表示的状态中,能量最低和最高的分别为___________ 、___________ (填标号)。
A. B.
B.
C. D.
D.
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A. | B. | C. | D. |
 成为阳离子时首先失去
成为阳离子时首先失去 的价层电子排布式为
的价层电子排布式为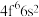 ,
, 价层电子排布式为
价层电子排布式为(3)
 基态核外电子排布式为
基态核外电子排布式为(4)下列
 原子电子排布图表示的状态中,能量最低和最高的分别为
原子电子排布图表示的状态中,能量最低和最高的分别为A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次
名校
解题方法
4 . 第四周期有14种金属元素,其中4种为主族元素,10种为过渡元素。 回答下列问题:
(1)写出其中原子序数最小的副族元素的元素符号___________ ,主族序数最大的元素名称___________ ;
(2)锰元素在周期表中的位置为___________ ;属于___________ 区元素 填“s”“p”“d”“ds”或“f”
填“s”“p”“d”“ds”或“f” 。
。
(3)基态铬原子的电子排布式为___________ ,与铬同周期的所有元素的基态原子中,最外层电子数与铬原子相同的有___________ 。
(4)基态Fe原子中,电子占据的最高能层的符号为___________ ,该能层具有的原子轨道数为___________ 。
(5)铜、锌两种元素的第一电离能、第二电离能如表所示:
铜的第二电离能 却大于锌的第二电离能,其主要原因是
却大于锌的第二电离能,其主要原因是___________ 。
(1)写出其中原子序数最小的副族元素的元素符号
(2)锰元素在周期表中的位置为
 填“s”“p”“d”“ds”或“f”
填“s”“p”“d”“ds”或“f” 。
。(3)基态铬原子的电子排布式为
(4)基态Fe原子中,电子占据的最高能层的符号为
(5)铜、锌两种元素的第一电离能、第二电离能如表所示:
电离能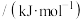 |  |  |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
铜的第二电离能
 却大于锌的第二电离能,其主要原因是
却大于锌的第二电离能,其主要原因是
您最近一年使用:0次
5 . 下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。
(1)元素b位于周期表中_______ 区,其基态原子核外有_______ 种运动状态不同的电子。
(2)基态c原子中有_______ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为_______ 形。
(3)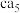 理论上为离子化合物,猜测其电子式为
理论上为离子化合物,猜测其电子式为_______ 。
(4)基态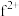 外围电子的电子排布图为
外围电子的电子排布图为_______ ,已知高温下化合物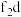 比化合物fd更稳定,试从核外电子排布的角度解释原因
比化合物fd更稳定,试从核外电子排布的角度解释原因_______ 。
(5)b、c、d三种元素的第一电离能由大到小的顺序为_______ (填元素符号)。

(1)元素b位于周期表中
(2)基态c原子中有
(3)
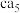 理论上为离子化合物,猜测其电子式为
理论上为离子化合物,猜测其电子式为(4)基态
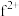 外围电子的电子排布图为
外围电子的电子排布图为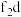 比化合物fd更稳定,试从核外电子排布的角度解释原因
比化合物fd更稳定,试从核外电子排布的角度解释原因(5)b、c、d三种元素的第一电离能由大到小的顺序为
您最近一年使用:0次
2021-07-09更新
|
900次组卷
|
6卷引用:第一章 原子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
(已下线)第一章 原子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)广东省肇庆市2020-2021学年高二下学期末教学质量检测化学(物质结构与性质)试题(已下线)1.2.2 原子结构与元素周期律(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)广西南宁市2022-2023学年高二下学期开学考试化学试题江苏省无锡市市北高级中学2023-2024学年高二上学期期末检测化学试卷(已下线)猜想01 原子结构与性质 【考题猜想】(8大题型)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
解题方法
6 . 根据下列五种元素的电离能数据(单位∶ kJ/mol),回答下列问题。
(1)在周期表中,最可能处于同一族的是_______ 。
A.Q和 R B.S和T C. T和U D.R和T E.R和U
(2)电解它们的熔融氯化物,以下过程最可能正确的是_________ 。
A.Q2++2e-→Q B.R2++2e-→R
C.S3++3e-→S D.T3++3e-→T
(3)它们的氯化物的化学式,最可能正确的是________
A. QCl2 B. RCl C. SCl3 D.TCl
(4)S 元素最可能是________ 素
A.S区元素 B.稀有气体元素 C.p 区元素 D .准金属
(5)下列元素中,化学性质和物理性质最像Q元素的是_____ 。
A.氦(1s2) B.铍(1s12s2) C.锂(1s22s1) D.氢(1s1)
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
A.Q和 R B.S和T C. T和U D.R和T E.R和U
(2)电解它们的熔融氯化物,以下过程最可能正确的是
A.Q2++2e-→Q B.R2++2e-→R
C.S3++3e-→S D.T3++3e-→T
(3)它们的氯化物的化学式,最可能正确的是
A. QCl2 B. RCl C. SCl3 D.TCl
(4)S 元素最可能是
A.S区元素 B.稀有气体元素 C.p 区元素 D .准金属
(5)下列元素中,化学性质和物理性质最像Q元素的是
A.氦(1s2) B.铍(1s12s2) C.锂(1s22s1) D.氢(1s1)
您最近一年使用:0次
2021-05-08更新
|
712次组卷
|
4卷引用:第1.2.2讲 元素周期律-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
(已下线)第1.2.2讲 元素周期律-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)福建省福州市金山中学2020-2021学年高二下期中考试化学试题第一章原子结构与性质(基础卷)浙江省绍兴蕺山外国语学校2021-2022学年高二下学期第一次月考化学试题
7 . 金属氢化物是具有良好发展前景的储氢材料。
(1)LiH中,离子半径:Li+_________ H-(填“>”、“=”或“<”)。
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_________ (填元素符号)。
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是_____ 。
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是_____________________ ;只含有σ键的是__________ ;含有由两个原子的s轨道重叠形成的σ键的是________ ;不存在化学键的是________ ;含有离子键和非极性键的是_________ 。
(1)LiH中,离子半径:Li+
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是
您最近一年使用:0次
9-10高二下·河南郑州·期末
名校
8 . 不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如下图所示。试根据元素在周期表中的位置,分析图中曲线的变化特点,并回答下列问题。1至19号元素气态原子失去最外层一个电子所需能量
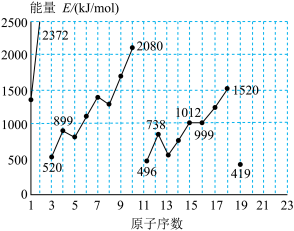
(1)同主族内不同元素的E值变化的特点是_______ 。各主族中E值的这种变化特点体现了元素性质_______ 变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系中正确的是_______ (填写编号)。
①E(砷)>E(硒) ②E(砷)<E(硒)
③E (溴)>E(硒) ④E(溴)<E(硒)
(3)估计l mol气态Ca原子失去最外层一个电子所需能量E值的范围_______ <E<_______ 。
(4)10号元素E值较大的原因______________________________ 。

(1)同主族内不同元素的E值变化的特点是
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系中正确的是
①E(砷)>E(硒) ②E(砷)<E(硒)
③E (溴)>E(硒) ④E(溴)<E(硒)
(3)估计l mol气态Ca原子失去最外层一个电子所需能量E值的范围
(4)10号元素E值较大的原因
您最近一年使用:0次
2019-04-10更新
|
201次组卷
|
6卷引用:2019年4月14日 《每日一题》选修3-每周一测
(已下线)2019年4月14日 《每日一题》选修3-每周一测(已下线)2010年郑州市盛同学校高二下学期期末考试化学试题(已下线)2012年苏教版高中化学选修3 2.2元素性质的递变规律练习卷云南省昭通市威信县第一中学2018-2019学年高二上学期12月份考试化学试题云南省玉溪市新平三中2019-2020学年高二上学期12月份月考化学试题云南省瑞丽市第一民族中学2021-2022学年高二下学期3月月考化学试题
9 . 现有核电荷数小于18的元素A,其电离能数据如表所示[I1表示失去第1个电子的电离能,In(n=2,3,4,5,6,7,8,9,10,11)表示失去第n个电子的电离能,单位为eV]。
(1)外层电子离核越远,能量越高,电离能越________ (填“大”或“小”);阳离子电荷数越多,在失去电子时,电离能越_______ (填“大”或“小”)。
(2)上述11个电子分属_______ 个电子层。
(3)去掉11个电子后,该元素还有_______ 个电子。
(4)该元素的最高价氧化物对应的水化物的化学式是_______ 。
| 符号 | I1 | I2 | I3 | I4 | I5 | I6 |
| 电离能 | 7.64 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 |
| 符号 | I7 | I8 | I9 | I10 | I11 | |
| 电离能 | 224.9 | 226.0 | 327.9 | 367.4 | 1 761 |
(1)外层电子离核越远,能量越高,电离能越
(2)上述11个电子分属
(3)去掉11个电子后,该元素还有
(4)该元素的最高价氧化物对应的水化物的化学式是
您最近一年使用:0次



