1 . 元素第一电离能变化规律

(1)每个周期的第一种元素的第一电离能_______ ,最后一种元素的第一电离能_______ ,即一般来说,随着核电荷数的递增,元素的第一电离能呈_______ 趋势。
(2)同一族,从上到下第一电离能逐渐_______ 。

(1)每个周期的第一种元素的第一电离能
(2)同一族,从上到下第一电离能逐渐
您最近一年使用:0次
2 . 注意:电离能的影响因素及特例
(1)电离能数值的大小主要取决于原子的_______ 、原子半径及原子的电子构型。
(2)具有全充满、半充满及全空的电子构型的元素稳定性较高,其电离能数值_______ ,如稀有气体的电离能在同周期元素中_______ ,N为半充满、Mg为全充满状态,其电离能均比同周期相邻元素大。一般情况,第一电离能:ⅡA_______ ⅢA,ⅤA_______ ⅥA。
(1)电离能数值的大小主要取决于原子的
(2)具有全充满、半充满及全空的电子构型的元素稳定性较高,其电离能数值
您最近一年使用:0次
3 . 电离能的应用
(1)根据电离能数据,确定元素原子核外电子的排布及元素的化合价。如Li:I1≪I2<I3,表明Li原子核外的_______ 个电子排布在两个能层上(K、L能层),且最外层上只有一个电子,易失去_______ 形成_______ 阳离子。
(2)判断元素的金属性、非金属性强弱:I1越_______ ,元素的非金属性越_______ ;I1越小,元素的金属性越_______ 。
(1)根据电离能数据,确定元素原子核外电子的排布及元素的化合价。如Li:I1≪I2<I3,表明Li原子核外的
(2)判断元素的金属性、非金属性强弱:I1越
您最近一年使用:0次
21-22高二下·全国·单元测试
解题方法
4 . 元素第一电离能的概念与意义
(1)概念
①第一电离能:_______ 电中性_______ 原子失去一个电子转化为_______ 正离子所需要的_______ 叫做第一电离能,符号:_______ 。
②逐级电离能:气态基态_______ 价正离子再_______ 一个电子成为气态基态_______ 价正离子所需的最低能量叫做第二电离能,第三电离能和第四、第五电离能依此类推。由于原子失去电子形成离子后,若再失去电子会更加_______ ,因此同一原子的各级电离能之间存在如下关系:I1<I2<I3……
(2)意义:可以衡量元素的原子_______ 一个电子的_______ 程度。第一电离能数值越_______ ,原子越_______ 失去一个电子;第一电离能数值越_______ ,原子越_______ 失去一个电子。
(1)概念
①第一电离能:
②逐级电离能:气态基态
(2)意义:可以衡量元素的原子
您最近一年使用:0次
21-22高二下·全国·单元测试
5 . 解题技巧:电离能的应用
①根据电离能数据,确定元素在化合物中的化合价,如K:I1≪I2<I3,表明K原子易失去一个电子形成+1价阳离子。
②判断元素的金属性、非金属性强弱:I1越_______ ,元素的非金属性越_______ ;I1越_______ ,元素的金属性越_______ 。
①根据电离能数据,确定元素在化合物中的化合价,如K:I1≪I2<I3,表明K原子易失去一个电子形成+1价阳离子。
②判断元素的金属性、非金属性强弱:I1越
您最近一年使用:0次
20-21高二·全国·课时练习
6 . 在下列空格中,填上适当的元素符号。
(1)在第3周期中,第一电离能最小的元素是_______ ,第一电离能最大的元素是_______ 。
(2)在元素周期表中,电负性最大的元素是_______ ,电负性最小的元素是_______ 。
(3)在第4周期元素中,原子的4p轨道半充满的是_______ ,3d轨道半充满的_______ ,4s轨道半充满的是_______ ,外围电子中s电子数与d电子数相同的是_______ 。
(1)在第3周期中,第一电离能最小的元素是
(2)在元素周期表中,电负性最大的元素是
(3)在第4周期元素中,原子的4p轨道半充满的是
您最近一年使用:0次
2022-11-25更新
|
1021次组卷
|
3卷引用:【知识图鉴】单元讲练测选择性必修2第1章02基础练
7 . 按要求回答下列问题:
(1)研究发现,在CO2低压合成甲醇反应CO2+3H2=CH3OH+H2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布为___________ ;元素Mn与O中,第一电离能较大的是___________ ,基态原子核外未成对电子数较多的是___________ 。
(2)我国科学家成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl。
①氮原子的价层电子排布图为___________ 。
②元素的基态的气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1),第二周期部分元素的E1变化趋势如图所示。
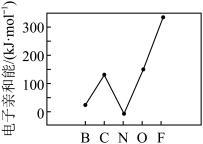
其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________ ,氮元素E1呈现异常的原因是___________ 。
(1)研究发现,在CO2低压合成甲醇反应CO2+3H2=CH3OH+H2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布为
(2)我国科学家成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl。
①氮原子的价层电子排布图为
②元素的基态的气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1),第二周期部分元素的E1变化趋势如图所示。

其中除氮元素外,其他元素的E1自左而右依次增大的原因是
您最近一年使用:0次
2022-10-20更新
|
208次组卷
|
10卷引用:第1章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修1)
(已下线)第1章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修1)(已下线)第一章 原子结构与性质(B卷) 湖北省咸宁市嘉鱼县第一中学2019-2020学年高二下学期期末考试化学试题广东省东莞市新世纪英才学校2021-2022学年高二上学期第一次教学质量检测化学试题第一章 本章达标检测2河北省石家庄市第23中学2022-2023学年高二上学期第一次月考化学试题常州市武进区礼嘉中学2021-2022学年高二下学期第二次阶段测试化学试题湖南省衡阳县第四中学 2022-2023学年高二下学期开学摸底考试(平行班)化学试题(已下线)考点33 原子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)
8 . 白铜是以镍为主要添加元素的铜基合金,呈银白色,有金属光泽,故名白铜。云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1) 的核外电子排布式为
的核外电子排布式为_______ ,3d能级上的未成对的电子数为_______ 。
(2)硫酸镍溶于氨水形成蓝色的 溶液。
溶液。
①在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为_______ ,提供孤电子对的成键原子是_______ (用元素符表示)。
②氨极易溶于 ,除因为它们都是极性分子外,还因为
,除因为它们都是极性分子外,还因为_______ 。
(3)单质铜及镍都是由_______ 键形成的晶体;元素铜与镍的第二电离能分别为: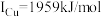 ,
,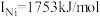 ,
,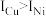 的原因是
的原因是_______ 。
(1)
 的核外电子排布式为
的核外电子排布式为(2)硫酸镍溶于氨水形成蓝色的
 溶液。
溶液。①在
 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为②氨极易溶于
 ,除因为它们都是极性分子外,还因为
,除因为它们都是极性分子外,还因为(3)单质铜及镍都是由
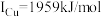 ,
,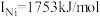 ,
,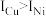 的原因是
的原因是
您最近一年使用:0次
9 . 黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能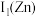
_______  (填“大于”或“小于”)。原因是
(填“大于”或“小于”)。原因是_______ 。
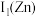
 (填“大于”或“小于”)。原因是
(填“大于”或“小于”)。原因是
您最近一年使用:0次
2022-08-22更新
|
637次组卷
|
3卷引用:专题2 原子结构与元素性质 ★第二单元综合拔高练
10 . 太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:
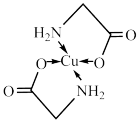
(1)铜位于周期表中___________ 区。
(2)基态二价铜离子的电子排布式为___________ ,已知高温下Cu2O比CuO更稳定,试从核外电子排布角度解释___________ 。
(3)硼核外电子的运动状态的概率密度分布可用___________ 形象化描述。
(4)Fe3+的价电子排布图为___________ 。
(5)N、O、Se三种元素中的第一电离能最大的为:___________ 。

(1)铜位于周期表中
(2)基态二价铜离子的电子排布式为
(3)硼核外电子的运动状态的概率密度分布可用
(4)Fe3+的价电子排布图为
(5)N、O、Se三种元素中的第一电离能最大的为:
您最近一年使用:0次
2021-05-11更新
|
455次组卷
|
4卷引用:专题1~2 综合检测(提升卷)
专题1~2 综合检测(提升卷)宁夏吴忠中学2020-2021学年高二下学期期中考试化学试题(已下线)作业02 原子结构与元素的性质-2021年高二化学暑假作业(人教版2019)(已下线)专题突破卷06 物质结构与性质?-2024年高考化学一轮复习考点通关卷(新教材新高考)



