1 . 按要求回答下列问题:
(1)消毒液的组成元素中,基态O原子的电子排布式是______ ,基态Cl原子未成对电子数为_____ 个。
(2)与氧元素相邻的氮元素的第一电离能的大小顺序为_______ (填元素符号),氧元素和氮元素的非金属性的大小顺序为________ (填元素符号)
(3)某元素原子的最外层电子构型为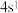 ,元素周期表的位置第
,元素周期表的位置第____ 周期,第_____ 族,它属于____ 区元素。
(1)消毒液的组成元素中,基态O原子的电子排布式是
(2)与氧元素相邻的氮元素的第一电离能的大小顺序为
(3)某元素原子的最外层电子构型为
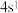 ,元素周期表的位置第
,元素周期表的位置第
您最近一年使用:0次
2 . 依据原子结构知识回答下列问题。
(1)下列有关说法错误的是___________。
(2)基态V原子中具有___________ 种不同能量的电子,具有___________ 种不同空间运动状态的电子,具有___________ 种不同运动状态的电子。
(3)基态Cu原子的简化电子排布式为___________ ,基态Se原子的价电子轨道表示式为___________ ,基态Mn2+的价电子排布式为___________ 。
(1)下列有关说法错误的是___________。
| A.简单离子的还原性:P3->O2->F- |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(3)基态Cu原子的简化电子排布式为
您最近一年使用:0次
3 . 按要求回答下列问题:
(1)已知A和B为第三周期元素,其第一至第四电离能如表所示:
A通常显___________ 价,B的基态原子核外电子排布式为___________ 。
(2)如图为元素周期表中部分元素某种性质(X值)随原子序数变化的关系:___________ (填元素符号)。
②同主族内不同元素的X值变化的特点是___________ ;同周期内,随着原子序数的增大,X值的变化总趋势是___________ 。周期表中X值的这种变化特点体现了元素性质的___________ 变化规律。
③X值较小的元素集中在元素周期表的___________ (填字母)。
a.左下角 b.右上角 c.分界线附近
④下列关于元素此性质的说法正确的是___________ (填字母)。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
(1)已知A和B为第三周期元素,其第一至第四电离能如表所示:
电离能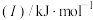 |  | 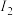 | 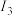 | 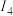 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)如图为元素周期表中部分元素某种性质(X值)随原子序数变化的关系:
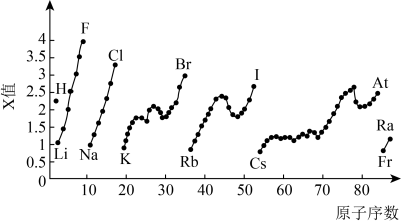
②同主族内不同元素的X值变化的特点是
③X值较小的元素集中在元素周期表的
a.左下角 b.右上角 c.分界线附近
④下列关于元素此性质的说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
您最近一年使用:0次
2024-04-27更新
|
38次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期1月期末化学试题
4 . 北宋卷轴画《千里江山图》,颜色绚丽,由石绿、雌黄、赭石、阵磲、朱砂等颜料绘制而成,颜料中含有硫、砷、铜、锌、钛、铁等元素。
(1)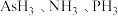 热稳定性由大到小的顺序为
热稳定性由大到小的顺序为_____ 。
(2) 属于元素周期表中的
属于元素周期表中的_____ 区;基态 原子的电子排布式为
原子的电子排布式为_____ ;基态硫原子核外电子的空间运动状态有_____ 种;基态 的价层电子的轨道表示式为
的价层电子的轨道表示式为_____ 。
(3) 的第二电离能
的第二电离能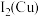
_____  的第二电离能
的第二电离能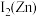 (填“>”或“<”),理由为
(填“>”或“<”),理由为_____ 。
(1)
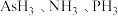 热稳定性由大到小的顺序为
热稳定性由大到小的顺序为(2)
 属于元素周期表中的
属于元素周期表中的 原子的电子排布式为
原子的电子排布式为 的价层电子的轨道表示式为
的价层电子的轨道表示式为(3)
 的第二电离能
的第二电离能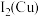
 的第二电离能
的第二电离能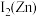 (填“>”或“<”),理由为
(填“>”或“<”),理由为
您最近一年使用:0次
5 . 按要求解答下列各题。
(1)黄铜是人类最早使用的合金之一,主要由 和
和 组成。基态
组成。基态 原子的核外价层电子排布图为
原子的核外价层电子排布图为_______ ;第二电离能
_______ (填“<”“>”或“=”)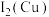 。
。
(2) 和
和 中
中 之间以双键结合,
之间以双键结合, 之间以单键结合。请你预测
之间以单键结合。请你预测 和
和 分子的空间结构为
分子的空间结构为_______ 。 分子中
分子中
_______  分子中
分子中 (选填“<”“>”或“=”)。
(选填“<”“>”或“=”)。
(3)甲醇的沸点(64.7℃)介于水和甲硫醇 ,其原因是
,其原因是_______ 。
(1)黄铜是人类最早使用的合金之一,主要由
 和
和 组成。基态
组成。基态 原子的核外价层电子排布图为
原子的核外价层电子排布图为
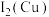 。
。(2)
 和
和 中
中 之间以双键结合,
之间以双键结合, 之间以单键结合。请你预测
之间以单键结合。请你预测 和
和 分子的空间结构为
分子的空间结构为 分子中
分子中
 分子中
分子中 (选填“<”“>”或“=”)。
(选填“<”“>”或“=”)。(3)甲醇的沸点(64.7℃)介于水和甲硫醇
 ,其原因是
,其原因是
您最近一年使用:0次
6 . 填空
(1)基态铜原子价层电子排布图为______ ﹔已知Cu第一电离能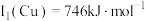 ,Fe第一电离能
,Fe第一电离能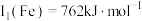 ,则
,则
______  (填“>”、“=”或“<”),其主要原因是
(填“>”、“=”或“<”),其主要原因是______ ;
(2) 和
和 的中心原子的杂化轨道类型分别为
的中心原子的杂化轨道类型分别为______ ,试判断 和
和 的键角大小关系:
的键角大小关系:
______  ,说明原因:
,说明原因:______
(3)比较 和
和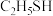 的酸性:
的酸性:
______ 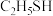 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(1)基态铜原子价层电子排布图为
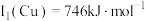 ,Fe第一电离能
,Fe第一电离能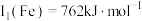 ,则
,则
 (填“>”、“=”或“<”),其主要原因是
(填“>”、“=”或“<”),其主要原因是(2)
 和
和 的中心原子的杂化轨道类型分别为
的中心原子的杂化轨道类型分别为 和
和 的键角大小关系:
的键角大小关系:
 ,说明原因:
,说明原因:(3)比较
 和
和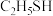 的酸性:
的酸性:
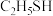 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
2024-04-03更新
|
346次组卷
|
2卷引用:浙江省杭州市源清中学2023-2024学年高二上学期期末考试化学试题
7 . 现有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
(2) 元素的原子核外共有
元素的原子核外共有___________ 种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3) 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是___________ 。
(4) 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是___________ 。
(5) 位于元素周期表中
位于元素周期表中___________ 区(按电子排布分区),其基态原子的价层电子排布式为___________ 。
(6)G单质投入水中所得溶液阳离子检验方法___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
 元素是形成化合物种类最多的元素 元素是形成化合物种类最多的元素 |
 元素基态原子的核外 元素基态原子的核外 能级电子数比 能级电子数比 能级电子总数少1个 能级电子总数少1个 |
 元素基态原子的核外 元素基态原子的核外 轨道中有两个未成对电子 轨道中有两个未成对电子 |
 元素的气态基态原子的第一至第四电离能分别是 元素的气态基态原子的第一至第四电离能分别是 , , , , , ,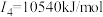 |
 元素的主族序数与周期数的差为4 元素的主族序数与周期数的差为4 |
 元素是前四周期中电负性最小的元素 元素是前四周期中电负性最小的元素 |
 元素位于元素周期表中的第8列 元素位于元素周期表中的第8列 |
 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)(2)
 元素的原子核外共有
元素的原子核外共有(3)
 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是(4)
 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是(5)
 位于元素周期表中
位于元素周期表中(6)G单质投入水中所得溶液阳离子检验方法
您最近一年使用:0次
解题方法
8 . A、B、C、D、E、F为六种原子序数依次增大的短周期元素,A、B、D位于同一主族,且D的原子半径在短周期元素原子中最大。C是周期表中电负性最大的元素。基态E原子的核外电子有7种空间运动状态。基态F原子有3个未成对电子。按要求回答下列问题:
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式___________ 。
(2)基态原子第一电离能大小介于E和F之间的元素有___________ 。(用元素符号表示)
(3)氨硼烷(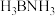 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为___________ (用元素符号表示)。
(4)磷酸盐在微生物作用下可转化为 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为___________ 。 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为___________ 。
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式
(2)基态原子第一电离能大小介于E和F之间的元素有
(3)氨硼烷(
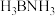 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为(4)磷酸盐在微生物作用下可转化为
 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为
您最近一年使用:0次
2024-03-04更新
|
234次组卷
|
2卷引用:浙江省杭州第二中学东河校区2023-2024学年高二上学期期末考试化学试题
9 . 化学的符号表征是化学交流与传承的基础。关于C、N、O、Cl、Fe、Cr六种元素有关的问题,完成下列填空。
(1)可以正确描述碳原子结构的是___________。
(2)基态原子Cl核外电子总共有___________ 种能量,电子占据的能量最高的能级符号为___________ 。
(3)C、N、O元素的第一电离能由大到小顺序为___________ ,判断理由是___________ 。
(4)上述六种元素中,基态原子的未成对电子数最多的是___________ (填元素名称),其价电子轨道表示式为___________ 。
(1)可以正确描述碳原子结构的是___________。
A.原子结构示意图: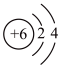 | B.原子核外能量最高的电子云图像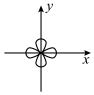 |
| C.碳-12原子:C | D.原子的轨道表示式: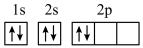 |
(2)基态原子Cl核外电子总共有
(3)C、N、O元素的第一电离能由大到小顺序为
(4)上述六种元素中,基态原子的未成对电子数最多的是
您最近一年使用:0次
10 . 深入研究物质的微观结构,有利于理解物质变化的本质。请回答下列问题:
(1)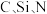 的电负性由大到小的顺序是
的电负性由大到小的顺序是___________ 。
(2)C、N、O、F的第一电离能由大到小的顺序是___________ 。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为 或
或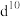 排布时,无颜色;为
排布时,无颜色;为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,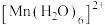
_________ 颜色(填“无”或“有”)。
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是___________ (填元素符号)。
(5) 能与
能与 形成正四面体形的配合物
形成正四面体形的配合物 ,
,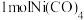 中含有
中含有__________  键。
键。
(1)
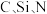 的电负性由大到小的顺序是
的电负性由大到小的顺序是(2)C、N、O、F的第一电离能由大到小的顺序是
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
 或
或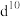 排布时,无颜色;为
排布时,无颜色;为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,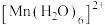
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是
(5)
 能与
能与 形成正四面体形的配合物
形成正四面体形的配合物 ,
,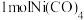 中含有
中含有 键。
键。
您最近一年使用:0次



