名校
1 . 血红蛋白结合O2后的结构如图所示,CO也可与血红蛋白结合,它与血红蛋白结合的能力约为O2的230~270倍。二者与血红蛋白(Hb)结合的反应可表示为:①Hb+O2⇌Hb(O2)K1;②Hb+CO⇌Hb(CO)K2
下列说法不正确的是

下列说法不正确的是

| A.Fe2+的基态电子的空间运动状态有14种 |
| B.电负性:O>C>Fe |
| C.由题意可得结论:相同温度下,K2<K1 |
| D.CO中毒患者进入高压氧舱治疗,平衡①、②移动的方向相反 |
您最近一年使用:0次
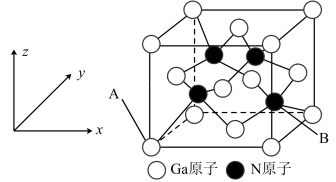
2 . 氮(N)、镓(Ga)合金由于其良好的电学传导和光学透明性被广泛用于薄膜太阳能电池领域,氮化镓晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。
(2)晶胞中与同一个N原子相连的Ga原子构成的空间构型为___________ ,晶胞中与Ga原子相邻且最近的Ga原子个数为___________ 。
(3)以晶胞边长为单位长度建立的坐标系可以表示晶胞中的原子位置,称作原子分数坐标。A原子坐标为(0, ,
, ),则B原子坐标为
),则B原子坐标为___________ 。
(4)若GaN晶胞边长为apm,则Ga原子与N原子的最短核间距为___________ pm,该晶胞的密度为___________ g/cm3
(5)吡啶(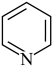 )是类似于苯的芳香族化合物。广义酸碱理论认为:凡能给出质子(
)是类似于苯的芳香族化合物。广义酸碱理论认为:凡能给出质子( )的任何分子或离子都是酸:凡能结合质子(
)的任何分子或离子都是酸:凡能结合质子( )的分子或离子都是碱。按此理论,吡啶(
)的分子或离子都是碱。按此理论,吡啶(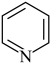 )属于
)属于___________ (填“酸”、“碱”或“盐”)。
| A.GaN晶体中存在非极性共价键 | B.电负性:N>Ga |
| C.原子半径:N>Ga | D.沸点:NH3>PH3 |
(3)以晶胞边长为单位长度建立的坐标系可以表示晶胞中的原子位置,称作原子分数坐标。A原子坐标为(0,
 ,
, ),则B原子坐标为
),则B原子坐标为(4)若GaN晶胞边长为apm,则Ga原子与N原子的最短核间距为
(5)吡啶(
 )是类似于苯的芳香族化合物。广义酸碱理论认为:凡能给出质子(
)是类似于苯的芳香族化合物。广义酸碱理论认为:凡能给出质子( )的任何分子或离子都是酸:凡能结合质子(
)的任何分子或离子都是酸:凡能结合质子( )的分子或离子都是碱。按此理论,吡啶(
)的分子或离子都是碱。按此理论,吡啶( )属于
)属于
您最近一年使用:0次
名校
解题方法
3 . 丁二酮肟常用于检验 ,在稀氨水介质中,丁二酮肟与
,在稀氨水介质中,丁二酮肟与 反应可生成鲜红色沉淀,其结构如图所示。下列说法不正确的是
反应可生成鲜红色沉淀,其结构如图所示。下列说法不正确的是
 ,在稀氨水介质中,丁二酮肟与
,在稀氨水介质中,丁二酮肟与 反应可生成鲜红色沉淀,其结构如图所示。下列说法不正确的是
反应可生成鲜红色沉淀,其结构如图所示。下列说法不正确的是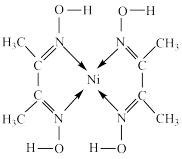
A.元素H、C、N、O、Ni电负性由大到小的顺序为 |
| B.1mol该沉淀含有σ键与π键的个数比为17:2 |
C.基态 的价电子排布式为 的价电子排布式为 |
D.该沉淀中C的杂化方式为 、 、 |
您最近一年使用:0次
2022-12-17更新
|
755次组卷
|
7卷引用:吉林省延边第二中学2022-2023学年高二上学期期末考试化学试题
4 . 咔唑(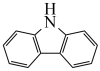 )是一种新型有机液体储氢介质。下列说法错误的是
)是一种新型有机液体储氢介质。下列说法错误的是
 )是一种新型有机液体储氢介质。下列说法错误的是
)是一种新型有机液体储氢介质。下列说法错误的是| A.碳、氮、氢三种元素电负性:N>C>H |
| B.同周期元素中第一电离能高于N的有3种 |
C.咔唑的沸点比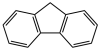 的沸点高 的沸点高 |
D.基态氮原子的外围电子轨道表示式不能写为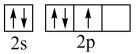 ,因为违背了洪特规则 ,因为违背了洪特规则 |
您最近一年使用:0次
5 . 下列说法中正确的个数是
①从空间的角度看,2s轨道比1s轨道大,其空间包含了1s
②2p、3p、4p能级的轨道数依次增多
③s区全部是金属元素
④电负性的大小可以用作判断元素非金属性强弱的依据
⑤第一电离能的大小可以作为判断金属性强弱的依据
⑥共价化合物中,电负性大的成键元素表现为负价
⑦电负性越大,元素的非金属性越强,第一电离能也越大
⑧第四周期元素中,未成对电子数最多的元素位于钾元素后面第五位
⑨电负性大于1.8的一定为非金属,小于1.8的一定为金属
①从空间的角度看,2s轨道比1s轨道大,其空间包含了1s
②2p、3p、4p能级的轨道数依次增多
③s区全部是金属元素
④电负性的大小可以用作判断元素非金属性强弱的依据
⑤第一电离能的大小可以作为判断金属性强弱的依据
⑥共价化合物中,电负性大的成键元素表现为负价
⑦电负性越大,元素的非金属性越强,第一电离能也越大
⑧第四周期元素中,未成对电子数最多的元素位于钾元素后面第五位
⑨电负性大于1.8的一定为非金属,小于1.8的一定为金属
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近一年使用:0次
6 . 下列关于原子结构与元素周期表的说法正确的是
| A.电负性最大的元素位于周期表的左下角 |
| B.原子核外可能有两个电子的运动状态是相同的 |
| C.2s轨道在空间呈哑铃形 |
| D.某基态原子的价电子排布式为4s24p1,该元素位于周期表第四周期IIIA族 |
您最近一年使用:0次
2022-03-20更新
|
103次组卷
|
2卷引用:吉林省长春外国语学校2021-2022学年高二上学期期末考试化学试题
7 . 下列说法不正确的是
A.酸性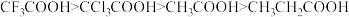 |
B. 氯丁烷分子中含1个手性碳原子 氯丁烷分子中含1个手性碳原子 |
C. 存在顺反异构 存在顺反异构 |
| D.同一分子内也可能形成氢键 |
您最近一年使用:0次
名校
8 . 元素X、Y、Z在周期表中的相对位置如图。已知X元素原子的价层电子排布式为 ,则下列说法错误的是
,则下列说法错误的是
 ,则下列说法错误的是
,则下列说法错误的是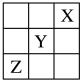
| A.Y元素原子核外d能级无电子填充 |
| B.电负性:X>Y>Z |
| C.元素的最高正价:X>Y>Z |
| D.基态Z原子的核外电子占据的最高能级的电子云轮廓图的形状为哑铃形 |
您最近一年使用:0次
2023-07-10更新
|
134次组卷
|
5卷引用:吉林省松原市前郭尔罗斯蒙古族自治县榆树实验,九台一中,前郭,农安2022-2023学年高二下学期7月期末考试化学试题
名校
9 . X、Y、Z、W为原子序数依次增大的短周期主族元素,Y、Z均可与X形成含10个电子的分子,且第一电离能Y>Z。W原子电离能:I1=500、I2=4600、I3=6900、I4=9500、I5…,下列说法错误的是
| A.Y、Z还均可与X形成含18个电子的分子 |
| B.这四种元素位于三个不同周期 |
| C.简单离子半径:Y>Z>W |
| D.电负性:Y>Z>X |
您最近一年使用:0次
2022-02-20更新
|
432次组卷
|
3卷引用:吉林省吉林市田家炳高级中学2022-2023学年高二上学期期末线上考试化学试题
名校
10 . 新型光催化剂Zn2GeO4具有较高的催化活性。下列有关其组成元素的说法正确的是
| A.Zn处于元素周期表中的d区 |
| B.Ge的价电子排布式为3d104s24p2 |
| C.基态O原子中成对电子数是未成对电子数的2倍 |
| D.三种元素电负性由大到小的顺序是:O>Ge>Zn |
您最近一年使用:0次
2022-12-14更新
|
245次组卷
|
2卷引用:吉林省长春外国语学校2022-2023学年高二上学期期末考试化学试卷



