18-19高二下·吉林延边·期中
名校
解题方法
1 . I.金属元素在现代工业中也占据极其重要的地位,钛被称为“未来的钢铁”,具有质轻,抗腐蚀,硬度大特点,是理想化工设备材料.
(1)基态钛原子核外共有_____ 种运动状态不相同的电子.金属钛晶胞如图所示,为___________ 堆积(填堆积方式).

(2)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图.化合物乙的沸点明显高于化合物甲,主要原因是_____ .化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为_____ .

(3)钙钛矿晶体的结构如图所示.假设把氧离子看做硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,则一个钛离子被_____ 个氧离子包围.

II.碳是地球上组成生命的最基本元素之一,可以sp3、sp2和sp杂化轨道成共价键,具有很强的结合能力,与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。请回答下列问题:
(4)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?____________
(5)碳的一种同素异形体——C60,又名足球烯,是一种高度对称的球碳分子。立方烷(分子式:C8H8,结构是立方体: )是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
)是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为________ 。

(6)碳的另一种同素异形体——石墨,其晶体结构如上图所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为___________ 个。已知石墨的密度为ρg.cm-3 ,C-C键长为rcm,阿伏伽德罗常数的值为NA,计算石墨晶体的层间距为____________ cm。
(1)基态钛原子核外共有

(2)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图.化合物乙的沸点明显高于化合物甲,主要原因是

(3)钙钛矿晶体的结构如图所示.假设把氧离子看做硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,则一个钛离子被

II.碳是地球上组成生命的最基本元素之一,可以sp3、sp2和sp杂化轨道成共价键,具有很强的结合能力,与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。请回答下列问题:
(4)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
| 碳酸盐 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
(5)碳的一种同素异形体——C60,又名足球烯,是一种高度对称的球碳分子。立方烷(分子式:C8H8,结构是立方体:
 )是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
)是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
(6)碳的另一种同素异形体——石墨,其晶体结构如上图所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为
您最近一年使用:0次
名校
2 . 前四周期元素X、Y、Z、W的原子序数依次增大,X原子中有6个运动状态不同的电子,Y是地壳中含量最多的元素,基态Z原子K、L层上的电子总数是3p原子轨道上电子数的两倍,基态W原子中有6个未成对电子。下列说法不正确的是
A.电负性: ,原子半径: ,原子半径: |
| B.同周期中,元素Z的第一电离能最大 |
C.简单氢化物的沸点: |
D.在一定条件下,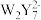 和 和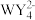 可以相互转化 可以相互转化 |
您最近一年使用:0次
名校
解题方法
3 . 磷及其化合物在电池、催化等领域有重要应用。黑磷与石墨类似,也具有层状结构(如图1)。为大幅度提高锂电池的充电速率,科学家最近研发了黑磷-石墨复合负极材料,其单层结构俯视图如图2所示。

回答下列问题:
(1)Li、C、P三种元素中,电负性最小的是___________ 。(用元素符号作答)
(2)基态磷原子价电子排布式为___________ 。
(3)图2石墨区中C原子的杂化方式为___________ 。
(4)氢化物 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为___________ 。
(5)根据图1和图2的信息,下列说法正确的有___________。(填字母)
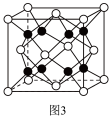
(6)贵金属磷化物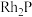 可用作电解水的高效催化剂,其立方晶胞如图3所示。晶体中与Rh距离最近的P的数目为
可用作电解水的高效催化剂,其立方晶胞如图3所示。晶体中与Rh距离最近的P的数目为___________

回答下列问题:
(1)Li、C、P三种元素中,电负性最小的是
(2)基态磷原子价电子排布式为
(3)图2石墨区中C原子的杂化方式为
(4)氢化物
 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为(5)根据图1和图2的信息,下列说法正确的有___________。(填字母)
| A.黑磷区中P-P键的键能完全相同 |
| B.黑磷与石墨都属于混合型晶体 |
| C.由石墨与黑磷制备该复合材料的过程,发生了化学反应 |
| D.复合材料单层中,P原子与C原子之间的作用力属范德华力 |
 可用作电解水的高效催化剂,其立方晶胞如图3所示。晶体中与Rh距离最近的P的数目为
可用作电解水的高效催化剂,其立方晶胞如图3所示。晶体中与Rh距离最近的P的数目为
您最近一年使用:0次
名校
4 . 下列说法不正确的是


| A.拟卤素(SCN)2对应的酸有两种,理论上异硫氰酸(H-N=C=S)的沸点高于硫氰酸(H-S-C≡N) |
| B.硫酸铜溶液中加入过量氨水生成[Cu(NH3)4]2+,NF3与NH3结构相似,NF3更易与Cu2+形成配离子 |
C.1mol的三种微粒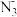 、OCN-和N2O,含有的π键数目均为2NA 、OCN-和N2O,含有的π键数目均为2NA |
| D.直链多磷酸盐的阴离子有多种,焦磷酸根离子、三磷酸根离子的结构如图所示,这类磷酸根离子可用通式(PnO3n+1)(n+2)-表示 |
您最近一年使用:0次
解题方法
5 . 下列关于物质结构与性质的说法,正确的是
| A.玻尔原子结构模型能够成功地解释各种原子光谱 |
B. 、 、 、 、 三种元素的电负性顺序为 三种元素的电负性顺序为 |
C. |
D.氨分子间存在氢键,故 的熔沸点及稳定性均大于 的熔沸点及稳定性均大于 |
您最近一年使用:0次
名校
6 . 下列说法中正确的是
| A.羧酸的pKa(pKa=-lgKa)越大,其酸性越强 |
| B.CF3COOH的酸性大于CCl3COOH,这与F、Cl元素的电负性大小有关 |
| C.CHCl2COOH的酸性大于CCl3COOH,这与Cl原子的数目有关 |
| D.烃基(R-)是推电子基团,随着烃基加长,羧酸的酸性差异越来越大 |
您最近一年使用:0次
2022-06-17更新
|
111次组卷
|
2卷引用:吉林省通化市2021-2022学年高二下学期期中联考化学试题
名校
解题方法
7 . 某化合物M结构简式如图所示,下列有关说法正确的是


| A.M中配体是N元素,中心原子是Fe原子 |
B.M中非金属元素的电负性由大到小的顺序是 |
| C.M中所含有的化学键类型有离子键、共价键、配位键、氢键 |
| D.M中非金属元素原子间形成的σ键和π键的数目比为13∶2 |
您最近一年使用:0次
2022-05-15更新
|
92次组卷
|
2卷引用:吉林省长春市实验中学2021-2022学年高二下学期线上教学诊断检测(二)化学试题
名校
解题方法
8 . 以下有关元素性质的说法不正确的是
| A.具有下列电子排布式的原子:①1s22s22p63s23p2②1s22s22p3③1s22s22p2④1s22s22p63s23p4,原子半径最大的是① |
| B.具有下列价电子排布式的原子:①3s23p1②3s23p2③3s23p3④3s23p4,第一电离能最大的是③ |
| C.①Na、K、Rb②N、P、S③Na、P、Cl,元素的电负性随原子序数增大而增大的是③ |
| D.某主族元素气态基态离子的逐级电离能数据(单位:kJ·mol-1)分别为738、1451、7733、10540、13630、17995、21703……它与氯气反应时,生成的阳离子是X3+ |
您最近一年使用:0次
2021-10-09更新
|
258次组卷
|
2卷引用:吉林省长春市清蒲中学2020-2021学年高二下学期期中考试化学试题
9 . 下列说法中正确的是
| A.12.4g白磷(分子式为P4,正四面体形,键角为60°)中含有P-P键为1.2NA |
| B.磷化铜(Cu3P2)用于制造磷青铜,电负性:Cu>P |
| C.某原子处于能量最低状态时,外围电子排布式为4d15s2,则该元素基态原子中第N层还有5个空轨道 |
| D.位于同一周期的甲、乙两种元素,甲位于第ⅠA族,原子序数为m,乙位于第ⅢA族,则乙原子序数可能为m+26 |
您最近一年使用:0次
2021-10-23更新
|
178次组卷
|
2卷引用:吉林省梅河口市第五中学2021-2022学年高二上学期期中考试化学试题
13-14高二上·江苏泰州·期中
名校
解题方法
10 . 如图是第三周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是
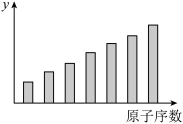
| A.y轴表示的可能是第一电离能 |
| B.y轴表示的可能是电负性 |
| C.y轴表示的可能是原子半径 |
| D.y轴表示的可能是形成基态离子转移的电子数 |
您最近一年使用:0次
2021-04-24更新
|
973次组卷
|
51卷引用:吉林省辽源市田家炳高级中学2018-2019学年高二下学期期中考试化学试题
吉林省辽源市田家炳高级中学2018-2019学年高二下学期期中考试化学试题吉林省长春市清蒲中学2020-2021学年高二下学期期中考试化学试题(已下线)2013-2014学年江苏省泰州市姜堰区高二上学期期中考试化学试卷2015-2016学年黑龙江省哈尔滨六中高二下期中化学试卷湖北省蕲春县2016-2017学年高二下学期期中考试化学试题山东师范大学附属中学2017-2018学年高二下学期期中考试(理)化学试题山东省师范大学附属中学2017-2018学年高二下学期第七次学分认定考试(期中)(理)化学试题【全国百强校】黑龙江省实验中学2017-2018学年高二下学期期中考试(理)化学试题河南省兰考县第二高级中学2017-2018学年高二下学期期中考试化学试题山西省阳泉市第二中学2018-2019学年高二下学期期中考试化学试题黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高二下学期期中考试化学试题宁夏回族自治区石嘴山市平罗中学2019-2020学年高二上学期期中考试化学试题四川省南充市白塔中学2019-2020学年高二上学期期中考试化学试题福建省福州市格致中学2018-2019学年高二下学期期中考试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题新疆维吾尔自治区乌鲁木齐市第四中学2020-2021学年高二年级下学期期中考试化学试题福建省漳州市正兴学校等三校2021-2022学年高二下学期期中联考化学试题甘肃省兰州第一中学2021-2022学年高二下学期期中考试化学试题新疆维吾尔自治区皮山县高级中学2022-2023学年高二下学期4月期中化学试题福建省南平市浦城县2022-2023学年高二下学期期中考试化学试题四川省阆中中学校2023-2024学年高二下学期4月期中化学试题2016-2017学年河南省商丘市第一高级中学高二上学期期末考试化学试卷2018版化学(苏教版)高考总复习专题十一课时跟踪训练--原子结构与元素的性质【全国百强校】山西省大同市第一中学2017-2018学年高二5月月考化学试题鲁科版高中化学选修3模块综合测评卷福建省平和县第一中学2018-2019学年高二下学期期末考试化学试题新疆阿勒泰地区第二高级中学2018-2019学年高二下学期期末(A卷)化学试题山东省济宁市2018-2019学年高二期末模块检测化学试题人教化学选修3第一章第二节课时5天津市第二十中学2019-2020学年高二下学期阶段性检测化学试题第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)福建省建瓯市芝华中学2019-2020学年高二下学期居家学习检测化学试题安徽省定远县育才学校2019-2020学年高一6月月考化学试题安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题福建省建瓯市芝华中学2019-2020学年高二下学期第一次阶段考试化学试题河南省洛阳市2019-2020学年高二下学期期末质量检测化学试题(已下线)第35讲 原子结构与性质(精练)-2021年高考化学一轮复习讲练测(已下线)第1章 原子结构与元素性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)福建省宁德市柘荣县第一中学2021-2022学年高二下学期月考八化学试题(已下线)专题13 原子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)新疆乌鲁木齐高级中学2021-2022学年高二上学期期末考试化学试题湖南省长沙市长郡梅溪湖中学2021-2022学年高二下学期入学考试化学试题河北省石家庄市第二十七中学2022-2023学年高三上学期九月月考化学试题新疆疏勒县实验学校2021-2022学年高二下学期期末考试化学试题陕西省西安市阎良区关山中学2021-2022学年高二下学期期末质量检测化学试题重庆市缙云教育联盟2022-2023学年高二上学期期末联考化学试题黑龙江省大庆市大庆中学2022-2023学年高二下学期4月月考化学试题重庆市2022-2023学年高二上学期期末考试化学试题(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)天津市九十六中学2023-2024学年高三上学期12月月考化学试题(已下线)清单01 原子结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)



