名校
1 . (1)如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。

①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围在哪两种元素之间为_____ (填元素符号);
②图中第一电离能最小的元素在周期表中的位置是___________ 。
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①通过分析电负性值变化规律,确定Mg元素电负性值的最小范围________ ;
②判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2 C.AlCl3 D.SiC
Ⅰ.属于离子化合物的是_____ ;Ⅱ.属于共价化合物的是____ ;请设计一个实验方案证明上述所得到的结论____

①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围在哪两种元素之间为
②图中第一电离能最小的元素在周期表中的位置是
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①通过分析电负性值变化规律,确定Mg元素电负性值的最小范围
②判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2 C.AlCl3 D.SiC
Ⅰ.属于离子化合物的是
您最近一年使用:0次
名校
解题方法
2 . 已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+ 原子核外有3层电子且M层3d轨道电子全充满。请回答:
(1)E元素基态原子的电子排布式为_________ 。
(2)B、C、D三种元素的第一电离能数值由小到大 的顺序为____ (填元素符号)
(3)D元素与氟元素相比,电负性:D______ F(填“>”、“=”或“<”),下列表述中能证明这一事实的是_______ (填选项序号)
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物,其电子式为______ ,它的晶体中含有多种化学键,但一定不含有的化学键是______ (填选项序号)。
A.极性键 B.非极性键 C.离子键 D.金属键
(5)B2A4是重要的基本石油化工原料。lmolB2A4分子中含 键
键______ mol。
(1)E元素基态原子的电子排布式为
(2)B、C、D三种元素的第一电离能数值由
(3)D元素与氟元素相比,电负性:D
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物,其电子式为
A.极性键 B.非极性键 C.离子键 D.金属键
(5)B2A4是重要的基本石油化工原料。lmolB2A4分子中含
 键
键
您最近一年使用:0次
名校
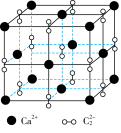
3 . 下列说法错误的是
| A.CO2与SiO2的键角相等 |
| B.SiH4、CO2均是由极性键构成的非极性分子 |
| C.HCNO中元素的电负性:O>N>C>H |
| D.CaC2晶胞如图所示,Ca2+的配位数为6 |
您最近一年使用:0次
4 . 硫代硫酸钠(Na2S2O3)是常用的化学试剂,反应的化学方程式为AgBr+2Na2S2O3=Na3[Ag(S2O3)2]+NaBr,产物中的Na3[Ag(S2O3)2]常用于切花保鲜。下列说法错误的是
| A.基态Na+的核外电子存在10种运动状态 |
| B.此化学方程式中涉及的S、Na、O三元素的电负性由小到大的顺序为O>S>Na |
| C.欲测定切花保鲜液中Na3[Ag(S2O3)2]的浓度,可用NaCl标准溶液滴定Ag+ |
| D.NaBr的晶体结构与NaCl晶体相似,每个Br-周围有6个Na+ |
您最近一年使用:0次
名校
解题方法
5 . 短周期元素 X、Y、Z原子序数依次增大,X元素基态原子有2个未成对电子,Y 元素基态原子的核外p电子数比s电子数少1个,Z的一种“超原子” ( )具有40个价电子,下列说法错误的是
)具有40个价电子,下列说法错误的是
 )具有40个价电子,下列说法错误的是
)具有40个价电子,下列说法错误的是| A.第一电离能: Y<Z | B.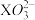 的空间结构为平面三角形 的空间结构为平面三角形 |
C.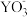 中心原子的杂化方式为sp2杂化 中心原子的杂化方式为sp2杂化 | D.X、Y、Z的电负性; Y>X>Z |
您最近一年使用:0次
2024-04-26更新
|
74次组卷
|
2卷引用:福建省福州第二中学2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
6 . 一种合成药物结构如图,下列有关说法不正确的是
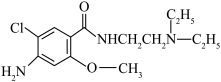
| A.分子中碳原子有2种杂化类型 |
| B.组成元素的电负性由大到小的顺序为O>N>C>H |
| C.该分子中有手性碳因而分子具有旋光性 |
| D.分子中所有氮原子上都有1对孤电子对 |
您最近一年使用:0次
2024-03-30更新
|
217次组卷
|
2卷引用:福建省泉州市永春第一中学2023-2024学年高二下学期4月期中考试化学试题
名校
7 . 某电池的电解液部分微观结构如图,“---”表示微粒间存在较强静电作用。M、N、W、X、Y、Z为原子序数依次增大的短周期元素。下列说法错误的是
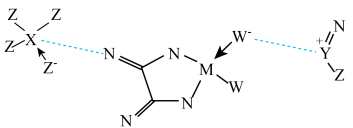
A.未成对电子数: | B.电负性: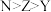 |
C.最简单氢化物的沸点: | D.熔点: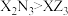 |
您最近一年使用:0次
2024-03-07更新
|
346次组卷
|
3卷引用:福建省福州第二中学2023-2024学年高二下学期4月期中考试化学试题
名校
8 . 碳、硫、氧、氮是中学常见元素,下列说法不正确的是
A. 、 、 、 、 都是直线形分子 都是直线形分子 |
B. 、 、 、 、 的键角依次减小 的键角依次减小 |
C. 、 、 分子的中心原子都是 分子的中心原子都是 化 化 |
| D.C、N、F元素的电负性依次增大 |
您最近一年使用:0次
2023-06-08更新
|
151次组卷
|
5卷引用:福建省三明市四地四校2021-2022学年高二下学期期中联考化学试题
名校
9 . 离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子结构如图所示,下列有关EMTM+的说法正确的是


| A.该离子中碳原子杂化类型均为sp3 |
| B.该离子中存在类似苯中的大π键,5元环上的5个原子共用6个电子 |
| C.该离子可与Cl-结合形成有18个σ键的离子化合物 |
| D.该离子中所含元素电负性:C>N>H |
您最近一年使用:0次
名校
10 . 已知氯化1-乙基-3-甲基咪唑(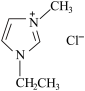 )被广泛应用于有机合成和聚合反应、分离与提纯以及电化学研究中。下列说法错误的是
)被广泛应用于有机合成和聚合反应、分离与提纯以及电化学研究中。下列说法错误的是
A.电负性: |
B.五元环处于同一平面,则两个氮原子的杂化方式都为 |
C. 氯化1-乙基-3-甲基咪唑中含有 氯化1-乙基-3-甲基咪唑中含有 键数目为 键数目为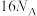 |
| D.氯化1-乙基-3-甲基咪唑中的化学键类型:离子键、共价键 |
您最近一年使用:0次
2023-03-09更新
|
703次组卷
|
5卷引用:福建省福建师范大学附属中学2022-2023学年高二下学期期中考试化学试题



