22-23高三下·福建泉州·阶段练习
解题方法
1 . 点击化学(click chemistry)是一种能够让分子的构建模块快速、高效地结合在一起的化学反应。科学工作者可以利用基础模块搭建出变化无穷的造型,就如同玩乐高玩具一般。叠氨化物和块经合成抗真菌药物三唑是点击化学的重要应用,反应示例如下:
 +CH3CH2N3
+CH3CH2N3

 +CH3CH2N3→
+CH3CH2N3→
回答下列问题:
(1) 的核外电子排布式为
的核外电子排布式为_______ 。
(2)C、N、Cu的电负性由大到小的顺序为_______ 。
(3)分子乙中存在5中心6电子的大 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是_______ (填对应原子的序号)。
(4)分子中碳碳三键的活泼性:甲_______ 丙(填“>”“=”“<”),理由是_______ (从分子的结构角度分析)。
(5)丁形成的晶体中不存在的微粒间作用力有_______ 。
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中, 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。

① 的配位数为
的配位数为_______ 。
②由 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为_______ 。
 +CH3CH2N3
+CH3CH2N3

 +CH3CH2N3→
+CH3CH2N3→
回答下列问题:
(1)
 的核外电子排布式为
的核外电子排布式为(2)C、N、Cu的电负性由大到小的顺序为
(3)分子乙中存在5中心6电子的大
 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是(4)分子中碳碳三键的活泼性:甲
(5)丁形成的晶体中不存在的微粒间作用力有
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中,
 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。
①
 的配位数为
的配位数为②由
 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为
您最近一年使用:0次
2 . 下表是前20号元素中的部分元素的一些数据:
试回答下列问题:
(1)以上10种元素电负性最大的是_____ (填元素符号)。比元素B原子序数大7的元素在元素周期表中的位置:第_____ 周期,第_____ 族,其基态原子的核外电子排布式是________ 。
(2)H、I、J三种元素对应单质的熔点依次升高的顺序是(用单质的具体化学式排序)__________ 。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其分子中共形成________ 个σ键,________ 个π键。
(4)I与氢元素形成的10电子分子X的空间构型为________ ;将X溶于水后的溶液滴入到CuSO4溶液中至过量,得到的络离子的化学式为________ ,其中X与Cu2+之间以_____________ 键结合。
(5)下图是I元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
a._________________________________ 。
b._________________________________ 。

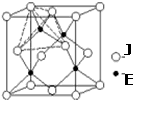
(6)如图是J和E组成的晶体结构,则每个与J周围最近J原子数目为_________ ,若晶胞边长为a cm,则晶体的密度为_______________ (用含a、NA的代数式表示)(g/mL)。
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)以上10种元素电负性最大的是
(2)H、I、J三种元素对应单质的熔点依次升高的顺序是(用单质的具体化学式排序)
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其分子中共形成
(4)I与氢元素形成的10电子分子X的空间构型为
(5)下图是I元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
a.
b.

(6)如图是J和E组成的晶体结构,则每个与J周围最近J原子数目为

您最近一年使用:0次
2017-12-20更新
|
309次组卷
|
3卷引用:2020届高三化学二轮选修大题必练—— 物质结构与性质大题练



