名校
解题方法
1 . 运用物质结构与性质的相关知识,回答下列问题:
(1) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是_______ 。基态 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有_____ 个伸展方向,原子轨道呈______ 形。
(2) 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为________ , 价电子轨道表示式为
价电子轨道表示式为________ 。
(3) 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
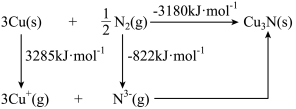
通过图中数据________ (填“能”或“不能”)计算出 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为________  。
。
(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。
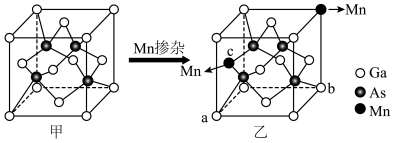
①GaAs晶胞中距离Ga原子最近As原子的个数为________ 。
②掺杂 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为________ (化为最简整数比)。
(1)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有(2)
 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为 价电子轨道表示式为
价电子轨道表示式为(3)
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
通过图中数据
 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为 。
。(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①GaAs晶胞中距离Ga原子最近As原子的个数为
②掺杂
 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为
您最近一年使用:0次
名校
解题方法
2 . 咔唑(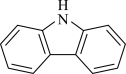 )是一种新型有机液体储氢介质。下列说法错误的是
)是一种新型有机液体储氢介质。下列说法错误的是
 )是一种新型有机液体储氢介质。下列说法错误的是
)是一种新型有机液体储氢介质。下列说法错误的是| A.电负性:N>C>H |
| B.同周期元素中第一电离能小于N的有4种 |
C.咔唑的沸点比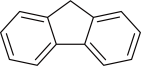 的沸点高 的沸点高 |
D.基态氮原子的外围电子轨道表示式不能写为 ,因为违背了洪特规则原理 ,因为违背了洪特规则原理 |
您最近一年使用:0次
2023-09-22更新
|
121次组卷
|
3卷引用:福建省泉州市部分中学2022-2023学年高二下学期期末联考化学试题
3 . 实验室用邻二氮菲(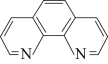 )与
)与 形成的红色配合离子(图1)测定
形成的红色配合离子(图1)测定 的浓度。回答下列问题:
的浓度。回答下列问题:

(1)Fe元素在周期表中的位置为__________ ,该配合物中心离子的配位数为__________ 。
(2)该配合离子所含元素的电负性最大的是__________ ,C原子的杂化方式为__________ 。
(3)该配合离子存在的化学键类型有__________ 。
a.离子键 b.配位键 c.极性键 d.非极性键 e.金属键 f.氢键
(4)从结构角度分析, 易被氧化成
易被氧化成 的原因是
的原因是__________ 。
(5)合成氨反应中铁催化剂表面吸附氮原子,图2为氮原子在铁的晶面上的单层附着局部示意图,图中铁原子与氮原子的个数比为__________ 。
(6)铁晶体中的原子堆积方式如图3所示, 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为 ,若晶胞密度为
,若晶胞密度为 ,则
,则
__________ (列出表达式)。
 )与
)与 形成的红色配合离子(图1)测定
形成的红色配合离子(图1)测定 的浓度。回答下列问题:
的浓度。回答下列问题:
(1)Fe元素在周期表中的位置为
(2)该配合离子所含元素的电负性最大的是
(3)该配合离子存在的化学键类型有
a.离子键 b.配位键 c.极性键 d.非极性键 e.金属键 f.氢键
(4)从结构角度分析,
 易被氧化成
易被氧化成 的原因是
的原因是(5)合成氨反应中铁催化剂表面吸附氮原子,图2为氮原子在铁的晶面上的单层附着局部示意图,图中铁原子与氮原子的个数比为
(6)铁晶体中的原子堆积方式如图3所示,
 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为 ,若晶胞密度为
,若晶胞密度为 ,则
,则
您最近一年使用:0次
名校
解题方法
4 . 氧化锌晶体常用于液晶显示器,该晶体可用醋酸锌[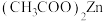 ]为原料在高温下分解制得。下列说法不正确的是
]为原料在高温下分解制得。下列说法不正确的是
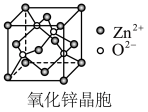
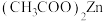 ]为原料在高温下分解制得。下列说法不正确的是
]为原料在高温下分解制得。下列说法不正确的是
A.ZnO中 的配位数为4 的配位数为4 |
| B.ZnO、ZnS均为离子晶体,ZnO的熔点低于ZnS |
C.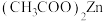 中非金属元素电负性: 中非金属元素电负性: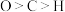 |
D.若氧化锌晶胞参数为a,则两个 的最近距离为 的最近距离为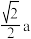 |
您最近一年使用:0次
名校
解题方法
5 .  是重要的还原剂,合成方法:
是重要的还原剂,合成方法: 。下列说法正确的是
。下列说法正确的是
 是重要的还原剂,合成方法:
是重要的还原剂,合成方法: 。下列说法正确的是
。下列说法正确的是A.半径大小: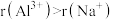 | B.电负性大小: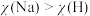 |
C.第一电离能: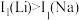 | D.碱性强弱: |
您最近一年使用:0次
2023-01-19更新
|
363次组卷
|
3卷引用:福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题
福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题江苏省南通市海安市2022-2023学年高三上学期1月期末考试化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题1-5)
解题方法
6 . 一水合甘氨酸锌是一种矿物类饲料添加剂,其结构简式如图所示。下列说法错误的是


A.基态Zn原子价电子排布式为 |
B.Cu与Zn相邻,第一电离能: |
C.该物质中, 的配位数为5,配原子为O、N 的配位数为5,配原子为O、N |
D.电负性由小到大的顺序为 |
您最近一年使用:0次
2022-09-24更新
|
571次组卷
|
3卷引用:福建省泉州科技中学2021-2022学年高二下学期期末考试化学试题
解题方法
7 . 建盏由建阳坯土、天然矿物釉烧制,含有SiO2、Al2O3、Fe2O3、FeO、CaO、TiO2等化学成分。
(1)现代化学可利用_______ 特征谱线来鉴定建盏中的元素。
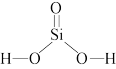
(2)建盏胎釉中含SiO2是硅酸的酸酐。硅酸结构式如图所示,硅原子的杂化方式_______ 。
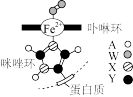
(3)Fe2+与蛋白质链上咪唑环通过配位键连接形成的物质结构如图所示。A、W、X、Y为短周期前10号主族元素。四种元素的电负性由大到小的顺序为_______ (用元素符号表示)。
(4)元素Fe在周期表中的位置为_______ ;其第三电离能(I3)为2957 KJ· mol-1、第四电离能(I4)为5290 KJ· mol-1,I4远大于I3的原因为_______ 。
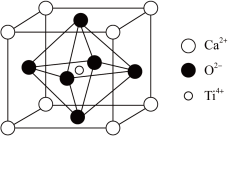
(5)建盏胎釉矿石中的钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的_______ 空隙中,在钙钛矿晶胞结构的另一种表示中,Ti4+处于各顶角位置,则O2-处于_______ 位置(选填“面心”“体心”或“棱心”)。已知晶胞密度为 ρ g∙cm-3,则两个O2-离子间的最短距离为_______ nm(阿伏加德罗常数的值为NA,列出表达式)。
(1)现代化学可利用
(2)建盏胎釉中含SiO2是硅酸的酸酐。硅酸结构式如图所示,硅原子的杂化方式

(3)Fe2+与蛋白质链上咪唑环通过配位键连接形成的物质结构如图所示。A、W、X、Y为短周期前10号主族元素。四种元素的电负性由大到小的顺序为

(4)元素Fe在周期表中的位置为
(5)建盏胎釉矿石中的钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的

您最近一年使用:0次
解题方法
8 . Al、Fe、Cu是重要的材料元素,在生产生活中有着广泛的应用。回答下列问题:
(1)Fe4[Fe(CN)6]3是较早发现的CN-配合物,其中铁元素呈现两种不同的价态。配离子的中心原子核外电子排布式为___ 。
(2)铁单质在一定条件下可与CO反应生成配位化合物——羰基铁[Fe(CO)5],沸点102.8℃,熔点-21℃,羰基铁[Fe(CO)5]属于___ 晶体。从电负性角度分析,Fe(CO)5中与Fe形成配位键的是原子___ (填名称)。
(3)已知Al的第一电离能为578 kJ/mol、第二电离能为1817 kJ/mol、第三电离能为2745 kJ/mol、第四电离能为11575 kJ/mol。请解释其第二电离能增幅较大的原因___ 。
(4)甲醇重整制氢反应中,铜基催化剂如CuO/SiO2具有重整温度低、催化选择性高的优点。Cu、Si、O元素电负性由大到小的顺序是___ ;SiO2中Si原子采取___ 杂化。
(5)金刚砂(SiC)晶胞如图所示:
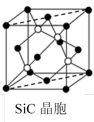
沿晶胞图中虚线方向的切面图为___ (填标号)。
a.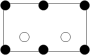 b.
b.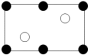
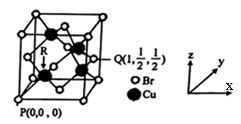
(6)一种铜的溴化物晶胞结构如图所示,该晶胞中铜的配位数是___ ,由图中P点和Q点的原子坐标参数可确定R点的原子坐标参数为___ ;已知晶胞参数为a pm,其密度为___ g/cm3。(列出计算式即可)
(1)Fe4[Fe(CN)6]3是较早发现的CN-配合物,其中铁元素呈现两种不同的价态。配离子的中心原子核外电子排布式为
(2)铁单质在一定条件下可与CO反应生成配位化合物——羰基铁[Fe(CO)5],沸点102.8℃,熔点-21℃,羰基铁[Fe(CO)5]属于
(3)已知Al的第一电离能为578 kJ/mol、第二电离能为1817 kJ/mol、第三电离能为2745 kJ/mol、第四电离能为11575 kJ/mol。请解释其第二电离能增幅较大的原因
(4)甲醇重整制氢反应中,铜基催化剂如CuO/SiO2具有重整温度低、催化选择性高的优点。Cu、Si、O元素电负性由大到小的顺序是
(5)金刚砂(SiC)晶胞如图所示:

沿晶胞图中虚线方向的切面图为
a.
 b.
b.
(6)一种铜的溴化物晶胞结构如图所示,该晶胞中铜的配位数是

您最近一年使用:0次
名校
9 . 下列叙述正确的是
| A.钾原子由激发态转变为基态可获得吸收光谱 |
B.磷化铜(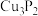 )用于制造磷青铜,电负性: )用于制造磷青铜,电负性: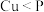 |
C.用原子轨道描述氢分子中化学键的形成: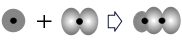 |
D.俗称光气的二氯甲醛(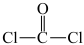 )分子中 )分子中 键角恰好为 键角恰好为 |
您最近一年使用:0次
2021-07-20更新
|
225次组卷
|
3卷引用:福建省宁德市2020-2021学年高二下学期期末考试化学试题
解题方法
10 . 目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。回答下列问题:
(1)镍能形成很多配合物,其中一种配合物二丁二酮肟合镍(Ⅱ)的结构如下图。
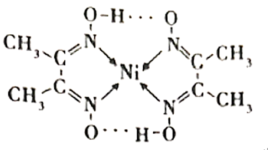
①基态Ni原子的电子排布式为___________ ,该元素在元素周期表中的位置是___________ 。
②元素C、N、O的电负性由大到小顺序为___________ 。
③二丁二酮肟合镍中存在的化学键有___________ (填标号)。
A.共价键 B.配位键 C.氢键 D.离子键 E.范德华力
④二丁二酮肟合镍中氮原子的杂化类型为___________ 。
(2)工业上采用反应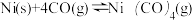 提纯粗镍,Ni(CO)4是呈正四面体形的配合物,0.5 mol Ni(CO)4中含有
提纯粗镍,Ni(CO)4是呈正四面体形的配合物,0.5 mol Ni(CO)4中含有___________ 个δ键。
(3)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下。
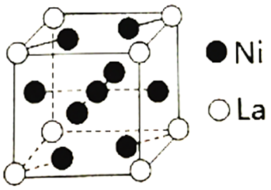
①测知镧镍合金晶胞边长为anm,则镧镍合金的晶体密度为___________ g·cm-3。
②若储氢后,氢原子占据晶胞上下底面的面心及棱的中点,则形成的储氢化合物的化学式为___________ 。
(1)镍能形成很多配合物,其中一种配合物二丁二酮肟合镍(Ⅱ)的结构如下图。

①基态Ni原子的电子排布式为
②元素C、N、O的电负性由大到小顺序为
③二丁二酮肟合镍中存在的化学键有
A.共价键 B.配位键 C.氢键 D.离子键 E.范德华力
④二丁二酮肟合镍中氮原子的杂化类型为
(2)工业上采用反应
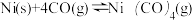 提纯粗镍,Ni(CO)4是呈正四面体形的配合物,0.5 mol Ni(CO)4中含有
提纯粗镍,Ni(CO)4是呈正四面体形的配合物,0.5 mol Ni(CO)4中含有(3)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下。

①测知镧镍合金晶胞边长为anm,则镧镍合金的晶体密度为
②若储氢后,氢原子占据晶胞上下底面的面心及棱的中点,则形成的储氢化合物的化学式为
您最近一年使用:0次



