(1)镍元素位于周期表第
(2)在CO分子中,C与O之间形成
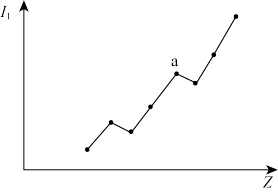
(3)第二周期元素的第一电离能(I1)随原子序数(Z)的变化情况如图。I1随Z的递增而呈增大趋势的原因是
(4)VA族元素及其化合物在生产、生活中用途广泛。如P4S3常用于制造火柴,As4S4俗称雄黄,那么
①P、S、As电负性由大到小的顺序是
②NH3、PH3、AsH3中沸点最高的是
| A.SO2、SO3都是极性分子 |
B.在 和[Cu(NH3)4]2+中都存在配位键 和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.CO可以和很多金属形成配合物,如Ni(CO)2,Ni与CO之间的键型为配位键 |
3 . 2019年10月1日,在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的DF—31a洲际战略导弹是我国大国地位,国防实力的显著标志,其制作材料中包含了Fe、Cr、Ni、C等多种元素,回答下列问题:
①基态铬原子的价电子排布式为
②Fe和Ni都能与CO形成配合物Fe(CO)5和Ni(CO)4。
(i)电负性比较:C
(ii)写出与CO互为等电子体的分子的电子式
(iii)Ni(CO)4的沸点为43℃,Fe(CO)5的沸点为103℃,请说明Fe(CO)5沸点更高的原因:
③金刚石晶胞如图所示,A、B坐标参数分别为A(0,0,0),B(1,1,1),则距离A位置最近的原子坐标参数为

④Ni可以形成多种氧化物,其中一种NiaO晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别是Ni2+、Ni3+,则晶体中Ni2+与Ni3+的最简整数比为
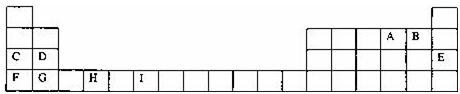
请回答下列问题:
(1)元素I的元素符号 ;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的 周期 族.
(2)表中元素第一电离能最小的是 (填元素符号,下同),电负性最大的是 ,化学性质最稳定的是 .
(3)表中元素处于d区的是 (填元素符号).
(4)请举出F的金属性比C强的实验事实: ,并用原子结构理论解释其原因: .
| A.原子半径的周期性变化 |
| B.电负性的周期性变化 |
| C.第一电离能的周期性变化 |
| D.原子核外电子排布的周期性变化 |
| A.Na、Mg、Al的第一电离能逐渐增大 |
| B.V、Cr、Mn的最外层电子数逐渐增大 |
| C.S2﹣、Cl﹣、K+的半径逐渐减小 |
| D.O、F、Ne的电负性逐渐增大 |



