名校
1 . 根据要求回答下列问题:
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是_________ 。
(2)①O2- ②Al3+ ③Cl- ④Ca2+的半径由大到小排列为:________ (用序号表示)。
(3)下列属于氧原子激发态的轨道表示式的有___________ (填字母)。_________ ,位于在周期表______ 区(填s、p、d或ds)。
(5)基态Si原子中,电子占据的最高能层符号为________ 。
(6)基态S原子的原子核外电子有______ 种空间运动状态,其能量最高的电子电子云轮廓图为______ 形。
(7)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:________ 。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)①O2- ②Al3+ ③Cl- ④Ca2+的半径由大到小排列为:
(3)下列属于氧原子激发态的轨道表示式的有
a.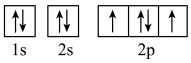 b.
b.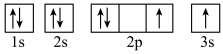
c.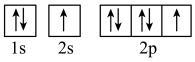 d.
d.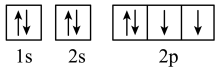
(5)基态Si原子中,电子占据的最高能层符号为
(6)基态S原子的原子核外电子有
(7)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
您最近一年使用:0次
2024-02-07更新
|
327次组卷
|
3卷引用:山东省济南市历城第二中学2023-2024学年高二上学期期末化学模拟试题
2 . 铬是一种重要的元素,在合金、电镀、鞣制领域都有重要的应用, 的配位能力很强,可以形成多种配离子。
的配位能力很强,可以形成多种配离子。
(1)基态Cr原子价层电子的轨道表达式为__________ ,同周期元素的基态原子最外层电子数与Cr相同的元素有__________ 种。
(2) 是最重要的铬(Ⅲ)盐之一,阴离子
是最重要的铬(Ⅲ)盐之一,阴离子 的空间构型为
的空间构型为__________ ,基态S原子核外电子中成对电子数和未成对电子数之比为__________ 。
(3)NH3、H2O、 都是常见的配体,以上配体中所含元素的电负性由大到小的顺序是
都是常见的配体,以上配体中所含元素的电负性由大到小的顺序是____________________ 。
(4) 中
中 键的数目为
键的数目为__________ ,基态N原子电子占据最高能级的电子云轮廓图为__________ 形。
(5)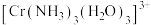 中配体
中配体 的杂化类型是
的杂化类型是__________ , 的键角
的键角__________  的键角(填“大于”、“小于”或“等于”),判断依据是
的键角(填“大于”、“小于”或“等于”),判断依据是______________________________ 。
 的配位能力很强,可以形成多种配离子。
的配位能力很强,可以形成多种配离子。(1)基态Cr原子价层电子的轨道表达式为
(2)
 是最重要的铬(Ⅲ)盐之一,阴离子
是最重要的铬(Ⅲ)盐之一,阴离子 的空间构型为
的空间构型为(3)NH3、H2O、
 都是常见的配体,以上配体中所含元素的电负性由大到小的顺序是
都是常见的配体,以上配体中所含元素的电负性由大到小的顺序是(4)
 中
中 键的数目为
键的数目为(5)
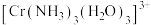 中配体
中配体 的杂化类型是
的杂化类型是 的键角
的键角 的键角(填“大于”、“小于”或“等于”),判断依据是
的键角(填“大于”、“小于”或“等于”),判断依据是
您最近一年使用:0次
2024-02-01更新
|
270次组卷
|
2卷引用:山东省德州市2023-2024学年高二上学期期末考试化学试题
名校
解题方法
3 . 下列说法不正确的是
| A.石墨片层中存在大π键,所以沿片层方向容易导电 |
| B.苯甲酸容易形成分子间氢键,形成二聚分子,所以熔沸点较高 |
| C.碳链可以连接很长,但硅链不可以连接很长,因为Si-Si键的键能小于C-C键的键能 |
| D.依据元素周期律,与相同浓度的稀硫酸反应,Pb比Sn反应剧烈 |
您最近一年使用:0次
2024-01-13更新
|
266次组卷
|
3卷引用:山东省中学联盟2023-2024学年高三上学期12月全省大联考化学试题
山东省中学联盟2023-2024学年高三上学期12月全省大联考化学试题(已下线)化学(九省联考考后提升卷,甘肃卷)-2024年1月“九省联考”真题完全解读与考后提升河南省信阳高级中学2023-2024学年高二下学期开学化学试题
名校
解题方法
4 . X、Q、Y、Z、W、M、R、T是原子半径依次增大的前四周期元素,基态R原子核外电子有9种空间运动状态,并有2个单电子;基态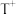 的d轨道半充满。由上述元素中的六种组成的一种化合物常作为“相转移催化剂”被广泛应用于有机合成中,其结构简式如图Ⅰ所示。
的d轨道半充满。由上述元素中的六种组成的一种化合物常作为“相转移催化剂”被广泛应用于有机合成中,其结构简式如图Ⅰ所示。
(1)基态R原子的价电子排布式为_______ 的,第一电离能小于R的同周期元素有_______ 种。
(2) 的结构如图Ⅱ所示,分子中存在大
的结构如图Ⅱ所示,分子中存在大 键
键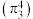 ,比较键长:①
,比较键长:①_______ ②(填“>”“<”或“=”),理由是_______ 。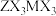 分子中M原子的杂化方式为
分子中M原子的杂化方式为_______ ,熔点比
_______ (填“高”或“低”); 中T的化合价为
中T的化合价为 ,且含有4个
,且含有4个 价的Y,则该分子中
价的Y,则该分子中 键与
键与 键的个数比为
键的个数比为_______ 。
(4)53号元素A的电负性与W近似相等,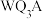 水解反应的产物为
水解反应的产物为_______ 。
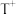 的d轨道半充满。由上述元素中的六种组成的一种化合物常作为“相转移催化剂”被广泛应用于有机合成中,其结构简式如图Ⅰ所示。
的d轨道半充满。由上述元素中的六种组成的一种化合物常作为“相转移催化剂”被广泛应用于有机合成中,其结构简式如图Ⅰ所示。
(1)基态R原子的价电子排布式为
(2)
 的结构如图Ⅱ所示,分子中存在大
的结构如图Ⅱ所示,分子中存在大 键
键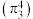 ,比较键长:①
,比较键长:①
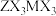 分子中M原子的杂化方式为
分子中M原子的杂化方式为
 中T的化合价为
中T的化合价为 ,且含有4个
,且含有4个 价的Y,则该分子中
价的Y,则该分子中 键与
键与 键的个数比为
键的个数比为(4)53号元素A的电负性与W近似相等,
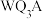 水解反应的产物为
水解反应的产物为
您最近一年使用:0次
2023-12-03更新
|
316次组卷
|
3卷引用:2024届山东省临沂市高三11月教学质量检测考试 化学
2024届山东省临沂市高三11月教学质量检测考试 化学四川省宜宾市叙州区第一中学校2023-2024学年高二上学期12月月考化学试题(已下线)通关练06 元素位-构-性推断-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
解题方法
5 . 布洛芬(Ibuprofen,空间填充模型如图所示)为解热镇痛类,非甾体抗炎药。下列叙述不正确的是
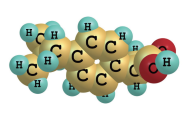

| A.组成元素电负性由大到小:O>C>H |
| B.分子结构中一定存在含氧官能团 |
| C.3种组成元素的价电子轨道均为哑铃形 |
| D.分子中存在极性键和非极性键 |
您最近一年使用:0次
解题方法
6 . 铜可以形成许多结构和性质特殊的化合物或合金。回答下列问题:
(1)基态铜原子价电子的轨道表示式为___________ ;同周期中与铜原子未成对电子数相同的元素有___________ 种。
(2)含H2O2的稀硫酸溶解铜可得到CuSO4溶液,通入氨气先形成蓝色沉淀然后溶解得到深蓝色 溶液。
溶液。
①H、N、O、S四种元素的电负性由大到小的顺序为___________ ;其中第一电离能最大的为___________ (填元素名称)。
②液态NH3与液态H2O2中存在的分子间作用力类型___________ (填“完全相同”或“部分相同”);NH3分子中 小于
小于 中的
中的 的原因为
的原因为___________ 。
③ 溶液中Cu2+的存在形式为
溶液中Cu2+的存在形式为 ,则铜的杂化方式可能为
,则铜的杂化方式可能为___________ (填标号)。
A. B.
B. C.
C. D.
D.
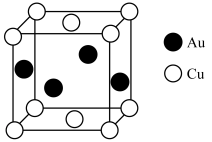
(3)已知: 为阿伏加德罗常数的值。铜与金(Au)可形成一种具有有序结构的储氢合金,其晶胞采取面心立方最密堆积方式,结构如图所示,该晶胞参数为anm。该合金晶胞密度为
为阿伏加德罗常数的值。铜与金(Au)可形成一种具有有序结构的储氢合金,其晶胞采取面心立方最密堆积方式,结构如图所示,该晶胞参数为anm。该合金晶胞密度为___________ g·cm-3(用含a、 的式子表示,列出计算式即可);晶胞中铜原子与金原子以原子数之比为1:1可以形成四面体,四面体空隙中填充氢原子后化学式为H4CuAu,则四面体空隙的填充率为
的式子表示,列出计算式即可);晶胞中铜原子与金原子以原子数之比为1:1可以形成四面体,四面体空隙中填充氢原子后化学式为H4CuAu,则四面体空隙的填充率为___________ 。
(1)基态铜原子价电子的轨道表示式为
(2)含H2O2的稀硫酸溶解铜可得到CuSO4溶液,通入氨气先形成蓝色沉淀然后溶解得到深蓝色
 溶液。
溶液。①H、N、O、S四种元素的电负性由大到小的顺序为
②液态NH3与液态H2O2中存在的分子间作用力类型
 小于
小于 中的
中的 的原因为
的原因为③
 溶液中Cu2+的存在形式为
溶液中Cu2+的存在形式为 ,则铜的杂化方式可能为
,则铜的杂化方式可能为A.
 B.
B. C.
C. D.
D.
(3)已知:
 为阿伏加德罗常数的值。铜与金(Au)可形成一种具有有序结构的储氢合金,其晶胞采取面心立方最密堆积方式,结构如图所示,该晶胞参数为anm。该合金晶胞密度为
为阿伏加德罗常数的值。铜与金(Au)可形成一种具有有序结构的储氢合金,其晶胞采取面心立方最密堆积方式,结构如图所示,该晶胞参数为anm。该合金晶胞密度为 的式子表示,列出计算式即可);晶胞中铜原子与金原子以原子数之比为1:1可以形成四面体,四面体空隙中填充氢原子后化学式为H4CuAu,则四面体空隙的填充率为
的式子表示,列出计算式即可);晶胞中铜原子与金原子以原子数之比为1:1可以形成四面体,四面体空隙中填充氢原子后化学式为H4CuAu,则四面体空隙的填充率为
您最近一年使用:0次
名校
7 . 过渡元素镍(Ni)、铬(Cr)都是重要的合金元素,他们的配合物在科技生活中都有很重要的应用,例如我国科学家合成铬的化合物通过烷基铝和[ph3C]+[B(C6F5)4]-活化后,对乙烯聚合表现出较好的催化活性。合成铬的化合物过程中的一步反应为:

回答下列问题:
(1)Cr3+价电子核外电子排布式为______ ,分子甲中除铬外其他元素的电负性由大到小依次为______ (填元素符号)。
(2)一定条件下环戊二烯 可转化为
可转化为 ,在这个过程中C原子的杂化方式变化为由sp3变为
,在这个过程中C原子的杂化方式变化为由sp3变为_____ , 中大π键可表示为
中大π键可表示为_____ 。
(3)化合物丙中1、2、3、4处的化学键是配位键的是_______ 。
a.只有2 b.2、3、4 c.全部都是
(4)AsCl3也可以与铬离子形成配合物,当氯原子被烷基取代后,配位能力增强,其原因是__________ 。
(5)水在合成铬的化合物的过程中作溶剂。研究表明水能凝结成13种类型的结晶体。重冰(密度比水大)属于立方晶系,其立方晶胞沿x、y或z轴的投影图如图所示,晶体中H2O的配位数为_________ 。
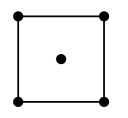
(6)一种由镍、氟、钾三种元素组成的化合物晶胞结构如图所示,原子A、B之间的距离是_________ (用字母a、b、c表示),晶胞中镍的分数坐标有____ 种。


回答下列问题:
(1)Cr3+价电子核外电子排布式为
(2)一定条件下环戊二烯
 可转化为
可转化为 ,在这个过程中C原子的杂化方式变化为由sp3变为
,在这个过程中C原子的杂化方式变化为由sp3变为 中大π键可表示为
中大π键可表示为(3)化合物丙中1、2、3、4处的化学键是配位键的是
a.只有2 b.2、3、4 c.全部都是
(4)AsCl3也可以与铬离子形成配合物,当氯原子被烷基取代后,配位能力增强,其原因是
(5)水在合成铬的化合物的过程中作溶剂。研究表明水能凝结成13种类型的结晶体。重冰(密度比水大)属于立方晶系,其立方晶胞沿x、y或z轴的投影图如图所示,晶体中H2O的配位数为

(6)一种由镍、氟、钾三种元素组成的化合物晶胞结构如图所示,原子A、B之间的距离是

您最近一年使用:0次
解题方法
8 . 头孢克肟(Cefixime)为口服用的第三代头孢菌素类抗生素,适用于治疗敏感菌所致的呼吸、泌尿和胆道等部位的感染。其结构简式如图所示,下列说法正确的是


| A.头孢克肟中C、H、O、N四种元素的电负性大小为N>O>C>H |
B.头孢克肟中C原子的杂化方式有两种,N原子的杂化方式只有 |
| C.1mol头孢克肟最多能与2mol NaOH反应 |
D.头孢克肟的分子式为 |
您最近一年使用:0次
名校
9 . Ⅰ.魔酸(Magic acid)是最早发现的超强酸,由五氟化锑(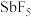 )和氟磺酸(
)和氟磺酸(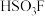 )按体积比
)按体积比 混合制成的混酸,酸性为纯硫酸的1000万倍。
混合制成的混酸,酸性为纯硫酸的1000万倍。
(1)氟磺酸(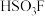 )中元素电负性由大到小的顺序为
)中元素电负性由大到小的顺序为___________ (写汉字名称)。
(2)魔酸根离子中与中心 原子配位的氟磺酸中的原子为
原子配位的氟磺酸中的原子为___________ (填元素符号)。
(3)五氟化锑(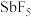 )分子中
)分子中 的杂化类型是下列中的
的杂化类型是下列中的___________ (填字母序号)。
a. b.
b.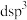 c.
c. d.
d.
Ⅱ.使用超酸可以活化碳氢化合物,如六氟合锑酸( 和
和 的物质的量比
的物质的量比 混合,酸性估计可达无水硫酸的
混合,酸性估计可达无水硫酸的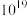 倍)溶液中对甲基环戊烷的羰基化反应。对
倍)溶液中对甲基环戊烷的羰基化反应。对 键的质子化导致失去一个氢气而生成一个碳正离子(其可能发生的重排-碳正离子可能的正电位置并未给出),加入的
键的质子化导致失去一个氢气而生成一个碳正离子(其可能发生的重排-碳正离子可能的正电位置并未给出),加入的 捕获这些碳正离子即生成稳定的酰基碳正离子,它与后处理过程中加入的乙醇发生反应生成相应的乙酯化合物如图所示(超酸中的氢离子用“
捕获这些碳正离子即生成稳定的酰基碳正离子,它与后处理过程中加入的乙醇发生反应生成相应的乙酯化合物如图所示(超酸中的氢离子用“ ”表示)。
”表示)。
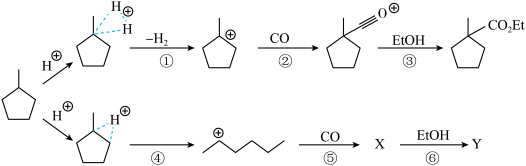
(4)“步骤①”生成的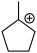 可能发生的碳正离子转移重排,写出“重排”后所得产物“乙酯化合物”的结构简式
可能发生的碳正离子转移重排,写出“重排”后所得产物“乙酯化合物”的结构简式___________ (除题给产物外任写1种)。
(5)步骤③的反应方程式为___________ 。
(6)满足下列条件的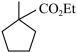 的同分异构体种类有
的同分异构体种类有___________ 种(不考虑立体异构)。
a.存在六元环状结构、且环上只有1~2个侧链
b.能发生银镜反应
c.热氢氧化钠溶液中能水解
(7)Y的系统名称为___________ 。
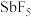 )和氟磺酸(
)和氟磺酸(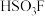 )按体积比
)按体积比 混合制成的混酸,酸性为纯硫酸的1000万倍。
混合制成的混酸,酸性为纯硫酸的1000万倍。(1)氟磺酸(
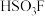 )中元素电负性由大到小的顺序为
)中元素电负性由大到小的顺序为(2)魔酸根离子中与中心
 原子配位的氟磺酸中的原子为
原子配位的氟磺酸中的原子为(3)五氟化锑(
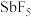 )分子中
)分子中 的杂化类型是下列中的
的杂化类型是下列中的a.
 b.
b.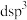 c.
c. d.
d.
Ⅱ.使用超酸可以活化碳氢化合物,如六氟合锑酸(
 和
和 的物质的量比
的物质的量比 混合,酸性估计可达无水硫酸的
混合,酸性估计可达无水硫酸的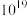 倍)溶液中对甲基环戊烷的羰基化反应。对
倍)溶液中对甲基环戊烷的羰基化反应。对 键的质子化导致失去一个氢气而生成一个碳正离子(其可能发生的重排-碳正离子可能的正电位置并未给出),加入的
键的质子化导致失去一个氢气而生成一个碳正离子(其可能发生的重排-碳正离子可能的正电位置并未给出),加入的 捕获这些碳正离子即生成稳定的酰基碳正离子,它与后处理过程中加入的乙醇发生反应生成相应的乙酯化合物如图所示(超酸中的氢离子用“
捕获这些碳正离子即生成稳定的酰基碳正离子,它与后处理过程中加入的乙醇发生反应生成相应的乙酯化合物如图所示(超酸中的氢离子用“ ”表示)。
”表示)。
(4)“步骤①”生成的
 可能发生的碳正离子转移重排,写出“重排”后所得产物“乙酯化合物”的结构简式
可能发生的碳正离子转移重排,写出“重排”后所得产物“乙酯化合物”的结构简式(5)步骤③的反应方程式为
(6)满足下列条件的
 的同分异构体种类有
的同分异构体种类有a.存在六元环状结构、且环上只有1~2个侧链
b.能发生银镜反应
c.热氢氧化钠溶液中能水解
(7)Y的系统名称为
您最近一年使用:0次
10 . M、X、Y、Z四种短周期主族元素,M为金属元素,X、Y和Z为非金属元素,原子序数Z<X<M<Y。M在常压下可生成 :
: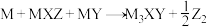 ,其中
,其中 为无色无味气体,反应消耗
为无色无味气体,反应消耗 的同时可获得标准状况下
的同时可获得标准状况下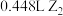 ,
, 可表示成
可表示成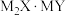 形式。下列说法正确的是
形式。下列说法正确的是
 :
: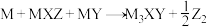 ,其中
,其中 为无色无味气体,反应消耗
为无色无味气体,反应消耗 的同时可获得标准状况下
的同时可获得标准状况下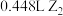 ,
, 可表示成
可表示成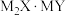 形式。下列说法正确的是
形式。下列说法正确的是| A.基态M原子核外电子空间运动状态有6种 |
| B.电负性:X<Y |
C.Z与X能组合成非极性分子 |
D. 与水反应能得到含有离子键和极性共价键的产物 与水反应能得到含有离子键和极性共价键的产物 |
您最近一年使用:0次



